
科目: 来源:2016届浙江省温州市高三上学期返校联考化学试卷(解析版) 题型:选择题
H2O2(l)在有MnO2条件下和无MnO2条件下分解的能量变化如图所示。下列说法正确是
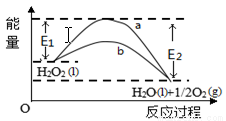
A.有MnO2条件下的反应曲线是a曲线
B.a曲线变为b曲线,反应的活化分子百分数增大
C.a曲线变为b曲线,平衡时H2O2的转化率增大
D.b曲线的热化学方程式为:H2O2(l) =H2O(l) +1/2O2(g) ΔH= - ( E1 - E2 )KJ •mol-1
查看答案和解析>>
科目: 来源:2016届浙江省温州市高三上学期返校联考化学试卷(解析版) 题型:选择题
装置(Ⅰ)为铁镍(Fe-Ni)可充电电池:Fe+NiO2+2H2O  Fe(OH)2+Ni(OH)2;装置(Ⅱ)为电解示意图。当闭合开关K时,Y附近溶液先变红。下列说法正确的是
Fe(OH)2+Ni(OH)2;装置(Ⅱ)为电解示意图。当闭合开关K时,Y附近溶液先变红。下列说法正确的是
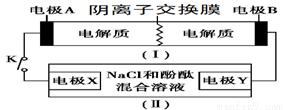
A.闭合K时,X的电极反应式为:2H++2e-= H2↑
B.闭合K时,A电极反应式为:NiO2+2e-+2H+= Ni(OH)2
C.给装置(Ⅰ)充电时,B极参与反应的物质被氧化
D.给装置(Ⅰ)充电时,OH- 通过阴离子交换膜,移向A电极
查看答案和解析>>
科目: 来源:2016届浙江省温州市高三上学期返校联考化学试卷(解析版) 题型:填空题
I.(7分)请回答:
(1)CO2的电子式 。
(2)钠燃烧不能用CO2灭火,用化学方程式表示其理由 。
(3)重晶石(BaSO4)不溶于酸,用饱和Na2CO3处理转化为易溶于酸的BaCO3,写出反应的离子方程式 。
(4)完成以下氧化还原反应的离子方程式:
( )Cr2O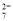 + ( )H2O2+ _____ =( ) Cr3++ ( ) O2 ↑ + ________
+ ( )H2O2+ _____ =( ) Cr3++ ( ) O2 ↑ + ________
II.(8分)化合物K3Fe(A2B4)3·3H2O是重要的催化剂。将化合物K3Fe(A2B4)3·3H2O受热完全分解,只得到气体产物和固体产物。经分析,气体产物只有甲、乙和水蒸气。已知甲、乙均由A、B两元素组成,且摩尔质量:M(甲)<M(乙)。A元素的最外层电子数是次外层电子数2倍,B元素的主族序数是其所在周期数的3倍。经分析,固体产物只有Fe、FeO 和K2AB3。某同学再进行以下定量分析。
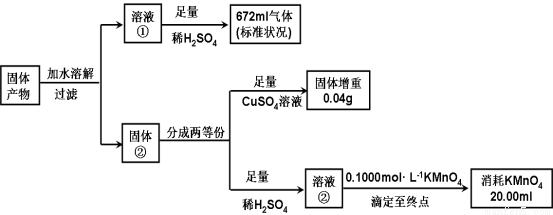
(1)甲的化学式: 。
(2)溶液②与KMnO4发生氧化还原的离子方程式: 。
(3)由以上实验数据的分析可知n(Fe):n(FeO) :n(K2AB3) = : : 。
(4)某同学认为:溶液②由紫红色变为无色,振荡试样半分钟内不变色,即可证明溶液②与KMnO4溶液反应到达滴定终点。判断该同学设想的合理性并说明理由 。
查看答案和解析>>
科目: 来源:2016届江苏省无锡市高三上学期10月月考化学试卷(解析版) 题型:选择题
下列有关化学用语表示正确的是
A. 中子数为20的氯原子: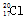
B. 苯的结构简式:C6H6
C. 硅的原子结构示意图: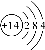
D. Na2S的电子式:
查看答案和解析>>
科目: 来源:2016届江苏省无锡市高三上学期10月月考化学试卷(解析版) 题型:选择题
设NA表示阿伏加德罗常数的值。下列说法正确的是
A. 17.6 g丙烷中所含的共价键数目为4NA
B. 常温下,pH=13的NaOH溶液中含有的OH-离子数目为0.1NA
C. 标准状况下,5.6 L NO和5.6 L O2混合后的分子总数目为0.5NA
D. 电解精炼铜时,若阳极质量减少64 g,则阴极得到电子的数目为2NA
查看答案和解析>>
科目: 来源:2016届江苏省无锡市高三上学期10月月考化学试卷(解析版) 题型:选择题
X、Y、Z、W、R是原子序数依次增大的短周期主族元素,X是原子半径最小的元素,Y的最高正价与最低负价的代数和为0,Z的二价阳离子与氖原子具有相同的核外电子排布,W原子最外层电子数是最内层电子数的3倍。下列说法正确的是
A. X与Y形成的化合物只有一种
B. R的氢化物的热稳定性比W的强
C. 原子半径:r(Z)<r(R)
D. Y的最高价氧化物的水化物的酸性比W的强
查看答案和解析>>
科目: 来源:2016届江苏省无锡市高三上学期10月月考化学试卷(解析版) 题型:选择题
下列根据实验操作和现象所得出的结论正确的是
选项 | 实验操作 | 实验现象 | 结论 |
A | Ag2CO3白色悬浊液中加入Na2S溶液 | 沉淀变为黑色 | Ksp(Ag2S)>Ksp(Ag2CO3) |
B | 向苯酚钠溶液中通入CO2 | 溶液变浑浊 | 碳酸的酸性比苯酚强 |
C | 向蛋白质溶液中加入甲醛和(NH4)2SO4饱和溶液 | 均有白色沉淀 | 蛋白质均发生了变性 |
D | 向溶液X中加入Na2O2粉末 | 出现红褐色沉淀和无色气体 | X中一定含有Fe3+ |
查看答案和解析>>
科目: 来源:2016届江苏省无锡市高三上学期10月月考化学试卷(解析版) 题型:填空题
(12分)利用铝灰(主要成分为Al、Al2O3、AlN、FeO等)制备铝鞣剂[主要成分为Al(OH)2Cl]的一种工艺如下:
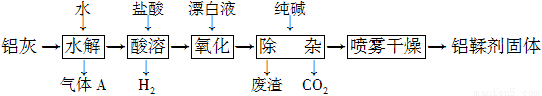
(1)气体A能使湿润的红色石蕊试纸变蓝。铝灰在90 ℃水解生成A的化学方程式为____________。“水解”采用90 ℃而不在室温下进行的原因是________________。
(2)“酸溶”时,Al2O3发生反应的离子方程式为 。
(3)“氧化”时,发生反应的离子方程式为 。
(4)“废渣”成分为______________(填化学式)。
(5)采用喷雾干燥而不用蒸发的原因是 。
查看答案和解析>>
科目: 来源:2016届江苏省无锡市高三上学期10月月考化学试卷(解析版) 题型:填空题
(14分)以硫铁矿(主要成分为FeS2)为原料制取硫酸,其烧渣可用来炼铁。
(1)煅烧硫铁矿时发生反应:FeS2+O2―→Fe2O3+SO2(未配平)。当产生448 L(标准状况)SO2时,消耗O2的物质的量为____________。
(2)Fe2O3用CO还原焙烧的过程中,反应物、生成物和温度之间的关系如图所示。
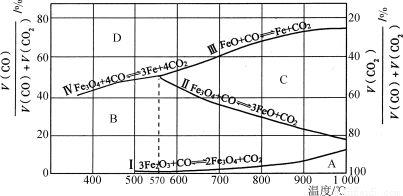
(图中Ⅰ、Ⅱ、Ⅲ、Ⅳ四条曲线是四个化学反应平衡时的气相组成对温度作图得到的;A、B、C、D四个区域分别是Fe2O3、Fe3O4、FeO、Fe稳定存在的区域)
已知:3Fe2O3(s)+CO(g)===2Fe3O4(s)+CO2(g);ΔH1=a kJ·mol-1
Fe3O4(s)+CO(g)===3FeO(s)+CO2(g);ΔH2=b kJ·mol-1
FeO(s)+CO(g)===Fe(s)+CO2(g);ΔH3=c kJ·mol-1
① 反应Fe2O3(s)+3CO(g)===2Fe(s)+3CO2(g)的ΔH=____________kJ·mol-1(用含a、b、c的代数式表示)。
② 800 ℃时,混合气体中CO2体积分数为40%时,Fe2O3用CO还原焙烧反应的化学方程式为__________________。
③ 据图分析,下列说法正确的是___________ (填字母)。
a. 温度低于570℃时,Fe2O3还原焙烧的产物中不含FeO
b. 温度越高,Fe2O3还原焙烧得到的固体物质组成中Fe元素的质量分数越高
c. Fe2O3还原焙烧过程中及时除去CO2有利于提高Fe的产率
(3) FeS2是Li/FeS2电池(示意图如图)的正极活性物质。
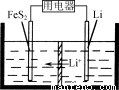
① FeSO4、Na2S2O3、S及H2O在200 ℃时以等物质的量连续反应24 h后得到FeS2。写出该反应的离子方程式: 。
② Li/FeS2电池的负极是金属Li,电解液是含锂盐的有机溶液。电池放电反应为FeS2+4Li===Fe+4Li++2S2-。该反应可认为分两步进行:第1步,FeS2+2Li===2Li++FeS22-,则第2步正极的电极反应式为____________________。
查看答案和解析>>
科目: 来源:2015-2016学年湖北省黄石市高一上学期10月月考化学试卷(解析版) 题型:选择题
对于相同物质的量的SO2和SO3,下列说法中正确的是
A.原子总数之比为1∶1
B.质量之比为1∶1
C.氧元素的质量比为1∶1
D.分子数之比为1∶1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com