
科目: 来源:2015-2016学年湖北省高二上学期10月月考化学试卷(解析版) 题型:填空题
(8分)已知在25℃时,醋酸、碳酸和亚硫酸的电离平衡常数如下表:
醋酸 | 碳酸 | 亚硫酸 |
Ka= 1.75×10-5 | Ka1= 4.30×10-7 Ka2 = 5.61×10-11 | Ka1= 1.54×10-2 Ka2 = 1.02×10-7 |
(1)写出碳酸的第一步电离平衡常数表达式:Ka1 = 。
(2)在相同条件下,试比较H2CO3、HCO3-和HSO3-的酸性强弱: > > 。
(3)下图表示常温时稀释醋酸、碳酸两种酸的稀溶液时,溶液PH随水量的变化
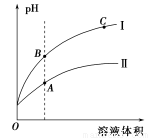
①图像中,曲线I表示的酸是 (填化学式)。
②A、B、C三点中,水的电离程度最大的是 (填字母)。
查看答案和解析>>
科目: 来源:2016届山西省校高三上学期阶段性考试化学试卷(解析版) 题型:选择题
下列叙述正确的是
A.煤的干馏和石油的分馏均属化学变化时,煤的气化和液化属于物理变化
B.溶液和胶体的本质区别是丁达尔效应
C.有单质参加和生成的化学反应一定是氧化还原反应
D.将浓度为18.4mol/L质量分数为98%的浓硫酸加水稀释至9.2 mol/L,则稀释后溶质的质量分数大于49 %
查看答案和解析>>
科目: 来源:2016届山西省校高三上学期阶段性考试化学试卷(解析版) 题型:选择题
下列几种溶液中的指定离子:①NaHCO3溶液中的HCO3-;②Na2SO3溶液中的SO32-;③NaHCO3和Na2CO3混合溶液中的CO32-;④CH3COONa溶液中的CH3COO-;⑤饱和氢氧化钠溶液中的Na+,向其中加入足量的过氧化钠固体后,忽略溶液体积变化,恢复到原温度,离子浓度基本保持不变的是
A.②和③ B.③和④ C.④和⑤ D.①和③
查看答案和解析>>
科目: 来源:2016届山西省校高三上学期阶段性考试化学试卷(解析版) 题型:选择题
下列除去杂质所选用的试剂或方法完全正确的是
A.除去NaCl溶液中的少量I2:用无水乙醇,萃取分液
B.除 CO2中的少量HCl:通入饱和Na2CO3溶液,洗气
C.镁粉中混有少量铝粉:加入过量烧碱溶液充分反应,过滤、洗涤、干燥
D.除去NaHCO3固体中的少量Na2CO3:加热灼烧
查看答案和解析>>
科目: 来源:2016届山西省校高三上学期阶段性考试化学试卷(解析版) 题型:选择题
CO2与H2的混合气体5g,在150℃时和足量的氧气混合,用电火花充分引燃,在相同状况下,再将反应后所得混合气体通入到足量的Na2O2中,测得Na2O2固体增重的质量为3.4g,则原混合气体中CO2的物质的量分数为
A.25% B.75% C.88% D.32%
查看答案和解析>>
科目: 来源:2016届山西省校高三上学期阶段性考试化学试卷(解析版) 题型:选择题
某溶液中含有的溶质是FeBr2、FeI2,若先向该溶液中通入一定量的氯气,再向反应后的溶液中滴加KSCN溶液,溶液变为红色,则下列叙述正确的是
①原溶液中的Br - 一定被氧化;
②通入氯气之后,原溶液中的Fe2+一定有部分或全部被氧化;
③不能确定通入氯气后的溶液中是否存在Fe2+;
④若取少量所得溶液,再加入CCl4溶液充分振荡,静置、分液,向上层溶液中加入足量AgNO3溶液,只产生白色沉淀,说明原溶液中的Fe2+,Br - ,I-均被完全氧化
A.①②③ B.②③④ C.①③④ D.①②③④
查看答案和解析>>
科目: 来源:2016届山西省校高三上学期阶段性考试化学试卷(解析版) 题型:实验题
实验室用氯化钠固体配制1.00mol/L的NaCl溶液0.5L,回答下列问题
(1)根据计算,需称取氯化钠 g。
(2)配制时,必须用到的玻璃仪器有 。
(3)配制溶液有下列几步操作:a.溶解,b.摇匀,c.洗涤,d.冷却,e.称量,f.将溶液移至容量瓶,g.贴标签,h.定容。正确的操作顺序是 。
(4)下列操作结果使溶液物质的量浓度偏低的是 。
A.没有将洗涤液转入容量瓶中 B.容量瓶洗涤后,未经干燥处理
C.定容时,俯视容量瓶的刻度线 D.加水定容时,水的量超过了刻度线
查看答案和解析>>
科目: 来源:2016届山西省校高三上学期阶段性考试化学试卷(解析版) 题型:填空题
取 A、B 两份物质的量浓度相等的 NaOH 溶液,体积均为 50mL,分别向其中通入一定量的 CO2后,再分别稀释为 100mL。
(1)在 NaOH 溶液中通入一定量的 CO2后,溶液中溶质的组成可能是:(填化学式)①__________②___________③____________④______________。
(2)在稀释后的溶液中分别逐滴加 0.1mol/L 的盐酸,产生的 CO2 的体积(标准状况)与所加盐酸的体积关系如图所示:
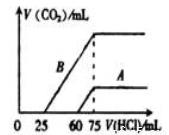
①分别加入足量的盐酸后,溶液中的溶质是_____________,原 NaOH 溶液的物质的量浓度为_________。
②A 曲线表明,原溶液通入CO2后,所得溶质的化学式为_________,与盐酸反应 产生 CO2的最大体积是_________mL(标准状况)。
③B 曲线表明,原溶液通入 CO2后,所得溶质的化学式为_________,其物质的量 之比为_________。
查看答案和解析>>
科目: 来源:2016届山西省校高三上学期阶段性考试化学试卷(解析版) 题型:填空题
(一)氧化还原反应中实际上包含氧化和还原两个过程。下面是一个发生还原过程的反应式:
NO3ˉ+4H++3e-→ NO+2H2O
在下列四种物质KMnO4、Na2CO3、KI、Fe2(SO4)3中的一种物质(甲)中滴加少量稀硝酸能使上述还原过程发生。
(1)写出并配平该氧化还原反应的化学方程式:
(2)上述反应中 被还原,还原剂是 。
(3)反应生成0.3mol H2O,则转移电子的数目为 个。
(二)请配平下面方程式
CH3CH2OH+ KMnO4→ CH3CHO+ MnO2+ KOH+ H2O
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com