
科目: 来源:2015-2016学年甘肃兰州一中高二上期中测试理科化学试卷(解析版) 题型:选择题
下图曲线a表示放热反应X(g)+Y(g) Z(g)+M(g)+N(s)进行过程中X的转化率随时间变化的关系。若要改变起始条件,使反应过程按b曲线进行,可采取的措施是
Z(g)+M(g)+N(s)进行过程中X的转化率随时间变化的关系。若要改变起始条件,使反应过程按b曲线进行,可采取的措施是
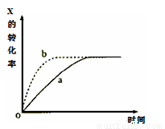
A.减小体积 B.加大X的投入量
C.减压 D.升高温度
查看答案和解析>>
科目: 来源:2015-2016学年甘肃兰州一中高二上期中测试理科化学试卷(解析版) 题型:选择题
某温度下在密闭容器中发生反应2M(g)+N(g) 2E(g),若开始时只充入2mol E(g),达平衡时,混合气体的压强比起始时增大了10%;若开始只充入2mol M和1mol N混合气体,达平衡时M的转化率为
2E(g),若开始时只充入2mol E(g),达平衡时,混合气体的压强比起始时增大了10%;若开始只充入2mol M和1mol N混合气体,达平衡时M的转化率为
A.20% B.60% C.80% D.90%
查看答案和解析>>
科目: 来源:2015-2016学年甘肃兰州一中高二上期中测试理科化学试卷(解析版) 题型:选择题
下列叙述正确的是
A.95℃纯水的pH<7,说明加热可导致水呈酸性
B.pH=13的氨水溶液稀释至10倍后pH=12
C.0.2 mol/L的盐酸与等体积水混合后pH=1
D.pH=12的氨水溶液与pH=2的盐酸等体积混合后pH=7
查看答案和解析>>
科目: 来源:2015-2016学年甘肃兰州一中高二上期中测试理科化学试卷(解析版) 题型:选择题
下列溶液中导电性最强的是
A.1L0.1mol/L醋酸 B.0.1L 0.1mol/L H2SO4溶液
C.0.5L 0.1mol/L盐酸 D.2L 0.1mol/L H2SO3溶液
查看答案和解析>>
科目: 来源:2015-2016学年甘肃兰州一中高二上期中测试理科化学试卷(解析版) 题型:选择题
在恒温条件下,有甲、乙两容器,甲容器为体积不变的密闭容器,乙容器为一个恒压的密闭容器,两容器起始状态完全相同,都充有C气体,若发生可逆反应C(g) A(g)+B(g),经一段时间后,甲、乙两容器反应都达到平衡。下列说法中正确的是
A(g)+B(g),经一段时间后,甲、乙两容器反应都达到平衡。下列说法中正确的是
A.平均反应速度:乙>甲 B.平衡时C的物质的量甲>乙
C.平衡时C的转化率:乙<甲 D.平衡时A的物质的量甲>乙
查看答案和解析>>
科目: 来源:2015-2016学年甘肃兰州一中高二上期中测试理科化学试卷(解析版) 题型:选择题
pH相同的氨水、氢氧化钠和氢氧化钡溶液,分别用蒸馏水稀释到原来的X倍、Y倍、Z倍,稀释后三种溶液的pH相同,则X、Y、Z的关系是
A.X=Y=Z B.X>Y=Z C.X<Y=Z D.X=Y<Z
查看答案和解析>>
科目: 来源:2015-2016学年甘肃兰州一中高二上期中测试理科化学试卷(解析版) 题型:选择题
在温度、容积相同的3个密闭容器中,按不同方式投入反应物,保持恒温、恒容,测得反应达到平衡时的有关数据如下(已知N2(g)+3H2(g) 2NH3(g)△H=-92.4kJ/mol)
2NH3(g)△H=-92.4kJ/mol)
容器 | 甲 | 乙 | 丙 |
反应物投入量 | 1mol N2、3mol H2 | 2mol NH3 | 4mol NH3 |
NH3的浓度(mol·L-1) | c1 | c2 | c3 |
反应的能量变化 | 放出akJ | 吸收bkJ | 吸收ckJ |
体系压强(Pa) | p1 | p2 | p3 |
反应物转化率 | α1 | α2 | α3 |
下列说法正确的是
A.2 c1>c3 B.a+b=92.4 C.2 p1<p3 D.α1+α2>1
查看答案和解析>>
科目: 来源:2015-2016学年甘肃兰州一中高二上期中测试理科化学试卷(解析版) 题型:填空题
(10分)FeCl3 具有净水作用,但腐蚀设备,而聚合氯化铁是一种新型的絮凝剂,处理污水比FeCl3 高效,且腐蚀性小。请回答下列问题:
(1)FeCl3 净水的原理是 。FeCl3溶液腐蚀钢铁设备,除H+作用外,另一主要原因是(用离子方程式表示) 。
(2)为节约成本,工业上用NaClO3 氧化酸性FeCl2 废液得到FeCl3。
①若酸性FeCl2 废液中c(Fe2+)=2.0×10-2mol·L-1, c(Fe3+)=1.0×10-3mol·L-1, c(Cl-)=5.3×10-2mol·L-1,则该溶液的pH约为 。
②完成NaClO3 氧化FeCl2 的离子方程式:_____ClO3-+______Fe2++______ =_____Cl-+_____Fe3++______
(3)FeCl3 在溶液中分三步水解:Fe3++H2O Fe(OH)2++H+ K1
Fe(OH)2++H+ K1
Fe(OH)2++H2O Fe(OH)2++H+ K2 Fe(OH)++H2O
Fe(OH)2++H+ K2 Fe(OH)++H2O Fe(OH)3+H+ K3
Fe(OH)3+H+ K3
通过控制条件,以上水解产物聚合,生成聚合氧化铁,离子方程式为:
xFe3++yH2O Fex(OH)y(3x-y)++yH+,欲使平衡正向移动可采用的方法是(填序号) 。
Fex(OH)y(3x-y)++yH+,欲使平衡正向移动可采用的方法是(填序号) 。
a.降温 b.加水稀释 c.加入NH4Cl d.加入NaHCO3
查看答案和解析>>
科目: 来源:2016届吉林省高三上学期第一次模拟化学试卷(解析版) 题型:选择题
在100 mL HNO3和H2SO4混合溶液中,两种酸物质的量浓度之和为0.60 mol/L。向该溶液中加入足量的铜粉,加热,充分反应后,所得溶液中Cu2+的物质的量浓度最大为
A.0.225 mol/L B.0.36 mol/L C.0.30 mol/L D.0.45 mol/L
查看答案和解析>>
科目: 来源:2016届吉林省高三上学期第一次模拟化学试卷(解析版) 题型:选择题
为了测定某镁铝合金的成分,取14.7 g合金完全溶于500 mL 3 mol/L的硫酸中,再加入400 mL 8 mol/L的氢氧化钠溶液充分反应,最后只产生一种沉淀。则关于该合金的测定过程的描述正确的是
A.该合金中含有铝的质量至少为5.4 g
B.合金中镁的质量分数为63.3%≤Mg%<100%
C.在产生沉淀后的溶液中一定含有0.2 mol NaAlO2
D.在产生沉淀后的溶液中有1.6 mol Na2SO4
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com