
科目: 来源:2016届甘肃省高三上学期第二次检测化学试卷(解析版) 题型:选择题
下列离子方程式正确的是
A.氯气溶解于水:Cl2+H2O =HClO+Cl-+H+
B.沸水中滴入饱和FeCl3 溶液,溶液呈红褐色:Fe3++3H2O= Fe(OH)3↓+3H+
C.醋酸钠溶液显碱性:CH3COO-+H2O =CH3COOH+OH-.
D、久置的H2S 溶液变浑浊:2S2-+O2+4H+ =2S↓+2H2O
查看答案和解析>>
科目: 来源:2016届甘肃省高三上学期第二次检测化学试卷(解析版) 题型:选择题
已知25 ℃下,Ka(HCOOH)=1.78×10-4,Kb(NH3·H2O)=1.79×10-5。保持25 ℃不变,向一定体积0.1 mol·L-1 的氨水中滴加0.1 mol·L-1 的甲酸溶液。在滴加过程中
A.水的电离常数先增大后减小
B.当氨水和甲酸溶液体积相等时,c(HCOO-)=c(NH4+)
C.c(NH3·H2O)与c(NH4+)之和始终保持不变
D. 始终保持不变
始终保持不变
查看答案和解析>>
科目: 来源:2016届甘肃省高三上学期第二次检测化学试卷(解析版) 题型:填空题
【化学与技术】钛铁矿的主要成分可表示为FeTiO3(Ti 为+4 价),某钛铁矿中含FeTiO3 为76%。钛白粉在涂料、塑料、油墨、造纸等行业具有广泛的用途,钛白粉的主要成分为TiO2。利用该钛铁矿生产钛白粉及绿矾的工艺流程如下:
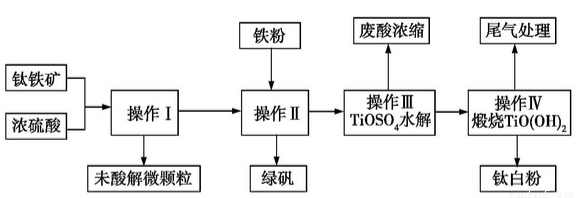
(1)若钛铁矿与浓硫酸反应时Ti 的转化率为92%,操作Ⅰ~Ⅳ中Ti 的转化率均为96%,则1t 该矿石可生产钛白粉(TiO2) t (计算结果保留两位小数,下同),能否计算生成的绿矾(FeSO4·7H2O)的质量? (能则写出计算结果,不能则说明理由)。
(2)钛铁矿与硫酸的反应可表示为FeTiO3+H2SO4 →TiOSO4+X+H2O(未配平)。其中X的化学式为 。
(3)操作Ⅰ的名称是 ,操作Ⅱ包括冷却结晶、 。操作Ⅱ中加入铁粉的目的是 (用离子方程式表示)。
(4)写出操作Ⅲ中TiOSO4水解的化学方程式: 。
查看答案和解析>>
科目: 来源:2016届甘肃省高三上学期第二次检测化学试卷(解析版) 题型:实验题
某校化学课外研究小组为研究浓硫酸与金属M 反应的气体生成物,进行了下列实验活动:
【提出假设】
假设1:气体生成物只有SO2;
假设2:气体生成物只有H2;
假设3: 。
【实验验证】
实验装置及实验中使用的试剂如图:
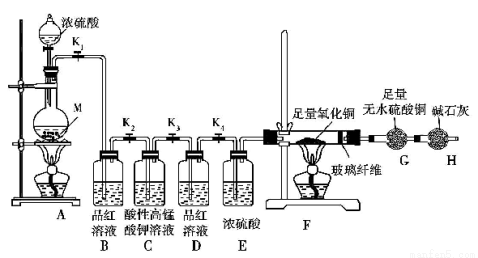
(1)在装入药品前,甲同学检查装置A 的气密性,方法是 。
(2)乙同学通过所学知识排除了上面提出的一个假设,他排除的是假设 ,理由是 。
(3)如果实验中观察到装置B 中溶液褪色,装置F 和装置G 中无明显变化,则假设 成立,实验测得消耗金属M 和浓硫酸的物质的量之比为1∶2,则在M 的硫酸盐中,M 元素的化合价为 。
(4)如果假设3 正确,填写下表中的实验现象:

(5)装置C 的作用是 ,装置D 的作用是 。
(6)如果装置A 中放入的金属M 的质量为11.2 g,加入适量浓硫酸,反应完成后,装置B中溶液褪色,装置A 中金属无剩余;反应后G 的质量增加了0.9 g;取少量装置A 中溶液稀释,分为两份,一份滴加KSCN 溶液,溶液变红色,另一份滴加酸性KMnO4 溶液,溶液褪色。如果装置A 中溶液内的金属离子浓度相等,则装置A 中烧瓶内发生反应的总化学方程式是 。
查看答案和解析>>
科目: 来源:2016届福建省莆田市高三上学期第一次月考化学试卷(解析版) 题型:选择题
下面对氯气的叙述正确的是
A.氯气可使湿润的红布条褪色,所以氯气具有漂白性
B.氯气没有漂白性,但通入品红溶液中,品红褪色
C.过量的铜在氯气中燃烧可生成氯化亚铜
D.闻其气味时要小心的将集气瓶放在鼻孔下直接闻
查看答案和解析>>
科目: 来源:2016届福建省莆田市高三上学期第一次月考化学试卷(解析版) 题型:选择题
已知氧化剂、稀酸等都能迅速破坏传染病毒活性而杀死病毒,下列物质不能作为常用消毒剂的是
A.H2O2溶液 B.NaClO溶液 C.SO2 D.醋酸
查看答案和解析>>
科目: 来源:2016届福建省莆田市高三上学期第一次月考化学试卷(解析版) 题型:选择题
下列实验现象,与新制氯水中的某些成分(括号内物质)没有关系的是
A.将NaHCO3固体加入新制氯水,有无色气泡生成(H+)
B.使红色布条褪色(HClO)
C.向NaBr溶液中滴加氯水,再滴加CCl4,发现下层为橙红色(HCl)
D.滴加AgNO3溶液生成白色沉淀(Cl-)
查看答案和解析>>
科目: 来源:2016届福建省莆田市高三上学期第一次月考化学试卷(解析版) 题型:选择题
某纯碱厂技术科的人员对该厂纯碱样品的质量进行检验。其中能够说明纯碱样品中可能含有杂质(NaHCO3)的实验是
①样品溶于水,并加入足量的澄清石灰水,变浑浊
②样品溶于水,并加入足量的BaCl2溶液,变浑浊
③样品在硬质试管中加强热,排出的气体通入澄清石灰水,变浑浊
④向样品中滴加稀盐酸,排出的气体通入澄清石灰水,变浑浊
A.①②③ B.①③④ C.①②④ D.只有③
查看答案和解析>>
科目: 来源:2016届福建省莆田市高三上学期第一次月考化学试卷(解析版) 题型:选择题
建筑用的红砖和青砖,其颜色是由其中含有的不同价态的铁氧化物所致。我国古代砖瓦建筑能够保持到现在的,几乎无一例外的是由青砖建成。有人提出以下可能的原因:
①青砖中含的是FeO;②青砖中含的是Fe3O4;③Fe2O3遇长期酸雨侵蚀会风化溶解使砖瓦强度降低;④Fe3O4性质稳定;⑤FeO性质稳定。你认为有道理的是
A.①③⑤ B.②③④ C.③⑤ D.①②③④⑤
查看答案和解析>>
科目: 来源:2016届福建省莆田市高三上学期第一次月考化学试卷(解析版) 题型:选择题
为了证明硫酸亚铁铵[(NH4)2Fe(SO4)·26H2O]晶体的成分中含有NH4+、Fe2+、SO42-和H2O,下列实验叙述中不正确的是
A.取少量硫酸亚铁铵晶体放入试管中,加热,试管口有液体生成,则可证明晶体的成分中含有结晶水
B.取少量硫酸亚铁铵晶体放入试管,加浓NaOH溶液,加热,试管口湿润的蓝色石蕊试纸变红,则可证明晶体的成分中含有NH4+
C.取适量硫酸亚铁铵晶体溶于水,加少量稀盐酸,无现象,再滴入几滴BaCl2溶液,有白色沉淀生成,则可证明晶体的成分中含有SO42-
D.取适量硫酸亚铁铵晶体溶于水,得浅绿色溶液,滴入2滴KSCN溶液,溶液不显血红色,再滴入几滴新制氯水,溶液变为血红色,则可证明晶体的成分中含有Fe2+
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com