
科目: 来源:2016届河南省八市高三9月教学质量监测考试化学试卷(解析版) 题型:选择题
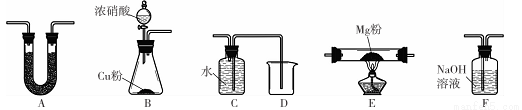
已知25℃时:①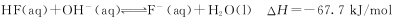
②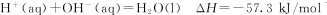 下列有关说法中正确的是
下列有关说法中正确的是
A.HF电离:HF(aq)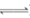 H+(aq)+F-(aq)△H=+10.4KJ/mol
H+(aq)+F-(aq)△H=+10.4KJ/mol
B.水解消耗0.1 mol F时,吸收的热量为6.77 kJ
C.中和热均为57.3 kJ/mol
D.含0.1 mol HF、0.1 mol NaOH的两种溶液混合后放出的热量为6.77 kJ
查看答案和解析>>
科目: 来源:2016届河南省八市高三9月教学质量监测考试化学试卷(解析版) 题型:实验题
(12分)Mg能在NO2中燃烧,产物为Mg3N2、MgO和N2。某科学小组通过实验验证反应产物并探究产物的比例关系。资料信息:
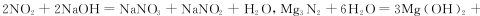
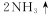
限用如下装置实验(夹持装置省略,部分仪器可重复使用)
(1)装置连接的顺序为 (填字母序号);
(2)连接好仪器,装入药品前检验装置气密性的方法是____;
(3)装置A中盛装的干燥剂是 ;装置F的作用__ __;
(4)验证产物中存在Mg3 N2的具体实验操作为 .确定产物中有N。生成的实验现象为 ;
(5)已知装置E中初始加入Mg粉质量为13.2 g,在足量的NO2中充分燃烧,实验结束后,硬质玻璃管冷却至室温、称量,测得硬质玻璃管中剩余固体的质量为21.0 g,产生N2的体积为1120 mL(标准状况)。写出玻璃管中发生反应的化学方程式:_ _。
查看答案和解析>>
科目: 来源:2016届河南省濮阳市心高三上第一次市统摸底化学试卷(解析版) 题型:选择题
下列表示对应反应的离子方程式正确的是
A.向稀 HNO3 中滴加 Na2SO3 溶液:SO32-+2H+=== SO2↑+H2O
B.双氧水中加入稀硫酸和KI溶液: H2O2+ 2I-+2H+=I2+ 2H2O
C.向 Al2(SO4)3 溶液中加入过量 NH3•H2O:Al3++4NH3•H2O === AlO2-+ 4NH4+ + 2H2O
D.醋酸除去水垢:2H++CaCO3=Ca2++ CO2↑+ H2O
查看答案和解析>>
科目: 来源:2016届河南省濮阳市心高三上第一次市统摸底化学试卷(解析版) 题型:选择题
下列关于普伐他汀的水解产物(结构简式如下图)的说法正确的是
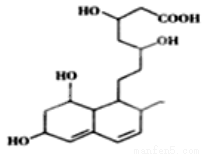
A.含有两种官能团
B.能发生加成、酯化、氧化反应
C.1mol该物质与足量Na反应,产生2.5gH2
D.能使溴水和酸性高锰酸钾溶液褪色,褪色原理相同
查看答案和解析>>
科目: 来源:2016届河南省濮阳市心高三上第一次市统摸底化学试卷(解析版) 题型:填空题
(15分)运用化学反应原理研究氮、硫等单质及其化合物的反应有重要意义。
(1)硫酸生产过程中2SO2(g)+O2(g)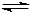 2SO3(g),平衡混合体系中SO3的百分含量和温度的关系如图所示,根据下图回答下列问题:
2SO3(g),平衡混合体系中SO3的百分含量和温度的关系如图所示,根据下图回答下列问题:
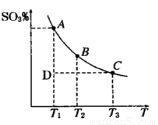
①2SO2(g)+O2(g)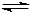 2SO3(g)的△H______0(填“>”或“<”)。
2SO3(g)的△H______0(填“>”或“<”)。
②一定条件下,将SO2与O2以体积比2:1置于一体积不变的密闭容器中发生以上反应,能说明该反应已达到平衡的是___________(填字母编号)。
a.体系的密度不发生变化
b.SO2与SO3的体积比保持不变
c.体系中硫元素的质量百分含量不再变化
d.单位时间内转移4 mol 电子,同时消耗2 mol SO3
e.容器内的气体分子总数不再变化
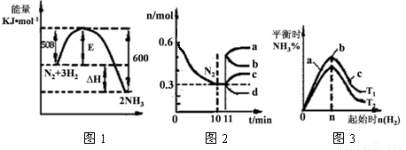
(2)一定的条件下,合成氨反应为:N2(g)+3H2(g)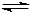 2NH3(g)。图1表示在此反应过程中的能量的变化,图2表示在2L的密闭容器中反应时N2的物质的量随时间的变化曲线。图3表示在其他条件不变的情况下,改变起始物氢气的物质的量对此反应平衡的影响。
2NH3(g)。图1表示在此反应过程中的能量的变化,图2表示在2L的密闭容器中反应时N2的物质的量随时间的变化曲线。图3表示在其他条件不变的情况下,改变起始物氢气的物质的量对此反应平衡的影响。
①该反应的平衡常数表达式为 ,升高温度,平衡常数 (填“增大”或“减小”或“不变”)。
②由图2信息,计算0~10min内该反应的平均速率v(H2)= ,从11min起其它条件不变,压缩容器的体积为1L,则n(N2)的变化曲线为 (填“a”或“b”或“c”或“d”)。
③图3 a、b、c三点所处的平衡状态中,反应物N2的转化率最高的是 点,温度T1 T2(填“>”或“=”或“<”)
(3)若将等物质的量的SO2与NH3溶于水充分反应,所得溶液呈 性,所得溶液中c(H+)- c(OH-)= (填写表达式)(已知:H2SO3:Ka1=1.7×10-2,Ka2=6.0×10-8,NH3·H2O:Kb=1.8×10-5)。
查看答案和解析>>
科目: 来源:2016届河南省濮阳市心高三上第一次市统摸底化学试卷(解析版) 题型:填空题
【选修3:物质结构与性质】(13分)某钙钛型复合氧化物(如图),以A原子为晶胞的顶点,A位可以是Ca、Sr、Ba或Pb,当B位是V、Cr、Mn、Fe时,这种化合物的电阻率在有外磁场作用时较之无外磁场作用时存在巨大变化(巨磁电阻效应)。
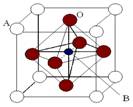
(1)用A、B、O表示这类特殊晶体的化学式 。在图中,与A原子配位的氧原子数目为 。
(2)基态Cr原子的核外电子排布式为 ,其中电子的运动状态有 种。
(3)某些钙钛型复合氧化物能够催化NO直接分解为N2和O2,N和O的基态原子中,未成对的电子数目比为 。
(4)下表是几种碳酸盐的热分解温度和阳离子半径
碳酸盐 | CaCO3 | SrCO3 | BaCO3 |
热分解温度/℃ | 900 | 1172 | 1360 |
阳离子半径/pm | 99 | 112 | 135 |
请解释碳酸钙热分解温度最低的原因:_____________。
(5)用晶体的X射线衍射法可以测得阿伏伽德罗常数。对金属钙的测定得到以下结果:晶胞为面心立方最密堆积,边长为a pm,阿伏加德罗常数的值为NA,金属钙的密度为 g·cm-3(用含a和NA的式子表示)。
查看答案和解析>>
科目: 来源:2016届湖北省高三优录班8月月考化学试卷(解析版) 题型:选择题
某无色溶液含有下列离子中的若干种:H+、NH4+、Fe3+、Ba2+、Al3+、CO32–、Cl–、OH–、NO3–。向该溶液中加入铝粉,只放出H2,则溶液中能大量存在的离子最多有
A.3种 B.4种 C.5种 D.6种
查看答案和解析>>
科目: 来源:2016届湖北省高三优录班8月月考化学试卷(解析版) 题型:选择题
离子方程式2Ca2+ + 3HCO3– + 3OH– = 2CaCO3↓ + CO32– + 3H2O可以表示
①Ca(HCO3)2与NaOH溶液反应
②NaHCO3与澄清石灰水反应
③Ca(HCO3)2与澄清石灰水反应
④NH4HCO3与澄清石灰水反应
A.①②③④ B.①②③ C.①②④ D.①②
查看答案和解析>>
科目: 来源:2016届湖北省高三优录班8月月考化学试卷(解析版) 题型:填空题
(8分) 乙苯催化脱氢制苯乙烯反应:
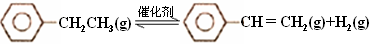
(1)已知:
化学键 | C-H | C-C | C=C | H-H |
键能/kJ·molˉ1 | 412 | 348 | 612 | 436 |
计算上述反应的△H=________ kJ·mol-1。
(2)维持体系总压强p恒定,在温度T时,物质的量为n、体积为V的乙苯蒸汽发生催化脱氢反应。已知乙苯的平衡转化率为α,则在该温度下反应的平衡常数Kp=___________(用α等符号表示)。
(3)工业上,通常在乙苯蒸气中掺混水蒸气(原料气中乙苯和水蒸气的物质的量之比为1︰9),控制反应温度600℃,并保持体系总压为常压的条件下进行反应。在不同反应温度下,乙苯的平衡转化率和某催化剂作用下苯乙烯的选择性(指除了H2以外的产物中苯乙烯的物质的量分数)示意图如下:
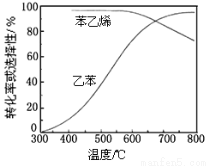
①掺入水蒸气能提高乙苯的平衡转化率,解释说明该事实 ___________。
②控制反应温度为600℃的理由是____________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com