
科目: 来源:2016届江苏省高三上学期第一次月考化学试卷(解析版) 题型:选择题
下列有关实验装置进行的相应实验,能达到实验目的的是
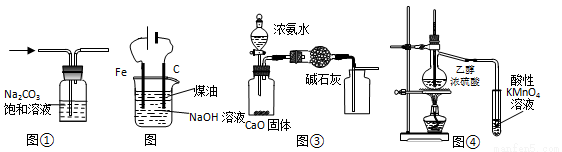
A.图①除去CO2中的HCl
B.图②装置制备Fe(OH)2并能较长时间观察其颜色
C.图③所示装置制取并收集干燥纯净的NH3
D.图④证明CH3CH2OH发生消去反应生成了乙烯
查看答案和解析>>
科目: 来源:2016届江苏省高三上学期第一次月考化学试卷(解析版) 题型:选择题
向一定量的Cu、Fe2O3的混合物中加入100 mL 1 mol·L-1的盐酸,恰好使混合物完全溶解,所得溶液中不含Fe3+,若用过量的CO在高温下还原相同质量的原混合物,固体减少的质量为
A.3.2 g B.2.4 g C.1.6 g D.0.8 g
查看答案和解析>>
科目: 来源:2016届江苏省高三上学期第一次月考化学试卷(解析版) 题型:选择题
研究人员最近发现了一种“水”电池,这种电池能利用淡水与海水之间含盐量差别进行发电,在 海水中电池总反应可表示为:5 MnO2+2 Ag+2 NaCl=Na2Mn5O10+2 AgCl。下列关于“水”电池的说法不正确的是
A.AgCl是还原产物
B.负极的电极反应为:Ag+Cl- — e-=AgCl
C.Na+不断向“水”电池的正极移动
D.每生成1mol Na2Mn5O10转移2mol电子
查看答案和解析>>
科目: 来源:2016届江苏省高三上学期第一次月考化学试卷(解析版) 题型:填空题
(16分)(1)P2O5是非氧化性干燥剂,下列气体不能用浓硫酸干燥,可用P2O5干燥的是______
a.NH3 b.HI c.SO2 d.CO2
(2)KClO3可用于实验室制O2,若不加催化剂,400℃时分解只生成两种盐,其中一种是无氧酸盐,另一种盐的阴阳离子个数比为1∶1。写出该反应的化学方程式:__________
(3)工业生产甲醇的常用方法是:CO(g)+2H2(g) CH3OH(g) △H = —90.8kJ/mol。
CH3OH(g) △H = —90.8kJ/mol。
已知:2H2(g)+O2(g)=2H2O(l) △H = -571.6kJ/mol;
2CO(g)+O2(g)=2CO2(g) △H = -566.0kJ/mol
计算2CH3OH(g)+3O2(g)=2CO2(g)+4H2O(l) △H = 。
(4)某实验小组设计了如图所示的甲醇燃料电池装置。
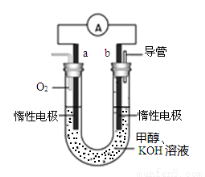
①该电池工作时,负极是 极(填“a”或 “b”);
②工作一段时间后,测得溶液的pH减小,该电池负极反应的离子方程式为 。
(5)电解法促进橄榄石(主要成分是Mg2SiO4)固定CO2的部分工艺流程如下:
已知:Mg2SiO4(s)+4HCl(aq) 2MgCl2(aq)+SiO2 (s)+ 2H2O(l) △H =-49.04 kJ·mol-1
2MgCl2(aq)+SiO2 (s)+ 2H2O(l) △H =-49.04 kJ·mol-1
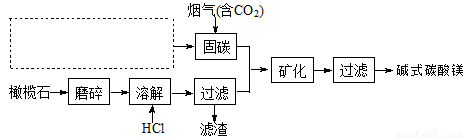
①某橄榄石的组成是Mg9FeSi5O20,用氧化物的形式可表示为 。
②在上图虚框内补充一步工业生产流程 。
③ 经分析,所得碱式碳酸镁产品中含有少量NaCl和Fe2O3。为提纯,可采取的措施依次为:对溶解后所得溶液进行除铁处理、对产品进行洗涤处理。判断产品洗净的操作是 。
查看答案和解析>>
科目: 来源:2016届西藏日喀则地区一中高三10月月考理综化学试卷(解析版) 题型:选择题
镍氢电池(NiMH)目前已经成为混合动力汽车的一种主要电池类型。NiMH中的M表示储氢金属或合金。该电池在充电过程中的总反应方程式是:Ni(OH)2 + M=NiOOH + MH,已知:6NiOOH + NH3 + H2O + OH-=6 Ni(OH)2 + NO2-,下列说法正确的是
A.NiMH电池放电过程中,正极的电极反应式为:NiOOH + H2O + e-= Ni(OH)2 + OH-
B.充电过程中OH-离子从阳极向阴极迁移
C.充电过程中阴极的电极反应式:H2O + M + e-= MH + OH-,H2O中的H被M还原
D.NiMH电池中可以用KOH溶液、氨水等作为电解质溶液
查看答案和解析>>
科目: 来源:2016届西藏日喀则地区一中高三10月月考理综化学试卷(解析版) 题型:实验题
(13分)半导体生产中常需要控制掺杂,以保证控制电阻率,三氯化磷(PCl3)是一种重要的掺杂剂。实验室要用黄磷(即白磷)与干燥的Cl2模拟工业生产制取PCl3,装置如下图所示:(部分夹持装置略去)

已知:
①黄磷与少量Cl2反应生成PCl3,与过量Cl2反应生成PCl5。
②PCl3遇水会强烈水解生成H3PO3和HCl;
③PCl3遇O2会生成POCl3,POCl3溶于PCl3。
④PCl3、POCl3的熔沸点如表:
物质 | 熔点/℃ | 沸点/℃ |
PCl3 | -112 | 75.5 |
POCl3 | 2 | 105.3 |
请回答下列问题:
(1)A装置中制氯气的离子方程式为____________。
(2)B中所装试剂是_______;F中碱石灰的作用有两种,分别是______、_______。
(3)实验时,检查装置气密性后,先打开K3通入干燥的CO2,再迅速加入黄磷。通干燥CO2的作用是_______。
(4)粗产品中常含有POCl3、PCl5等.加入黄磷加热除去PCl5后,通过_____(填实验操作名称),即可得到较纯净的PCl3。
(5)实验结束时,可以利用C中的试剂吸收多余的氯气,C中反应的离子方程式为_______。
(6)通过下面方法可测定产品中PCl3的质量分数:
①迅速称取1.00g产品,加水反应后配成250mL溶液;
②取以上溶液25.00mL,向其中加入10.00mL 0.1000mol/L碘水,充分反应;
③向②所得溶液中加入几滴淀粉溶液,用0.1000mol/L的Na2S2O3,溶液滴定;
④重复②、③操作,平均消耗Na2S2O3溶液8.40mL。
已知:H3PO3+I2=H3PO4+2HI,I2+2Na2S2O3=2NaI+Na2S4O6,假设测定过程中没有其他反应,该产品中PCl3的质量分数为_________。
查看答案和解析>>
科目: 来源:2016届西藏日喀则地区一中高三10月月考理综化学试卷(解析版) 题型:填空题
【化学—化学与技术】(15分)甲酸钠广泛用作催化剂、稳定合成剂、印染行业的还原剂,还可用于生产保险粉、草酸和甲酸。甲酸钠用电石炉废气(75%~90%CO,以及少量CO2、H2S、N2、CH4等)合成,其合成部分工艺流程如下:
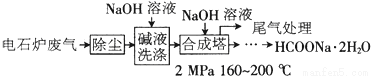
(1)上述工艺用碱液洗涤的目的是___________,可能发生的反应有_______(写两个化学方程式)。
(2)上述合成工艺中采用循环喷射吸收合成,其目的是_________;最后尾气主要成分是______。
(3)甲酸钠高温时分解制取草酸钠(Na2C2O4)的化学方程式为________。
(4)在甲酸钠、氢氧化钠混合溶液中通入二氧化硫气体,可得到重要的工业产品保险粉(Na2S2O4),同时产生二氧化碳气体,该反应的离子方程式为____________。
(5)某厂测知合成塔中甲酸钠生产产率为40%,要制得溶质质量分数为5%的HCOONa溶液1吨,需要CO在标况下的体积为___________。
查看答案和解析>>
科目: 来源:2015-2016学年河北省邯郸市高一上第一次月考化学试卷(解析版) 题型:选择题
下列说法正确的是
A.物质的量是一个基本物理量,表示物质所含粒子的多少
B.1 mol氢中含有2 mol氢原子和2 mol电子
C.1 mol H2O的质量等于NA个H2O分子质量的总和(NA表示阿伏加德罗常数的值)
D.摩尔表示物质的量的数量单位
查看答案和解析>>
科目: 来源:2015-2016学年河北省邯郸市高一上第一次月考化学试卷(解析版) 题型:选择题
下列说法正确的是
A.在标准状况下,1 mol酒精的体积是22.4 L
B.1 mol氢气所占的体积一定是22.4 L
C.标准状况下,6.02×1023个水分子所占有的体积约是22.4 L
D.标准状况下,28 g N2与CO的混合气体,体积为22.4 L
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com