
科目: 来源:2015-2016学年河北正定中学高二上学期第一次联考化学试卷(解析版) 题型:选择题
常温下0.1 mol·L-1氨水的pH=a,下列能使溶液pH=(a+1)的措施是
A.加入适量的氢氧化钠固体 B.将溶液稀释到原体积的10倍
C.加入等体积0.2 mol·L-1氨水 D.降低溶液的温度
查看答案和解析>>
科目: 来源:2015-2016学年河北正定中学高二上学期第一次联考化学试卷(解析版) 题型:选择题
常温下,体积相同、pH也相同的HCl、HNO3、CH3COOH溶液分别与足量的NaHCO3溶液反应,产生CO2的体积
A.同样多 B.HCl最多
C.HCl、HNO3一样多 D.CH3COOH最少
查看答案和解析>>
科目: 来源:2015-2016学年河北正定中学高二上学期第一次联考化学试卷(解析版) 题型:选择题
浓度均为0.10mol/L、体积均为V0的MOH和ROH溶液,分别加水稀释至体积V,pH随 的变化如图所示,下列叙述错误的是
的变化如图所示,下列叙述错误的是

A.MOH的碱性强于ROH的碱性
B.ROH的电离程度:b点大于a点
C.若两溶液无限稀释,则它们的c(OH-)相等
D.当 =2时,若两溶液同时升高温度,则
=2时,若两溶液同时升高温度,则  增大
增大
查看答案和解析>>
科目: 来源:2015-2016学年河北正定中学高二上学期第一次联考化学试卷(解析版) 题型:选择题
用已知浓度的NaOH滴定未知浓度的HCl溶液时,正确的操作顺序是
①用水洗净滴定管
②将滴定管进行检漏
③用待装液润洗滴定管后装液
④调整起始读数并记录
⑤向锥形瓶中加入指示剂
⑥用标准液进行滴定
⑦从酸式滴定管中取一定体积的待测液
⑧记录滴定终点读数并重复实验2~3次
A.①②③④⑤⑥⑦⑧ B.①②③④⑦⑤⑥⑧
C.②①③④⑦⑤⑥⑧ D.②①③④⑤⑥⑦⑧
查看答案和解析>>
科目: 来源:2015-2016学年河北正定中学高二上学期第一次联考化学试卷(解析版) 题型:选择题
水的电离平衡为H2O H+﹢OH-,△H>0,下列叙述不正确的是
H+﹢OH-,△H>0,下列叙述不正确的是
A.将水加热,pH减小
B.恒温下,向水中加入少量固体KOH,Kw不变
C.向水中滴入稀醋酸,c(H+)增大
D.向水中加入少量固体NaClO,平衡逆向移动
查看答案和解析>>
科目: 来源:2015-2016学年河北正定中学高二上学期第一次联考化学试卷(解析版) 题型:选择题
100℃时。下列三种溶液:①0.001 mol·L-1氨水与0.001 mol·L-1HCl溶液等体积混合液②pH=3的HCl与pH=11的NaOH溶液等体积混合液 ③pH=11的氨水与pH=1的HCl溶液等体积混合液。其中呈酸性的是
A.① B.③ C.②③ D.①③
查看答案和解析>>
科目: 来源:2015-2016学年河北正定中学高二上学期第一次联考化学试卷(解析版) 题型:选择题
相同温度下,在体积相等的三个恒容密闭容器中发生可逆反应:
N2(g)+ 3H2(g) 2NH3(g) △H=-92.4 kJ/mol
2NH3(g) △H=-92.4 kJ/mol
实验测得起始、平衡时的有关数据如下表:
容器编号 | 起始时各物质物质的量/mol | 平衡时反应中的能量变化 | ||
N2 | H2 | NH3 | ||
① | 1 | 3 | 0 | 放出热量a kJ |
② | 2 | 3 | 0 | 放出热量b kJ |
③ | 2 | 6 | 0 | 放出热量c kJ |
下列叙述正确的是
A.放出热量关系:a < b < 92.4
B.三个容器内反应的平衡常数:③ > ① > ②
C.达平衡时氨气的体积分数:① > ③
D.N2的转化率:② > ① > ③
查看答案和解析>>
科目: 来源:2015-2016学年河北正定中学高二上学期第一次联考化学试卷(解析版) 题型:选择题
一定条件下,体积为10 L的密闭容器中,1 mol X和1 mol Y进行反应:
2X(g)+Y(g)? ?Z(g),经60 s达到平衡,生成0.3 mol Z。下列说法正确的是
?Z(g),经60 s达到平衡,生成0.3 mol Z。下列说法正确的是
A.以X浓度变化表示的反应速率为0.001 mol/(L·s)
B.将容器体积变为20 L,Z的平衡浓度变为原来的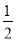
C.若增大压强,则物质Y的转化率减小
D.若升高温度,X的体积分数增大,则该反应的ΔH>0
查看答案和解析>>
科目: 来源:2015-2016学年河北正定中学高二上学期第一次联考化学试卷(解析版) 题型:选择题
分析下图所示装置,下列叙述不正确的是
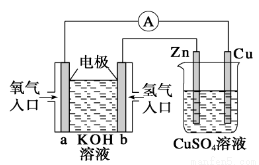
A.左边装置是燃料电池,右边装置是电镀池
B.电子流动方向:b→Zn→CuSO4(aq)→Cu→a
C.一段时间后,左端溶液浓度变小,右端溶液浓度不变
D.当锌片的质量变化12.8g时,a极消耗标准状况下的O2 2.24 L
查看答案和解析>>
科目: 来源:2015-2016学年河北正定中学高二上学期第一次联考化学试卷(解析版) 题型:实验题
(12分)乙二酸俗名草酸,下面是化学学习小组的同学对草酸晶体(H2C2O4·xH2O)
进行的探究性学习的过程,请你参与并协助他们完成相关学习任务。
该组同学的研究课题是:探究测定草酸晶体(H2C2O4·xH2O)中的x值。通过查阅资料和网络查寻得,草酸易溶于水,水溶液可以用酸性KMnO4溶液进行滴定。学习小组的同学设计了滴定的方法测定x值。
①称取2.520 g纯草酸晶体,将其制成100.00 mL水溶液为待测液。
②取25.00 mL待测液放入锥形瓶中,再加入适量的稀H2SO4。
③用浓度为0.100 0 mol·L-1的KMnO4标准溶液进行滴定,达到终点时消耗20.00 mL。
(1)写出草酸(H2C2O4)与酸性高锰酸钾溶液反应的离子方程式_______。
(2)滴定时,将酸性KMnO4标准液装在如图中的________(填“甲”或“乙”)滴定管中。

(3)本实验滴定达到终点的标志是___________。
(4)通过上述数据,求得x=________。
①若滴定终点时仰视滴定管刻度,则由此测得的x值会_____(填“偏大”、“偏小”或“不变”,下同)。
②若滴定时所用的酸性KMnO4溶液因久置而导致浓度变小,则由此测得的x值会________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com