
科目: 来源:2015-2016学年北京大学附属中学分校高二上抽考化学试卷(解析版) 题型:选择题
已知2H2(g)+O2(g)=2H2O(l);ΔH=-571.6kJ/mol,CO(g)+O2(g)=CO2(g);ΔH=-282.9kJ/mol某H2和CO的混合气体完全燃烧时放出113.74kJ热量,同时生成3.6g液态水,则原混合气体中H2和CO的物质的量之比为
A.1∶1 B.1∶2 C.2∶1 D.2∶3
查看答案和解析>>
科目: 来源:2015-2016学年北京大学附属中学分校高二上抽考化学试卷(解析版) 题型:填空题
写出298K常温时,下列反应的热化学方程式:
在稀溶液中1molH2SO4与足量NaOH反应放热114.6kJ,表示该中和热的热化学方程式为:
查看答案和解析>>
科目: 来源:2015-2016学年内蒙古包头九中高一上10月月考化学试卷(解析版) 题型:选择题
取m g相对原子质量为M的某金属与足量稀硫酸反应,在标准状况下产生a L氢气,该反应生成的硫酸盐中金属的化合价为
A.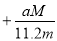 B.
B.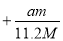 C.
C.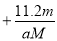 D.
D.
查看答案和解析>>
科目: 来源:2015-2016学年海南华侨中学高二上会考模拟化学试卷(解析版) 题型:选择题
下列各组性质比较中,正确的是
①失电子能力: K>Na>Li ②碱性: NaOH >Mg(OH)2>Al(OH)3
③氧化性:F>Si>O ④稳定性:PH3 <H2S<HCl
A.①②③ B.②③④ C.①②④ D.①③④
查看答案和解析>>
科目: 来源:2016届湖北省高三9月调考化学试卷(解析版) 题型:选择题
已知酸性高锰酸钾溶液可以将FeSO4 氧化,反应的化学方程式为 2KMnO4+10FeSO4+8H2SO4===K2SO4+X+5Fe2(SO4)3+8H2O,现将一定量的硫酸酸化的高锰酸钾溶液与硫酸亚铁溶液混合,充分反应后再向所得溶液中加入KI溶液,混合溶液中铁离子的物质的量随加入的KI的物质的量的变化关系如图所示,则下列有关说法不正确的是

A.方程式中的X为2MnSO4
B.氧化性:KMnO4>Fe3+>I2
C.根据OC段的数据可知开始加入的高锰酸钾的物质的量为0.30 mol
D.AB段是高锰酸钾和碘化钾溶液反应,BC段的反应为2Fe3++2I-===2Fe2++I2
查看答案和解析>>
科目: 来源:2016届湖北省高三9月调考化学试卷(解析版) 题型:填空题
(10分)粉煤灰中含有SiO2、Al2O3、Fe2O3等,某实验室对其进行处理的流程如下图所示:

回答下列问题:
(1)第①步得到的“熟料”中可溶性的成分主要是NH4Fe(SO4)2、NH4Al(SO4)2等,写出生成NH4Fe(SO4)2的化学方程式_____________。
(2)滤渣B的主要成分与NaOH溶液反应的离子方程式为________。
(3)步骤③中用NH4HCO3调节pH的实验原理为__________(用离子方程式表示)。
(4)实验室进行第④步操作时,所需的仪器是酒精灯、石棉网、三脚架、玻璃棒、_________,得到的晶体主要成份是_________(填化学式)。第⑥步生成Al(OH)3的离子方程式为_________。
查看答案和解析>>
科目: 来源:2016届湖北省高三9月调考化学试卷(解析版) 题型:填空题
(9分)磷是地壳中含量较为丰富的非金属元素,主要以难溶于水的磷酸盐如Ca3(PO4)2等形式存在。它的单质和化合物在工农业生产中有着重要的应用。
(1)白磷(P4)可由Ca3(PO4)2、焦炭和SiO2在电炉中高温(~1550℃)下通过下面三个反应共熔得到。
①4Ca3(PO4)2(s)+10C(s)=12CaO(s)+2P4(s)+10CO2(g)ΔH1=+Q1kJ·mol-1
②CaO(s)+SiO2(s)=CaSiO3(s) ΔH2=-Q2 kJ·mol-1
③CO2 (g)+C(s)=2CO(g) ΔH3=+Q3kJ·mol-1
已知:CaSiO3的熔点(1546℃)比SiO2低。
写出由磷酸钙矿制取白磷总的反应方程式____________。
(2)白磷在热的浓氢氧化钾溶液中歧化得到一种次磷酸盐(KH2PO2)和一种气体 (写化学式)。
(3)磷的重要化合物NaH2PO4可通过H3PO4与NaOH溶液反应获得。工业上为了使反应的主要产物是NaH2PO4,通常将pH控制在 之间(已知磷酸的各级电离常数为:K1 = 7.1×10?3 K2 = 6.3×10?8 K3 =4.2×10?13 lg7.1≈0.9 lg6.3≈0.8 lg4.2≈0.6) 。Na2HPO4 溶液显碱性,若向其溶液中加入足量的CaCl2 溶液,溶液则显酸性,其原因是 (用离子方程式表示)。
(4)白磷中毒后可用CuSO4溶液解毒,解毒原理可用下列化学方程式表示:
11P 4+60CuSO4+96H2O= 20Cu3P+24H3PO4+60H2SO4
60molCuSO4能氧化白磷的物质的量是 。
查看答案和解析>>
科目: 来源:2016届湖北省高三9月调考化学试卷(解析版) 题型:填空题
【化学——选修5:有机化学基础】(15分)某抗结肠炎药物有效成分的合成路线如下(部分反应略去试剂和条件):

根据以上信息回答下列问题:
(1)烃A的结构简式是 。
(2)①的反应条件是 。②的反应类型是 。
(3)下列对抗结肠炎药物有效成分可能具有的性质推测正确的是: 。
A.水溶性比苯酚好,密度比苯酚的大 B.能发生消去反应
C.能发生聚合反应 D.既有酸性又有碱性
(4)E与足量NaOH溶液反应的化学方程式是 。
(5)写出符合下列条件的E的同分异构体的结构简式(任写三种): 。
a.与E具有相同的官能团
b.苯环上的一硝基取代产物有两种
(6)已知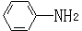 易被氧化,苯环上连有烷基时再引入一个取代基,常取代在烷基的邻对位,而当苯环上连有羧基时则取代在间位。据此写出以A为原料合成化合物
易被氧化,苯环上连有烷基时再引入一个取代基,常取代在烷基的邻对位,而当苯环上连有羧基时则取代在间位。据此写出以A为原料合成化合物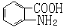 的合成路线 (仿照题中抗结肠炎药物有效成分的合成路线的表达方式答题)。
的合成路线 (仿照题中抗结肠炎药物有效成分的合成路线的表达方式答题)。
查看答案和解析>>
科目: 来源:2016届江西省高三上学期第一次月考化学试卷(解析版) 题型:选择题
用氢氧化钠固体配制0.10 mol/L的氢氧化钠溶液,下列说法中错误的是
A.定容时俯视容量瓶刻度线,会造成所配溶液浓度偏大
B.移液时不慎有部分液体溅出,会造成所配溶液浓度偏小
C.称量时托盘上要垫上干净的称量纸
D.定容摇匀后发现液面下降,不应再加蒸馏水
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com