
科目: 来源:2016届黑龙江省双鸭山市高三上第一次月考化学试卷(解析版) 题型:选择题
下列有关Fe2(SO4)3溶液的叙述正确的是
A.该溶液中K+、Fe2+、SCN-、Br-可以大量存在
B.和KI溶液反应的离子方程式: Fe3++2I-=Fe2++I2
C.和Ba(OH)2溶液反应离子方程式:Fe3++ SO42-+Ba2++3OH-=Fe(OH)3↓+BaSO4↓
D.1 L0.1 mol·L-1该溶液和足量的Zn充分反应,生成11.2g Fe
查看答案和解析>>
科目: 来源:2016届黑龙江省双鸭山市高三上第一次月考化学试卷(解析版) 题型:填空题
(14分)硫酸是用途广泛的化工原料,可作脱水剂、吸水剂、氧化剂和催化剂等。
(1)工业制硫酸铜的方法很多。
①方法一、用浓硫酸和铜制取硫酸铜。该反应的化学方程式是_____ _,此法的最大缺点是_ ______。
②方法二、用稀硫酸、铜和氧化铁制取硫酸铜,生产的主要过程如下图所示:

稀硫酸、铜和氧化铁反应的离子方程式是__ __;向混合溶液中通入热空气的反应的离子方程式是_ ____;由滤液得到无水硫酸铜的实验操作是 ______。
(2)氨法脱硫技术可吸收硫酸工业尾气中的二氧化硫,同时制得硫酸铵。主要的工艺流程如下图所示:

①吸收塔中发生反应的化学方程式是____ ___。
②有数据表明,吸收塔中溶液的pH在5.5~6.0之间,生产效率较高。当控制一定流量的尾气时,调节溶液的pH的简便方法是___ ____。
查看答案和解析>>
科目: 来源:2016届黑龙江省双鸭山市高三上第一次月考化学试卷(解析版) 题型:填空题
(14分)X、Y、Z、W四种物质有如下相互转化关系(其中X、W单质,Y、Z为化合物,未列出反应条件)。
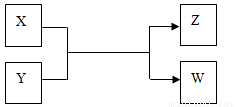
Ⅰ.若Z是生活中常用的调味品,W遇淀粉溶液变蓝,则:
(1)向FeCl2溶液中加入X的水溶液,是溶液颜色变为棕黄色的微粒是 。
(2)工业上Z有多种用途,用化学方程式表示Z的一种用途 。
(3)生活中所用的Z加入了碘酸钾,过量X与Y溶液反应时可以得到一种碘酸盐,此反应的离子方程式是 。
Ⅱ.若X是工业上用量最大的金属单质,Z是一种具有磁性的黑色晶体,则:
(1)X与Y反应的化学方程式是 。
(2)若用下列装置只进行Z + W X + Y反应(夹持装置未画出):
X + Y反应(夹持装置未画出):
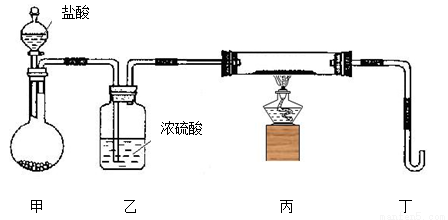
①完成此实验有多步操作,其中三步是:a.点燃酒精灯,b.滴加盐酸,c.检验气体纯度
这三步操作的先后顺序是 (填字母)。
②为保证实验成功,上述装置需要改进,方法是(用文字叙述) 。
(3)将3.48 g Z加入50 mL 4 mol/L的稀HNO3中充分反应,产生112 mL的NO(标准状况),向反应后的溶液中滴加NaOH溶液能产生沉淀。当沉淀量最多时,至少需要加入2 mol/L的NaOH溶液 mL (精确到0.1)。
查看答案和解析>>
科目: 来源:2016届湖南省衡阳市高三上学期第一次月考化学试卷(解析版) 题型:选择题
能正确表示下列反应的离子方程式是
A.Fe3O4溶于足量稀HNO3:Fe3O4+8H+=Fe2++2Fe3++4H2O
B.NH4HCO3溶液与足量Ba(OH)2溶液混合:HCO3-+Ba2++OH-=BaCO3↓+H2O
C.向澄清石灰水中通入少量CO2:OH-+CO2=HCO3-
D.将0.2 mol·L-1的NH4Al(SO4)2溶液与0.3 mol·L-1的Ba(OH)2溶液等体积混合:
2Al3++3SO42-+3Ba2++6OH-=2Al(OH)3↓+3BaSO4↓
查看答案和解析>>
科目: 来源:2016届湖南省衡阳市高三上学期第一次月考化学试卷(解析版) 题型:选择题
已知氧化还原反应:2Cu(IO3)2+24KI+12H2SO4===2CuI↓+13I2+12K2SO4+12H2O
其中1 mol氧化剂在反应中得到的电子为
A.10 mol B.11 mol C.12 mol D.13 mol
查看答案和解析>>
科目: 来源:2016届湖南省衡阳市高三上学期第一次月考化学试卷(解析版) 题型:填空题
饮水安全在人们生活中占有极为重要的地位,某研究小组提取三处被污染的水源进行了分析,给出了如下实验信息:其中一处被污染的水源含有A、B两种物质,一处含有C、D两种物质,一处含有E物质。A、B、C、D、E五种常见化合物都是由下表中的离子形成:
阳离子 | K+ Na+ Cu2+ Al3+ |
阴离子 | SO42- HCO3- NO3- OH- |
为了鉴别上述化合物,分别进行以下实验,其结果如下所示:
①将它们溶于水后,D为蓝色溶液,其他均为无色溶液;②将E溶液滴入到C溶液中出现白色沉淀,继续滴加,沉淀溶解;③进行焰色反应,只有B、C为紫色(透过蓝色钴玻璃片);④在各溶液中加入硝酸钡溶液,再加过量稀硝酸,A中放出无色气体,C、D中产生白色沉淀;⑤将B、D两溶液混合,未见沉淀或气体生成。
根据上述实验填空:
(1)写出B、D的化学式:B: ;D: 。
(2)将含1 mol A的溶液与含1 mol E的溶液反应后蒸干,仅得到一种化合物,该化合物为__________。
(3)写出实验②发生反应的离子方程式: 、 。
(4)C常用作净水剂,用离子方程式表示其净水原理: 。
查看答案和解析>>
科目: 来源:2015-2016学年山西太原五中高二上第一周考理科化学试卷(解析版) 题型:选择题
下列反应一定属于吸热反应的是
A.酸碱中和反应 B.实验室用氯酸钾和二氧化锰制氧气
C.物质燃烧反应 D.实验室制H2的反应
查看答案和解析>>
科目: 来源:2015-2016学年山西太原五中高二上第一周考理科化学试卷(解析版) 题型:选择题
白磷与氧可发生如下反应:P4 + 5O2 === P4O10。已知断裂下列化学键需要吸收的能量分别为:P-P a kJ·mol-1、P-O b kJ·mol-1、P=O c kJ·mol-1、O=O d kJ·mol-1。根据图示的分子结构和有关数据估算该反应的△H,其中正确的是

A.(6a + 5d-4c-12b)kJ·mol-1
B.(4c + 12b-6a-5d)kJ·mol-1
C.(4c + 12b-4a-5d)kJ·mol-1
D.(4a + 5d-4c-12b)kJ·mol-1
查看答案和解析>>
科目: 来源:2015-2016学年山西太原五中高二上第一周考理科化学试卷(解析版) 题型:选择题
在100g碳不完全燃烧所得气体中,CO占1/3体积,CO2占2/3体积,且:
C(s)+1/2O2(g)═CO(g)△H=-110.35kJ;
CO(g)+1/2O2(g)═CO2(g)△H=-282.5kJ 与这些碳完全燃烧相比,损失的热量是
A、392.92 KJ B、2489.4 kJ
C、784.72 kJ D、3274.3 kJ
查看答案和解析>>
科目: 来源:2015-2016学年山西太原五中高二上第一周考理科化学试卷(解析版) 题型:填空题
红磷P(s)和Cl2(g)发生反应生成PCl3(g)和PCl5(g)。反应过程和能量关系如下图所示(图中的ΔH表示生成1 mol产物的数据)。

根据上图回答下列问题:
(1)P和Cl2反应生成PCl3的热化学方程式是_____________;
(2)PCl5分解成PCl3和Cl2的热化学方程式是_______________。
上述分解反应是一个可逆反应,温度T1时,在密闭容器中加入0.80 mol PCl5,反应达平衡时PCl5还剩0.60 mol,其分解率α1等于 ;
(3)P和Cl2分两步反应生成1 mol PCl5的反应热ΔH3= ,P和Cl2一步反应生成1 mol PCl5的ΔH4 ΔH3(填“大于”、“小于”或“等于”);
(4)PCl5与足量水充分反应,最终生成两种酸,其化学方程式是____________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com