
科目: 来源:2015-2016学年山西阳泉十五中高三第一次阶段考试化学试卷(解析版) 题型:选择题
广口瓶被称为气体实验的“万能瓶”,是因为它可以配合玻璃管和其他简单仪器组成各种功能的装置。下列各图中能用作防倒吸安全瓶的是

查看答案和解析>>
科目: 来源:2015-2016学年山西阳泉十五中高三第一次阶段考试化学试卷(解析版) 题型:选择题
碳化硅的结构类似于金刚石的晶体,其中碳原子和硅原子的位置是交替的。在下列三种晶体①金刚石 ②晶体硅 ③碳化硅中,它们的熔点从高到低的顺序是
A.①③② B.②③① C.③①② D.②①③
查看答案和解析>>
科目: 来源:2015-2016学年山西阳泉十五中高三第一次阶段考试化学试卷(解析版) 题型:选择题
氢化钙(CaH2)可作为生氢剂,反应的化学方程式为CaH2+2H2O===Ca(OH)2+2H2↑,下列说法不正确的是
A.CaH2既是还原剂,又是氧化剂 B.H2既是氧化产物,又是还原产物
C.CaH2是还原剂,H2O是氧化剂 D.氧化产物与还原产物质量比为1∶1
查看答案和解析>>
科目: 来源:2015-2016学年山西阳泉十五中高三第一次阶段考试化学试卷(解析版) 题型:选择题
下列说法中正确的是
A.1 L水中溶解了58.5 g NaCl,该溶液的物质的量浓度为1 mol/L
B.从1 L 2 mol/L的H2SO4溶液中取出0.5 L,该溶液的浓度为1 mol/L
C.配制500 mL 0.5 mol/L的CuSO4溶液,需62.5 g胆矾
D.中和100 mL 1 mol/L的H2SO4溶液,需NaOH 4 g
查看答案和解析>>
科目: 来源:2015-2016学年山西阳泉十五中高三第一次阶段考试化学试卷(解析版) 题型:选择题
一定量的镁溶于一定浓度的硝酸的反应中,产生标准状况下的N2O气体11.2L,在所得的溶液中加入足量的氢氧化钠溶液,完全反应后过滤出沉淀,经洗涤、蒸干并充分灼烧,最后得到固体的质量为
A.20g B.40g C.58g D.80g
查看答案和解析>>
科目: 来源:2015-2016学年山西阳泉十五中高三第一次阶段考试化学试卷(解析版) 题型:选择题
在一种酸性溶液中可能存在Fe3+、NO3-、Cl-、I-中的一种或几种离子,向溶液中加入溴水,溴单质被还原,由此可推断溶液中
A.一定含有I-,不能含有Cl-
B.可能含有Cl-、NO3-和I-
C.可能含有NO3-
D.不含有Fe3+
查看答案和解析>>
科目: 来源:2015-2016学年山西阳泉十五中高三第一次阶段考试化学试卷(解析版) 题型:选择题
关于某无色溶液中所含离子的鉴别,下列判断正确的是
A.加入AgNO3溶液,生成白色沉淀,加稀盐酸沉淀不消失,可确定有Cl-存在
B.通入Cl2后,溶液变为黄色,加入淀粉溶液后溶液变蓝,可确定有I-存在
C.加入Ba(NO3)2,生成白色沉淀,加稀盐酸沉淀不消失,可确定有SO42-存在
D.加入盐酸,生成的气体能使澄清石灰水变浑浊,可确定有CO32-存在
查看答案和解析>>
科目: 来源:2015-2016学年山西阳泉十五中高三第一次阶段考试化学试卷(解析版) 题型:选择题
下列各组中的两种物质相互反应时,无论哪种过量,都可以用同一个离子方程式表示的是
①碳酸钠溶液与盐酸 ②偏铝酸钠溶液与盐酸 ③苯酚钠溶液和CO2
④硝酸银溶液和氨水 ⑤氯化铝溶液和氨水 ⑥碳酸氢钠溶液与澄清石灰水
A.③⑤ B.①③⑥ C.仅有⑤ D.②④
查看答案和解析>>
科目: 来源:2015-2016学年山西阳泉十五中高三第一次阶段考试化学试卷(解析版) 题型:实验题
(13分)铁的发现和大规模使用,是人类发展史上的一个光辉里程碑,它把人类从石器时代、青铜器时代带到了铁器时代,推动了人类文明的发展。
(1)高铁酸钠(Na2FeO4)是水处理过程中的一种新型净水剂,它的氧化性比高锰酸钾更强,本身在反应中被还原成三价铁离子达到净水的目的。按要求回答下列问题:
高铁酸钠主要通过如下反应制取:2Fe(OH)3 + 3NaClO + 4NaOH == 2Na2FeO4 + 3X + 5H2O, 则X的化学式 ,反应中被氧化的物质是 (写化学式)。
(2)铁红颜料跟某些油料混合,可以制成防锈油漆。以黄铁矿为原料制硫酸产生的硫酸渣中含Fe2O3、SiO2、Al2O3、MgO等,用硫酸渣制备铁红(Fe2O3)的过程如下:

①酸溶过程中Fe2O3与稀硫酸反应的化学方程式为 ____ ;“滤渣A”主要成份的化学式为 。
②还原过程中加入FeS2的目的是将溶液中的Fe3+还原为Fe2+,而本身被氧化为H2SO4,请完成该反应的离子方程式:
FeS2 + Fe3 + + H2O == Fe2 + + SO42- + ___ 。
③氧化过程中,O2、NaOH与Fe2+反应的离子方程式为 _______。
④为了确保铁红的质量和纯度,氧化过程需要调节溶液的pH的范围是3.2~3.8,
沉淀物 | Fe(OH)3 | Al(OH)3 | Fe(OH)2 | Mg(OH)2 |
开始沉淀pH | 2.7 | 3.8 | 7.6 | 9.4 |
完全沉淀pH | 3.2 | 5.2 | 9.7 | 12.4 |
如果pH过大,可能引起的后果是 __ (几种离子沉淀的pH见上表);滤液B可以回收的物质有(写化学式) 。
查看答案和解析>>
科目: 来源:2015-2016学年山西阳泉十五中高三第一次阶段考试化学试卷(解析版) 题型:填空题
(15分)已知A、B、C、D、E、F、G都是周期表中前四周期的元素,它们的核电荷数依次增大,其中A、B、C、D、E为不同主族的元素。A、C的最外层电子数都是其电子层数的2倍,B的电负性大于C,透过蓝色钴玻璃观察E的焰色反应为紫色,F的基态原子中有4个未成对电子,G的+1价阳离子正好充满K,L,M三个电子层。回答下列问题:
(1)A、B、C、D、E、F、G几种元素中第一电离能最小的是____(填元素符号),D元素的原子核外有 种不同运动状态的电子;有 种不同能级的电子。基态的F3+核外电子排布式是 。
(2)B的气态氢化物在水中的溶解度远大于A、C的气态氢化物,原因是 。
(3)化合物ECAB中的阴离子与AC2互为等电子体,该阴离子的电子式是 。
(4)FD3与ECAB溶液混合,得到含多种配合物的血红色溶液,其中配位数为5的配合物的化学式是 。
(5)化合物EF[F(AB)6]是一种蓝色晶体,下图表示其晶胞的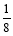
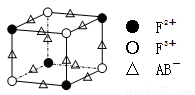
(E+未画出)。该蓝色晶体的一个晶胞中E+的个数为 。
(6)G的二价阳离子能与乙二胺(H2N—CH2一CH2一NH2)形成配离子:该配离子中含有的化学键类型有 。(填字母)
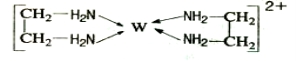
a.配位键 b.极性键 c.离子键 d.非极性键
阴离子CAB-中的A原子与乙二胺(H2N—CH2一CH2一NH2)中C原子的杂化方式为 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com