
科目: 来源:2016届甘肃省平凉市高三上学期第一次模拟考试化学试卷(解析版) 题型:选择题
下列关于工业生产的说法中正确的是
A.氯碱工业中阳离子交换膜的主要作用是防止氯气和氢气以及氢氧化钠反应
B.硫酸工业中合成SO3通常采用常压,是因为常压比高压更有利于SO3的生成
C.电解精炼铜时,纯铜作为阳极,粗铜作为阴极
D.工业合成氨通常采用500℃的高温主要是为了提高氮气的转化率
查看答案和解析>>
科目: 来源:2016届甘肃省平凉市高三上学期第一次模拟考试化学试卷(解析版) 题型:选择题
下列保存物质的方法正确的是
A.把汽油放在带橡皮塞的玻璃瓶中 B.把氢氟酸放在玻璃瓶中
C.把少量白磷贮存在冷水中 D.把水玻璃贮存在带玻璃塞的玻璃瓶中
查看答案和解析>>
科目: 来源:2016届甘肃省平凉市高三上学期第一次模拟考试化学试卷(解析版) 题型:选择题
阿伏加德罗常数为6.02×1023 mol-1,下列叙述正确的是
A.4 g重水(D2O)中所含中子数为0.2×6.02×1023
B.32 g含有少量臭氧的氧气中,共含有氧原子1.204×1024
C.4.48 L H2和O2的混合气体中所含分子数为0.2×6.02×1023
D.0.1 mol Na2O2溶解于足量的水中,转移电子数为0.2×6.02×1023
查看答案和解析>>
科目: 来源:2016届甘肃省平凉市高三上学期第一次模拟考试化学试卷(解析版) 题型:选择题
在标准状况下,m g气体A与n g气体B的分子数相同,下列说法中不正确的是
A.气体A与气体B的相对分子质量比为m∶n
B.同质量的气体A与B的分子个数比为n∶m
C.同温同压下,A气体与B气体的密度比为n∶m
D.同温同压下,同体积的A气体与B气体的质量比为m∶n
查看答案和解析>>
科目: 来源:2016届甘肃省平凉市高三上学期第一次模拟考试化学试卷(解析版) 题型:填空题
(8分)目前,我国采用“接触法”制硫酸,设备如图所示:
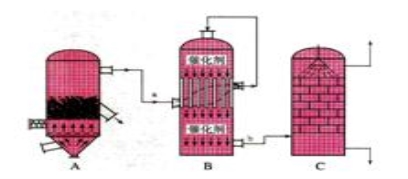
(1)图中设备A的名称是______________,该设备中主要反应的化学方程式为____________。
(2)有关接触法制硫酸的下列说法中,不正确的是______________________
A.二氧化硫的接触氧化在接触室中发生
B.吸收塔用浓度为98.3%浓硫酸吸收三氧化硫
C.B装置中反应的条件之一为较高温度是为了提高SO2的转化率
D.硫酸工业中在接触室安装热交换器是为了利用SO3转化为H2SO4时放出的热量
(3)用18 mol/L 的浓硫酸配制100 mL 3.6 mol/L 稀硫酸,所需浓硫酸的体积是_______。
查看答案和解析>>
科目: 来源:2016届江苏省高三上学期开学考试化学试卷(解析版) 题型:选择题
下列有关化学用语表示正确的是
A.中子数为20的氯原子: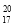 Cl
Cl
B.苯的结构简式:C6H6
C.H2CO3的电离方程式:H2CO3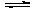 2H++CO32-
2H++CO32-
D.过氧化钙(CaO2)的电子式: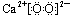
查看答案和解析>>
科目: 来源:2016届江苏省高三上学期开学考试化学试卷(解析版) 题型:选择题
质量分数为a的某物质的溶液mg与质量分数为b的该物质的溶液ng混合后,蒸发掉pg水。得到的溶液每毫升质量为qg,物质的量浓度为c,则溶质的相对分子质量为
A.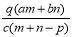 B.
B.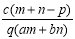 C.
C.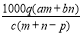 D.
D.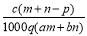
查看答案和解析>>
科目: 来源:2016届江苏省高三上学期开学考试化学试卷(解析版) 题型:选择题
下列说法正确的是
A.常温下,反应4Fe(OH)2(s)+2H2O(l)+O2(g)===4Fe(OH)3(s)的ΔH<0
B.常温下,BaSO4分别在相同物质的量浓度的Na2SO4溶液和Al2(SO4)3溶液中的溶解度相同
C.常温下,向饱和Na2CO3溶液中加少量BaSO4粉末,过滤,向洗净的沉淀中加稀盐酸,有气泡产生,说明常温下Ksp(BaCO3)<Ksp(BaSO4)
D.等体积、等物质的量浓度的NH3·H2O溶液与NH4Cl溶液混合后溶液呈碱性,说明NH3·H2O的电离程度小于NH的水解程度
查看答案和解析>>
科目: 来源:2016届江苏省高三上学期开学考试化学试卷(解析版) 题型:实验题
某种胃药片的制酸剂为碳酸钙,其中所含的制酸剂质量的测定如下:
①配制0.10 mol·L-1的 HCI和0.10mol·L-1的NaOH溶液
②取一粒(药片质量均相同)0.20g的此胃药片,磨碎后加入20.00mL蒸馏水
③以酚酞为指示剂,用0.1mol·L-1的NaOH溶液滴定至终点④加入50.00mL0.10 mol·L-1的HCl溶液
(1)写出实验过程中至少需要的步骤 (写编号顺序)。
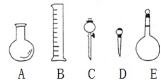
(2)下图所示的仪器中配制0.10 mol·L-1HCl溶液和0.10 mol·L-1的NaOH溶液肯定不需要的仪器是(填序号) ,配制上述溶液还需要的玻璃仪器是(填仪器名称) 。
(3)配制0.1mol·L-1的NaOH溶液时,下列操作会使得所配溶液浓度变大的是 。
a.称量NaOH固体时动作过慢
b.溶解氢氧化钠时有部分液体溅出
c.未洗涤烧杯和玻璃棒
d.未冷却至室温就转移到容量瓶中
e.定容时俯视标线
f.摇匀后发现液面低于标线加水至标线
(4)写出有关反应的离子方程式
(5)若滴定消耗NaOH溶液体积为14.00mL,则该胃药中含碳酸钙的质量分数是 。
查看答案和解析>>
科目: 来源:2016届江苏省高三上学期开学考试化学试卷(解析版) 题型:填空题
碱式氧化镍(NiOOH)可用作镍氢电池的正极材料。以含镍(Ni2+)废液为原料生产NiOOH的一种工艺流程如下:

(1)加入Na2CO3溶液时,确认Ni2+已经完全沉淀的实验方法是 。
(2)已知Ksp[Ni(OH)2]=2×10-15,欲使NiSO4溶液中残留c(Ni2+)≤2×10-5 mol·L-1,调节pH的范围是 。
(3)写出在空气中加热Ni(OH)2制取NiOOH的化学方程式: 。
(4)若加热不充分,制得的NiOOH中会混有Ni(OH)2,其组成可表示为xNiOOH·yNi(OH)2。现称取9.18 g样品溶于稀硫酸,加入100 mL 1.0 mol·L-1 Fe2+标准溶液,搅拌至溶液清亮,定容至200 mL。取出20.00 mL,用0.010 mol·L-1 KMnO4标准溶液滴定,用去KMnO4标准溶液20.00 mL,试通过计算确定x、y的值(写出计算过程)。涉及反应如下(均未配平):
NiOOH+Fe2++H+—Ni2++Fe3++H2O Fe2++MnO4-+H+—Fe3++Mn2++H2O
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com