
科目: 来源:2016届上海市十一校高三上学期12月联考化学试卷(解析版) 题型:选择题
黄铜矿(CuFeS2)是提取铜的主要原料,其煅烧产物Cu2S在1200℃高温下继续反应:2Cu2S + 3O2 →2Cu2O + 2SO2……① 2Cu2O + Cu2S →6Cu + SO2……②。则下列说法正确的是
A.反应②中Cu2S只发生了氧化反应
B.反应①中氧化产物只有SO2
C.若1molCu2S完全转化为2molCu,则转移电子数为2NA
D.将1molCu2S冶炼成2molCu,需要O2 1mol
查看答案和解析>>
科目: 来源:2016届上海市十一校高三上学期12月联考化学试卷(解析版) 题型:选择题
在含有0.6molCl-、0.8 molSO42-及一定量Mg2+和Al3+的混合溶液中,滴入一定浓度NaOH溶液,产生沉淀情况如图(不考虑Mg2+和Al3+水解及水电离对离子数目的影响)。若反应前Al3+的物质的量为a mol,Al3+的物质的量与混合溶液中离子总物质的量的比值为x。则下列正确的是
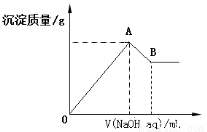
A.x=
B.x的取值范围是0<x<11/32
C.A点横坐标的值不随x发生变化
D.若B点横坐标为200mL时,c(NaOH)=7.0mol/L
查看答案和解析>>
科目: 来源:2016届上海市十一校高三上学期12月联考化学试卷(解析版) 题型:填空题
硫化钠是一种重要的化工原料。工业上用硫酸钠与碳反应得到硫化钠。反应方程式如下:
Na2SO4 + 2C Na2S + CO2↑
Na2S + CO2↑
完成下列填空:
(1)上述反应的元素中,原子半径最小的元素的原子有 种能级不同的电子。
(2)下列可以证明二氧化碳是非极性分子的事实是 (填编号)
a.二氧化碳密度比空气大
b.二氧化碳能溶于水
c.二氧化碳在电场中通过不偏向
d.二氧化碳常温常压下为气态
(3)硫化钠在一定条件下会与硫单质反应生成多硫化钠(Na2SX)。在碱性溶液中,Na2SX与NaBrO3反应生成Na2SO4与NaBr。若Na2SX与NaBrO3反应的物质的量之比为3:16,则 x = 。
(4)写出硫氢化钠与少量硫酸铜溶液反应的离子方程式 。能否用硫酸铜溶液来鉴别硫化钠溶液和硫氢化钠溶液?请简述实验操作和现象并说明自己的观点: 。
(5)已知:H2S Ki1 = 9.1×10-8 Ki2 = 1.1×10-12 HF Ki = 3.5×10-4
H2SO3 Ki1 = 1.5×10-2 Ki2 = 1.0×10-7 HAc Ki = 1.75×10-5
若用右图的装置,用硫化钠固体和下列溶液制取硫化氢气体,可选用的试剂是 。
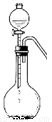
a.硝酸 b.亚硫酸氢钠 c.氢氟酸 d.醋酸
查看答案和解析>>
科目: 来源:2016届上海市十一校高三上学期12月联考化学试卷(解析版) 题型:填空题
利用氮气、氢气在一定条件下生成氨气这一可逆反应来合成氨,是一个重要的化工反应。常用来生产液氨和氨水。
完成下列填空:
(1)右图表示合成氨时生成1mol生成物时的能量变化,E的单位为kJ。请写出合成氨的热化学方程式 (热量用E1、E2或E3表示)。
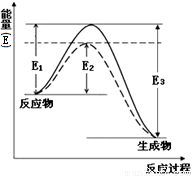
该图中的实线与虚线部分是什么反应条件发生了变化? 。
(2)在一定温度下,若将4amol H2和2amol N2放入VL的定容密闭容器中,2分钟后测得N2的转化率为50%,则该段时间用H2表示的反应速率为 摩尔/(升?秒)。若此时再向该容器中投入a mol H2、amol N2和2amol NH3,判断平衡移动的方向是 (填“正向移动”“逆向移动”或“不移动”)。
(3)液氨和水类似,也能电离:2NH3 NH4++ NH2-,某温度时,其离子积K=2×l0-30。该温度下:①将少量NH4Cl固体加入液氨中,K 2×10-30(填“<”、“>”或“=”);
NH4++ NH2-,某温度时,其离子积K=2×l0-30。该温度下:①将少量NH4Cl固体加入液氨中,K 2×10-30(填“<”、“>”或“=”);
②将少量金属钠投入液氨中,完全反应后所得溶液中各微粒物质的量大小排列为:
(4)工厂生产的氨水作肥料时需要稀释。用水稀释0.1mol/L稀氨水时,溶液中随着水量的增加而减少的是 。
a.c(NH4+)/c(NH3•H2O) b.c(NH3•H2O)/c(OH-)
c.c(OH-)/c(H+) d.c(H+)/c(NH4+)
查看答案和解析>>
科目: 来源:2016届上海市十一校高三上学期12月联考化学试卷(解析版) 题型:实验题
某化学小组拟采用如下装置(夹持和加热仪器已略去)来电解饱和食盐水,并用电解产生的H2还原CuO粉末来测定Cu元素的相对原子质量,同时检验氯气的氧化性。
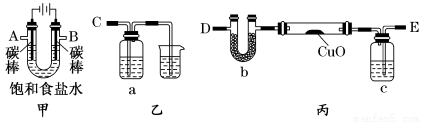
(1)为完成上述实验,正确的连接顺序为A连 ;B连 (填写连接的字母)。
(2)对硬质玻璃管里的氧化铜粉末加热前,需要的操作为 。
(3)若检验氯气的氧化性,则乙装置的a瓶中溶液可以是 ,对应的现象为 。
(4)丙装置的c瓶中盛放的试剂为 ,作用是 。
(5)为测定Cu的相对原子质量,设计了如下甲、乙两个实验方案,精确测量硬质玻璃管的质量为a g, 放入CuO后,精确测量硬质玻璃管和CuO的总质量为b g ,充分反应完全后。
甲方案:通过精确测定生成水的质量d g,进而确定Cu的相对原子质量。
乙方案:通过精确测量硬质玻璃管和Cu粉的总质量为c g, 进而确定Cu的相对原子质量。
①请你分析并回答: 方案测得结果更准确。你认为不合理的方案的不足之处在 。
②按测得结果更准确的方案进行计算,Cu的相对原子质量是 。
查看答案和解析>>
科目: 来源:2016届上海市十一校高三上学期12月联考化学试卷(解析版) 题型:实验题
实验室以苯、乙醛为原料,AlCl3为催化剂制备1,1–二苯乙烷,其反应原理为:

已知:AlCl3固体遇水会发生较强烈水解。
I.制取装置如右图所示。
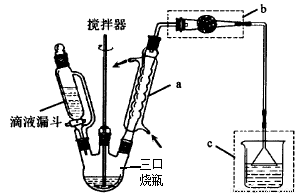
(1)该反应需控制反应温度为20℃。控制20℃的方法是 ;该反应不高于20℃的可能原因是: 。
(2)仪器a的作用是 ;装置c的作用是吸收HCl,写出产生HCl的化学方程式 ;装置b的作用是 。
Ⅱ.实验结束后,将三口烧瓶中的混合物倒入冷稀盐酸中,用分液漏斗分离出有机层,依次用水、2%碳酸钠溶液、水洗涤,洗涤后加入少量无水硫酸镁固体,过滤、蒸馏,得到1,1–二苯乙烷。
(1)分液漏斗中,产品在 (填“上”或“下”)层;洗涤操作中,第二次水洗的目的是 ;无水硫酸镁也可用物质 代替。
(2)蒸馏提纯时,下列装置中会导致收集到的产品中混有低沸点杂质的装置是 (选填编号)。
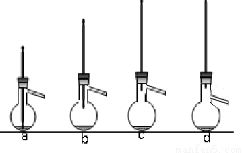
(3)三口烧瓶中加入120mL苯(密度0.88g/mL)、19g A1C13和3.7g乙醛,20℃时充分反应,制得纯净的1,1–二苯乙烷7.8g。该实验的产率约为 。
查看答案和解析>>
科目: 来源:2016届上海市十一校高三上学期12月联考化学试卷(解析版) 题型:推断题
已知: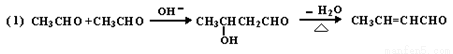 ,水杨酸酯E为紫外线吸收剂,可用于配制防晒霜。E的一种合成路线如下:
,水杨酸酯E为紫外线吸收剂,可用于配制防晒霜。E的一种合成路线如下:

请回答下列问题:
(1)饱和一元醇A中氧的质量分数约为21.6%,则A的分子式为 ;结构分析显示A只有一个甲基,A的系统命名法名称为 。
(2)B能与新制的Cu(OH)2悬浊液发生反应,该反应的化学方程式为 。
(3)C的可能结构有 种;若一次取样,检验C中所含官能团,按使用的先后顺序写出所用试剂: 。
(4)D所含官能团的名称为 ;第④步的反应类型为 ;
(5)同时符合下列条件的水杨酸所有同分异构体共有 种。
a.分子中有6个碳原子在一条直线上;
b.分子中所含官能团包括水杨酸具有的含氧官能团。
查看答案和解析>>
科目: 来源:2016届上海市十一校高三上学期12月联考化学试卷(解析版) 题型:推断题
优良的有机溶剂对孟烷、耐热型特种高分子功能材料PMnMA的合成路线如下:
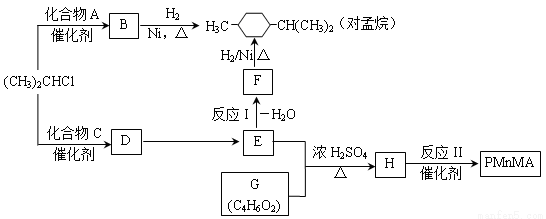
己知芳香化合物苯环上的氢原子可被卤代烷中的烷基取代。如:
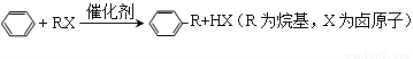
Ⅰ B为芳香烃。
(1)由B生成对孟烷的反应类型是 。
(2)(CH3)2CHCl与A生成B的化学方程式是 。
(3)A的同系物中相对分子质量最小的物质是 (填写名称)。
Ⅱ 1.08g的C与足量饱和溴水完全反应生成3.45 g白色沉淀。E不能使Br2的CC14溶液褪色。
(1)F的官能团是 。
(2)C的结构简式是 。
(3)反应I的条件是 。
(4)下列说法正确的是(选填字母) 。
a.B可使酸性高锰酸钾溶液褪色
b.C不存在醛类同分异构体
c.D的酸性比E弱
d.E的沸点高于对孟烷
(5)G有三种不同环境的H原子,且个数比为3:2:1。G能与NaHCO3溶液反应放出CO2。反应II的化学方程式是 。
查看答案和解析>>
科目: 来源:2016届上海市十一校高三上学期12月联考化学试卷(解析版) 题型:计算题
氢气是化工行业重要原料之一。
(1)电解饱和食盐水是生产H2的方法之一。常温下,电解250 mL饱和食盐水一段时间后,溶液质量减轻0.365 g(假设气体全部逸出)。生成的氢气在标准状况下的体积为 mL。
(2)在电弧炉中,甲烷裂解产生乙炔和氢气,若1 m3 甲烷经此过程生成0.27 m3氢气,则甲烷的裂解率为 %(体积均在相同条件下测定)。
(3)已知:CxHy + H2O → CO + CO2 + H2(未配平)。工业上用甲烷、乙烷的混合气体利用上述反应生产氢气,反应后气体经干燥组成如下表所示:
组分 | CO | CO2 | H2 |
体积分数 | 20% | 5% | 75% |
计算原混合气体中甲烷与乙烷的物质的量之比。
(4)合成氨生产过程中,消耗氮氢混合气2000 m3(其中CH4的体积分数为0.112%,下同),分离液氨后的氮氢混合气中含CH4 2.8%。计算分离出液氨为多少吨(保留2位小数,所有体积均已折算至标准状况)。
查看答案和解析>>
科目: 来源:2016届陕西省高三上学期期中化学试卷(解析版) 题型:选择题
我国清代《本草纲目拾遗》中记叙无机药物335种,其中“强水”条目下写道:“性最烈,能蚀五金……其水甚强,五金八石皆能穿第,惟玻璃可盛。”这里的“强水”是指
A.氨水 B.卤水 C.醋 D. 硝酸
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com