
科目: 来源:2015-2016学年浙江省桐乡市高二上期中(实验班)化学试卷(解析版) 题型:选择题
某一可逆反应的反应物和生成物都是气体,改变下列条件一定能使化学平衡向正反应方向移动的是
A.恒压下充入稀有气体 B.减小反应容器的体积
C.升高反应温度 D.分离出生成物
查看答案和解析>>
科目: 来源:2015-2016学年浙江省桐乡市高二上期中(实验班)化学试卷(解析版) 题型:选择题
常温下,下列四种溶液:①pH=2的CH3COOH溶液;②pH=2的HCl溶液;③pH=12的氨水;④pH=12的NaOH溶液。有关上述溶液的比较中,正确的是
A.将等体积的①、②溶液混合后,盐酸会抑制醋酸的电离,所以pH﹥2
B.将一定体积的②、③溶液混合后, 溶液显碱性,则该混合溶液中c(Cl-)﹥c(NH4+)
溶液显碱性,则该混合溶液中c(Cl-)﹥c(NH4+)
C.将一定体积的①、④溶液混合后,溶液显酸性,则V(NaOH)可能等于V(CH3COOH)
D.向等体积的③、④溶液中加水稀释10倍,稀释后溶液中由 水电离的c(H+):③﹥④
水电离的c(H+):③﹥④
查看答案和解析>>
科目: 来源:2015-2016学年浙江省桐乡市高二上期中(实验班)化学试卷(解析版) 题型:选择题
已知部分弱酸的电离平衡常数如下表:

下列离子方程式正确的是
A.少量CO2通入NaClO溶液中:CO2+H2O+2ClO-=CO +2HClO
+2HClO
B.少量的SO2通入Ca(ClO)2溶液中:SO2+H2O+Ca2++2ClO-=CaSO3↓+2HClO
C.少量的SO2通入Na2CO 3溶液中:SO2+H2O+2 CO
3溶液中:SO2+H2O+2 CO =SO
=SO +2HCO3-
+2HCO3-
D.相同浓度NaHCO3溶液与NaHSO3溶液等体积混合:H++HCO3-=CO2↑+H2O
查看答案和解析>>
科目: 来源:2015-2016学年浙江省桐乡市高二上期中(实验班)化学试卷(解析版) 题型:填空题
二甲醚是一种重要的化工原料,利用水煤气(CO、H2)合成二甲醚是工业上的常用方法,该方法由以下几步组成:
2H2(g)+CO(g)  CH3OH(g) ΔH= —90.0 kJ·mol-1 ①
CH3OH(g) ΔH= —90.0 kJ·mol-1 ①
2CH3OH(g)  CH3OCH3(g)+H2O(g) ΔH= —24.5 kJ·mol-1 ②
CH3OCH3(g)+H2O(g) ΔH= —24.5 kJ·mol-1 ②
CO(g)+H2O(g)  CO2(g)+H2(g) ΔH= —
CO2(g)+H2(g) ΔH= — 41.1 kJ·mol-1 ③
41.1 kJ·mol-1 ③
(1)反应①的ΔS 0(填“>”、“<”或“=”)。在 (填“较高”或“较低”)温度下该反应自发进行。
(2)在250℃的恒容密闭容器中,下列事实可以作为反应③已达平衡的是 (填选项字母)。
A.容器内气体密度保持不变 B.CO与CO2的物质的量之比保持不变
C.H2O与CO2的生成速率之比为1∶1 D.该反应的平衡常数保持不变
(3)当合成气中CO与H2的物质的量之比恒定时,温度、压强对CO转化率的影响如图1所示。图1中A点的v(逆) B点的v(正)(填“>”、“<”或“=”),说明理由 。实际工业生产中该合成反应的条件为500℃、4MPa请回答采用500℃的可能原因 。
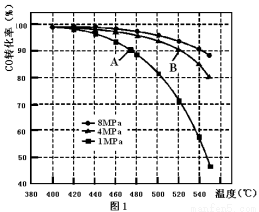
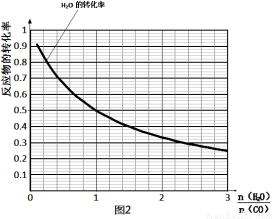
(4)一定温度下,密闭容器中发生反应③,水 蒸气的转化率与n(H2O)∕n(CO)的关系如图:计算该温度下反应③的平衡常数K= 。在图2中作出一氧化碳的转化率与n(H2O)∕n(CO)的曲线。
蒸气的转化率与n(H2O)∕n(CO)的关系如图:计算该温度下反应③的平衡常数K= 。在图2中作出一氧化碳的转化率与n(H2O)∕n(CO)的曲线。
查看答案和解析>>
科目: 来源:2015-2016学年浙江省桐乡市高二上期中(实验班)化学试卷(解析版) 题型:实验题
某化学活动小组按下图所示流程由粗氧化铜样品(含少量氧化亚铁及不溶于酸的杂质)制取无水硫酸铜。
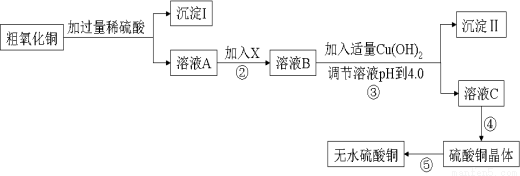
已知Fe3+、Cu2+、Fe2+三种离子在水溶液中形成氢氧化物沉淀的pH范围如下图所示:
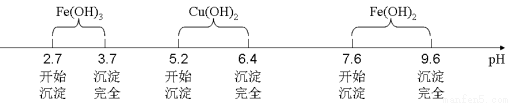
请回答下列问题:
(1)在整个实验过程中,下列实验装置不可能用到的是 (填序号)
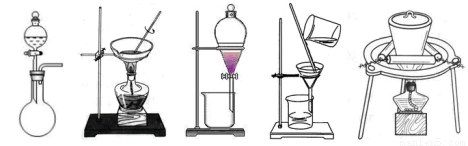
① ② ③ ④ ⑤
(2)溶液A中所含溶质为 ;
(3)物质X应选用 (填序号),沉淀II的主要成分是
①氯水 ②双氧水 ③铁粉 ④高锰酸钾
(4)从溶液C中制取硫酸铜晶体的实验操作为 。
(5)用“间接碘量法”可以测定溶液A中Cu2+(不含能与I-发生反应的杂质)的浓度。过程如下:
第一步:移取10.00mL溶液A于100mL容量瓶,加水定容至100mL。
第二步:取稀释后试液20.00mL于锥形瓶中,加入过量KI固体,充分反应生成白色沉淀与碘单质。
第三步:以淀粉溶液为指示剂,用0.05000mol·L-1的Na2S2O3标准溶液滴定,前后共测定三组。达到滴定终点时,消耗Na2S2O3标准溶液的体积如下表:
(已知:I2+2S2O32-===2I-+S4O62-)
滴定次数 | 第一次 | 第二次 | 第三次 |
滴定前读数(mL) | 0.10 | 0.36 | 1.10 |
滴定滴定后读数(mL) | 20.12 | 20.34 | 22.12 |
①CuSO4溶液与KI的反应的离子方程式为 。
②滴定中,试液Na2S2O3应放在  (填“酸式滴定管”或“碱式滴定管”),判断滴定终点的依据是 。
(填“酸式滴定管”或“碱式滴定管”),判断滴定终点的依据是 。
③溶液A中c(Cu2+)= mol·L-1
查看答案和解析>>
科目: 来源:2015-2016学年浙江省桐乡市高二上期中(普通班)化学试卷(解析版) 题型:选择题
已知:CH3CH2CH2CH3(g)+13/2O2(g)===4CO2(g)+5H2O(l) ΔH=-2 878 kJ/m ol
ol
(CH3)2CHCH3(g)+13/2O2(g)===4CO2(g)+5H2O(l) ΔH=-2 869 kJ/mol
下列说法正确的是
A.正丁烷分子储存的能量大于异丁烷分子
B.正丁烷的稳定性大于异丁烷
C.异丁烷转化为正丁烷的过程是一个放热过程
D.异丁烷分子中的碳氢键比正丁烷的多
查看答案和解析>>
科目: 来源:2015-2016学年浙江省桐乡市高二上期中(普通班)化学试卷(解析版) 题型:选择题
下列说法正确的是
A.氯化钠固体不导电,所以氯化钠是非电解质
B.向纯水中加入碳酸钠能使水的电离平衡正向移动,水的离子积增大
C.如图研究的是铁的吸氧腐蚀,实验中红色首先在食盐水滴的中心出现
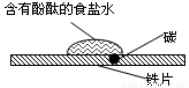
D.常温下,反应4Fe(OH)2(s)+2H2O(l)+O2(g)=4Fe(OH)3(s) 的△H<0 △S<0
查看答案和解析>>
科目: 来源:2015-2016学年浙江省桐乡市高二上期中(普通班)化学试卷(解析版) 题型:选择题
为探究足量锌与稀硫酸的反应速率(以v(H2)表示),向反应混合液中加入某些物质,下列判断正确的是
A.加入NH4HSO4固体,v(H2)不变,生成H2量不变
B.加入少量水,v(H2)减小,生成H2量减少
C.加入CH3COONa固体,v(H2)减小,生成H2量不变
D.滴加少量CuSO4溶液,v(H2)增大,生成H2量减少
查看答案和解析>>
科目: 来源:2015-2016学年浙江省桐乡市高二上期中(普通班)化学试卷(解析版) 题型:选择题
己知N2(g)+3H2(g) 2NH3(g)△H=﹣92.4kJ•mo1﹣1,下列结论正确的是
2NH3(g)△H=﹣92.4kJ•mo1﹣1,下列结论正确的是
A.在密闭容 器中加入1mol N2和3mol H2充分反应放热92.4kJ
器中加入1mol N2和3mol H2充分反应放热92.4kJ
B.N2(g)+3H2(g) 2NH3(l)△H=﹣QkJ•mo1﹣1,则Q>92.4
2NH3(l)△H=﹣QkJ•mo1﹣1,则Q>92.4
C.增大压强,平衡向右移动,平衡常数增大
D.若一定条件下反应达到平衡,N2的转化率为20%,则H2的转化率为60%
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com