
科目: 来源:2015-2016学年安徽省高二上第一阶段测化学试卷(解析版) 题型:选择题
用CH4催化还原NOx可以消除氮氧化物的污染。例如:
CH4(g)+4NO2(g)═4NO(g)+CO2(g)+2H2O(g)△H1=-574kJ•mol-1
CH4(g)+4NO(g)═2N2(g)+CO2(g)+2H2O(g)△H2=-1160kJ•mol-1 若在标准状况下用CH4还原4.48LNO2气体至N2,则下列说法中正确的是( )
A.该过程吸收的热量为86.7kJ
B.此过程中需要CH4气体1.12L
C.转移的电子数为0.8NA个
D.已知2NO(g)+O2(g)═2NO2(g)△H=-114 kJ•mol-1,则CH4的燃烧热是802kJ•mol-1
查看答案和解析>>
科目: 来源:2015-2016学年安徽省高二上第一阶段测化学试卷(解析版) 题型:选择题
某化学研究小组探究外界条件对化学反应mA(g)+nB(g) pC(g)的速率和平衡的影响图像如下,下列判断正确的是( )
pC(g)的速率和平衡的影响图像如下,下列判断正确的是( )
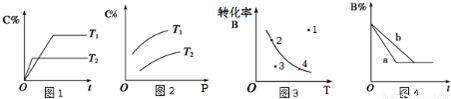
A.由图1可知,T1<T2,该反应正反应为吸热反应
B.由图2可知,该反应m+n<p
C.图3中,表示反应速率v正>v逆的是点3
D.图4中,若m+n=p,则a曲线一定使用了催化剂
查看答案和解析>>
科目: 来源:2015-2016学年安徽省高二上第一阶段测化学试卷(解析版) 题型:选择题
一定温度下,将NO2与SO2以体积比为1:2置于密闭容器中发生NO2(g)+SO2(g) SO3(g)+NO(g) △H= -41.8 kJ•mol-1,测得上述反应平衡时NO2与SO2体积比为1:6,下列说法正确的是( )
SO3(g)+NO(g) △H= -41.8 kJ•mol-1,测得上述反应平衡时NO2与SO2体积比为1:6,下列说法正确的是( )
A.平衡常数K=8/3
B.达到平衡后NO2和SO2的转化率相等
C.SO3和NO的体积比保持不变可以证明达到平衡状态
D.每消耗1molSO3的同时生成1molNO2
查看答案和解析>>
科目: 来源:2015-2016学年安徽省高二上第一阶段测化学试卷(解析版) 题型:选择题
向绝热恒容密闭容器中通入N2和H2,在一定条件下使反应N2(g)+3H2(g) 2NH3(g) △H<0达到平衡,n(NH3)和n(H2)随时间变化的关系如图所示。下列有关叙述正确的是( )
2NH3(g) △H<0达到平衡,n(NH3)和n(H2)随时间变化的关系如图所示。下列有关叙述正确的是( )
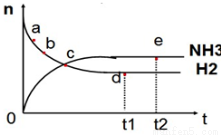
A.c点表示NH3生成速率与NH3分解速率相同
B.c点和e点时反应的平衡常数相同
C.N2的转化率:b>a
D.d点时,n(N2):n(H2):n(NH3)=1:3:2
查看答案和解析>>
科目: 来源:2015-2016学年安徽省高二上第一阶段测化学试卷(解析版) 题型:填空题
在化学反应中,只有极少数能量比平均能量高得多的反应物分子发生碰撞时才可能发生化学反应,这些分子称为活化分子,使普通分子变为活化分子所需提供的最低限度的能量叫活化能,其单位通常用kJ•mol-1表示。请认真观察下图,然后回答问题:
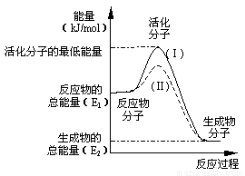
(1)图1中所示反应是____________(填“吸热”或“放热”)反应,该反应的△H=________(用含E1、E2的代数式表示)。
(2)下列4个反应中,符合示意图描述的反应的是_______________(填代号)。
a.盐酸与NaOH反应
b.Na与H2O反应生成H2
c.铝热反应
d.灼热的碳与CO2反应
查看答案和解析>>
科目: 来源:2015-2016学年安徽省高二上第一阶段测化学试卷(解析版) 题型:填空题
研究NO2、SO2、CO等大气污染气体的处理具有重大意义。
(1)NO2可用水吸收,相应的化学反应方程式为_________________________;利用反应6NO2+8NH3═7N2+12H2O也可处理NO2.当转移1.2mol电子时,消耗的NO2在标准状况下是____________L。
(2)已知:
2SO2(g)+O2(g)?2SO3(g)△H=-196.6kJ•mol-1
2NO(g)+O2(g)?2NO2(g)△H=-113.0kJ•mol-1
则反应NO2(g)+SO2(g)?SO3(g)+NO(g)的△H=_______ kJ•mol-1
(3)一定条件下,将NO2与SO2以体积比1:2置于密闭容器中发生上述反应,下列能说明反应达到平衡状态的是_______(填序号)
a.体系压强保持不变 b.混合气体颜色保持不变
c.SO3和NO的体积比保持不变 d.每消耗1mol SO3的同时生成1mol NO2
测得上述反应平衡时NO2与SO2体积比为1:6,则平衡常数K=_______。
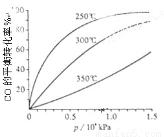
(3)CO可用于合成甲醇,反应方程式为CO(g)+2H2(g)═CH3OH(g).CO在不同温度下的平衡转化率与压强的关系如下图所示.该反应△H_____(填“>”或“<”),实际生产条件控制在250℃、1.3×104kPa左右,选择此压强的理由是_______。
查看答案和解析>>
科目: 来源:2015-2016学年安徽省高二上第一阶段测化学试卷(解析版) 题型:填空题
某研究小组在实验室探究氨基甲酸铵(NH2COONH4)分解反应平衡常数和水解反应速率的测定。
(1)将一定量纯净的氨基甲酸铵固体置于特制的密闭真空容器中(假设容器体积不变,固体试样体积忽略不计),在恒定温度下使其达到分解平衡:NH2COONH4(s) 2NH3(g)+CO2(g).实验测得不同温度下的平衡数据列于如表:
2NH3(g)+CO2(g).实验测得不同温度下的平衡数据列于如表:
温度(℃) | 15.0 | 20.0 | 25.0 | 30.0 | 35.0 |
平衡总压强(kPa) | 5.7 | 8.3 | 12.0 | 17.1 | 24.0 |
平衡气体总浓度 (×10-3mol/L) | 2.4 | 3.4 | 4.8 | 6.8 | 9.4 |
①可以判断该分解反应已经达到化学平衡的是___________;
A.2v(NH3)═v(CO2)
B.密闭容器中总压强不变
C.密闭容器中混合气体的密度不变
D.密闭容器中氨气的体积分数不变
②根据表中数据,列式计算25.0℃时氨基甲酸铵的分解平衡常数___________;
③取一定量的氨基甲酸铵固体放在一个带活塞的密闭真空容器中,在25℃下达到分解平衡.若在恒温下压缩容器体积,氨基甲酸铵固体的质量___________(填“增加”、“减小”或“不变”);
④氨基甲酸铵分解反应的焓变△H______0;
(2)已知:NH2COONH4+2H2O?NH4HCO3+NH3•H2O.该研究小组分别用三份不同初始浓度的氨基甲酸铵溶液测定水解反应速率,得到c(NH2COO-)随时间变化趋势如图所示.
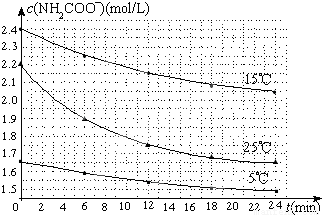
⑤计算25℃时,0~6min氨基甲酸铵水解反应的平均速率______________;
⑥根据图中信息,如何说明水解反应速率随温度升高而增大_____________________。
查看答案和解析>>
科目: 来源:2015-2016学年浙江省桐乡市高二上期中(实验班)化学试卷(解析版) 题型:选择题
下列物质的水溶液因水解而呈碱性的是
A.Ba(OH)2 B.FeCl3 C.NaHSO4 D.CH3COONa
查看答案和解析>>
科目: 来源:2015-2016学年浙江省桐乡市高二上期中(实验班)化学试卷(解析版) 题型:选择题
下列反应过程能量变化如下所示:
H2(g) + Cl2(g) = 2HCl(g) ΔH
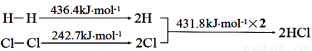
下列说法错误的是
A.H—H键比Cl—Cl键稳定
B.ΔH= — 18 4.5 kJ·mol-1
4.5 kJ·mol-1
C.正反应活化能比逆反应活化能高
D.在相同条件下,1mol H2(g)和1mol Cl2(g)分别在点燃和光照条件下反应生成2mol HCl(g),重新恢复到原来的状态时ΔH相同
查看答案和解析>>
科目: 来源:2015-2016学年浙江省桐乡市高二上期中(实验班)化学试卷(解析版) 题型:选择题
下列措施或事实能用勒夏特列原理解释的是
A.新制的氯水在光照下颜色逐渐变浅
B.H2、I2、HI平衡混合气缩小体积加压后颜色变深
C.工业上生产硫酸的过程中,SO2在催化氧化时条件控制为常压,而不是高压
D.工业上合成氨气时温度选择450℃左右,而不是常温
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com