
科目: 来源:2015-2016学年吉林省高二上期末考试化学试卷(解析版) 题型:选择题
为证明溴乙烷中含有溴元素,向溴乙烷中依次加入下列药品并加热,操作步骤中正确的是①加入硝酸银溶液 ②加入氢氧化钠溶液或加入氢氧化钠醇溶液③加热④加入蒸馏水⑤加入稀硝酸至溶液呈酸性
A.④③①⑤ B.②③⑤① C.④⑤③① D.①②③⑤
查看答案和解析>>
科目: 来源:2015-2016学年吉林省高二上期末考试化学试卷(解析版) 题型:填空题
(1)乙醇的分子结构如右图: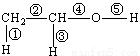 ,其中①②③④⑤表示化学键的代号,用代号回答:
,其中①②③④⑤表示化学键的代号,用代号回答:
i乙醇与钠反应断裂的键是_
ii乙醇与氧气在铜或银作催化剂,加热条件下反应断裂的键是
(2)把一端弯成螺旋状的铜丝放在酒精灯外焰部分加热,看到铜丝表面变成 色。趁热将它反复插入盛乙醇的试管中,铜丝表面又变成 色,并有 气味的物质生成,总反应的化学方程式 。
查看答案和解析>>
科目: 来源:2015-2016学年吉林省高二上期末考试化学试卷(解析版) 题型:填空题
北京奥运会“祥云”火炬燃料是丙烷(C3H8),亚特兰大奥运会火炬燃料是丙烯(C3H6)。
(1)丙烷脱氢可得丙烯。
已知:C3H8(g)═CH4(g)+HC≡CH(g)+H2(g)△H1=+156.6kJ/mol
CH3CH=CH2(g)═CH4(g)+HC≡CH(g)△H2=+32.4kJ/mol
则相同条件下,反应C3H8(g)═CH3CH=CH2(g)+H2(g)的△H= kJ·mol-1。
(2)以丙烷为燃料制作新型燃料电池,电池的正极通入O2和CO2,负极通入丙烷,电解质是熔融碳酸盐。电池反应方程式为 ;放电时CO32-移向电池的 (填“正”或“负”)极。
(3)碳氢化合物完全燃烧生成CO2和H2O。常温常压下,空气中的CO2溶于水,达到平衡时,溶液的pH =5.60,c(H2CO3)=1.5×10-5 mol·L-1。若忽略水的电离及H2CO3的第二步电离,则H2CO3 HCO3-+H+的平衡常数K1= mo1/L。(已知10-5.60=2.5×10-6)
HCO3-+H+的平衡常数K1= mo1/L。(已知10-5.60=2.5×10-6)
(4)常温下,0.1 mo1/L NaHCO3溶液的pH大于8,则溶液中c(H2CO3) c(CO32-)(填“>”、“=”或“<”),原因是 (用简要的文字明)。
查看答案和解析>>
科目: 来源:2015-2016学年广西柳州铁路一中高一上12月月考化学卷(解析版) 题型:选择题
NA为阿伏伽德罗常数的数值,下列叙述错误的有几个( )
①常温常压下,8 g O2含有4NA个电子
②标准状况下,11.2 L氦气中含有0.5 NA个原子
③标准状况下,0.1 mol Cl2参加反应,转移的电子数目一定为0.2 NA
④1 L 0.1 mol·L-1的氨水中有NA个NH4+
⑤1 mol Na与足量O2反应,生成Na2O和Na2O2的混合物,转移电子总数2NA
A.2个 B.3个 C.4个 D.5个
查看答案和解析>>
科目: 来源:2015-2016学年广西柳州铁路一中高一上12月月考化学卷(解析版) 题型:选择题
下列有关硝酸化学性质的叙述中,正确的是 ( )
A.敞口放置的浓硝酸浓度变小是因为浓硝酸的吸水性
B.硝酸可与Na2SO3反应制得SO2气体
C.浓硝酸因分解放出的NO2又溶解于硝酸而呈黄色
D.硝酸能与Fe2O3反应,表现氧化性
查看答案和解析>>
科目: 来源:2015-2016学年广西柳州铁路一中高一上12月月考化学卷(解析版) 题型:选择题
将a g Fe2O3、Al2O3样品溶解在过量的200 mL浓度为0.1 mol·L-1的盐酸溶液中,然后向其中加入NaOH溶液,使Fe3+、Al3+刚好完全沉淀,用去NaOH溶液100 mL,则NaOH溶液的浓度为( )
A.0.1 mol·L-1 B.0.2 mol·L-1 C.0.4 mol·L-1 D.0.8 mol·L-1
查看答案和解析>>
科目: 来源:2015-2016学年广西柳州铁路一中高一上12月月考化学卷(解析版) 题型:填空题
I.(1)鉴别KCl溶液和K2CO3的试剂是 ,除去SO2中的HCl的试剂是 。
(2)除去Na2CO3粉末中混入的NaHCO3杂质用 方法。分离碘和CCl4的操作方法 。
(3)除去混入Fe2O3中少量SiO2杂质的试剂是 ,离子方程式为 。
II.氧化还原反应在工农业生产和日常生活中有广泛的应用,回答下列问题:
(4)罐头厂在装食品罐头时,通常要添加一些对人体无害的防腐剂,防止食物被空气中的氧气氧化而变质,此类食物防腐剂应具有________。(填“氧化性”或“还原性”)
(5)铁是生物体中不可缺少的微量元素,铁在人体中是以Fe2+和Fe3+的形式存在的,而Fe2+更容易被吸收,服用维生素C可使食物中的Fe3+转化为Fe2+,在这个过程中维生素C所起的作用是 。(填“氧化剂”或“还原剂”)
(6)氯气是一种重要的工业原料且HCl遇NH3会产生NH4Cl,NH4Cl为白色固体。工业上利用反应:3Cl2+2NH3===N2+6HCl检查氯气管道是否漏气。下列说法错误的是________。
A.若管道漏气遇NH3就会产生白烟 B.该反应利用了Cl2的强氧化性
C.该反应属于复分解反应 D.生成1 mol N2有6 mol电子转移
查看答案和解析>>
科目: 来源:2015-2016学年甘肃省高二上期末考试化学试卷(解析版) 题型:选择题
下列有关同分异构体数目的叙述中,正确的是
A.甲苯苯环上的一个氢原子被含4个碳原子的烷基取代,所得产物有12种
B.等物质的量的氯气与乙烷在光照条件下反应得到9种产物
C.已知二氯苯有3种同分异构体,则四氯苯的同分异构体的数目为6种
D.苯乙烯和氢气完全加成的产物的一溴取代物有5种
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com