
科目: 来源:2016届陕西省高三上12月模拟化学试卷(解析版) 题型:选择题
已知Fe3O4纳米颗粒稳定、容易生产且用途广泛,是临床诊断、生物技术和环境化学领域多种潜在应用的有力工具,水热法制备Fe3O4纳米颗粒的总反应为:3Fe2++2S2O32-+O2+4OH—=Fe3O4+S4O62-+2H2O,下列说法不正确的是
A.参加反应的氧化剂与还原剂的物质的量之比为1:5
B.若有2molFe2+被氧化,则被Fe2+还原的O2为0.5mol
C.每生成1molFe3O4,则转移电子数为4mol
D.O2是氧化剂,S2O32-和Fe2+是还原剂
查看答案和解析>>
科目: 来源:2016届陕西省高三上12月模拟化学试卷(解析版) 题型:填空题
一氧化碳是一种用途广泛的化工基础原料。
(l)在高温下CO可将SO2还原为单质硫。已知:2CO(g)+O2(g) 2CO2(g) △H1=-566.0kJ·mol-1;S(s)+O2(g)
2CO2(g) △H1=-566.0kJ·mol-1;S(s)+O2(g) SO2(g) △H2=-296.0kJ·mol-1;
SO2(g) △H2=-296.0kJ·mol-1;
请写出CO还原SO2的热化学方程式______________________。
(2)工业上用一氧化碳制取氢气的反应为:CO(g)+H2O(g) CO2(g)+H2(g),已知420℃时,该反应的化学平衡常数K=9。如果反应开始时,在2L的密闭容器中充入CO和H2O的物质的量都是0.60mol,5min末达到平衡,则此时CO的转化率为 ,H2的平均生成速率为 mol·L-1·min-1。
CO2(g)+H2(g),已知420℃时,该反应的化学平衡常数K=9。如果反应开始时,在2L的密闭容器中充入CO和H2O的物质的量都是0.60mol,5min末达到平衡,则此时CO的转化率为 ,H2的平均生成速率为 mol·L-1·min-1。
(3)CO与H2反应还可制备CH3OH,CH3OH可作为燃料使用,用CH3OH和O2组合形成的质子交换膜燃料电池的结构示意图:
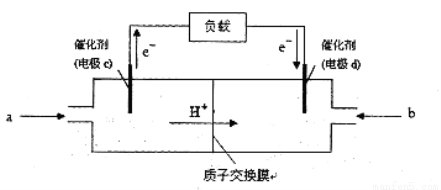
电池总反应为:2CH3OH+3O2=2CO2+4H2O,则c电极是 (填“正极”或“负极”),c电极的反应方程式为 。若用该电池电解精炼铜(杂质含有Ag和Fe),粗铜应该接此电源的________极(填“c”或“d”),反应过程中析出精铜64g,则上述CH3OH燃料电池,消耗的O2在标况下的体积为 L。
查看答案和解析>>
科目: 来源:2016届陕西省高三上12月模拟化学试卷(解析版) 题型:填空题
太阳能电池板材料除单晶硅外,还有铜、铟、镓、硒等化学物质。
(1)铟与镓同是IIIA族元素,写出铟基态原子的电子排布式: 。
(2)硒为第四周期VI A族元素,与其相邻的元素有砷(33号)、溴(35号),则三种元素的电负性由小到大的顺序为 (用元素符号表示)。SeO3分子的立体构型为 。
(3)硅烷(SinH2n+2)的沸点与相对分子质量的关系如图所示,呈现这种变化的原因是 。

(4)硼元素具有缺电子性,其化合物往往具有加合性,如硼酸(H3BO3)在水溶液中能与水反应生成[B(OH)4]-,其中B原子的杂化类型为 。
(5)金属铜投入氨水中或投入H2O2溶液中均无明显现象,但投入氨水—过氧化氢混合液中,则铜片溶解,溶液呈深蓝色,写出该反应的离子方程式: 。
(6)一种铜金合金晶体具有面心立方最密堆积结构,在晶胞中金原子位于顶点,铜原子位于面心,则该合金中金原子(Au)与铜原子(Cu)个数比为 ;若该晶体的晶胞参数为a pm,则该合金密度为 g/cm3。(列出计算式,不要求计算结果,阿伏伽德罗数的值为NA)
查看答案和解析>>
科目: 来源:2016届宁夏银川二中高三上学期统考理综化学试卷(解析版) 题型:选择题
用NA表示阿伏加德罗常数的值,下列叙述中正确的是
A.分子总数为NA的NO2和CO2混合气体中含有的氧原子数为2NA
B.常温常压下,0.1mol铁在0.1molC12中充分燃烧,转移的电子数为0.3NA
C.0.1mol/L的K2CO3溶液中CO32-数小于0.1NA
D.0.5mol雄黄(As4S4,结构如图 )含有NA个S—S键
)含有NA个S—S键
查看答案和解析>>
科目: 来源:2016届宁夏银川二中高三上学期统考理综化学试卷(解析版) 题型:选择题
下列有关说法不正确的是
A.25℃时,0.1mol·L-1的三种溶液的pH关系为:pH(Na2CO3) >pH(NaHCO3) > pH(CH3COONa)
B.25℃时,pH=5的CH3COOH溶液和pH=5的NH4Cl溶液,c(H+)相等
C.25℃时,BaCO3在纯水中的KSP比在Na2CO3溶液中的KSP大。
D.NaHCO3和Na2CO3混合溶液中,一定有c(Na+)+c(H+)=c(OH-)+c(HCO3-)+2c(CO32-)
查看答案和解析>>
科目: 来源:2016届宁夏银川二中高三上学期统考理综化学试卷(解析版) 题型:填空题
氯气是一种重要的化工原料。某学习小组在实验室中利用如图所示装置制取氯气并探究其性质。
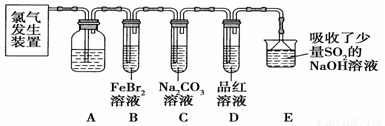
(1)实验室用二氧化锰和浓盐酸加热制取氯气,发生装置中除圆底烧瓶和导管外还需用到的玻璃仪器有 、 。
(2)装置A中盛有的试剂是: ,作用是:________________________。
(3)若D中品红溶液褪色,则B装置发生反应的离子方程式是: 。
(4)证明FeBr2与Cl2发生了(3)中氧化还原反应的实验方法是: (填操作方法)。
某研究性学习小组用刚吸收过少量SO2的NaOH溶液吸收处理上述实验后的尾气。经分析吸收尾气一段时间后,吸收液(呈强碱性)中肯定存在Cl-、OH-、CO32-和SO32-,对于可能存在的其他阴离子,研究小组提出以下3种假设:
假设1:只存在SO32-; 假设2:只存在ClO-; 假设3:既不存在SO32-,也不存在ClO-。
(5)学习小组判断同时存在SO32-和ClO-是不可能的,理由是: 。
(6)现限选以下试剂,设计实验方案,进行实验,请写出实验步骤以及预期现象和结论。
a. 3 mol·L-1 H2SO4 b.0.01 mol·L-1 KMnO4 c.1 mol·L-1 BaCl2溶液
d.淀粉碘化钾溶液 e.酚酞试液
步骤一:取少量吸收液于试管中,滴加3 mol·L-1 H2SO4至溶液呈中性,然后将所得溶液分装于A、B两试管中。
步骤二:向A试管中滴加少量 (填序号),若溶液__________________(填现象),则假设1成立。
步骤三:向B试管中滴加少量 (填序号),若溶液__________________(填现象),则假设2成立。
查看答案和解析>>
科目: 来源:2016届宁夏固原一中高三上适应性训练理综化学试卷(解析版) 题型:选择题
下列叙述正确的是
A.氯化铵、次氯酸钠、醋酸铵、硫酸钡都是强电解质
B.电解、电泳、电离、电化学腐蚀均需在通电条件下才能进行
C.红宝石、水晶、钻石的主要成分都是二氧化硅
D.福尔马林、水玻璃、氨水、胆矾均为混合物
查看答案和解析>>
科目: 来源:2016届宁夏固原一中高三上适应性训练理综化学试卷(解析版) 题型:选择题
工业上常用电解硫酸钠溶液联合生产硫酸和烧碱溶液的装置如图所示,其中阴极和阳极均为惰性电极.测得同温同压下,气体甲与气体乙的体积比约为1:2,以下说法正确的是
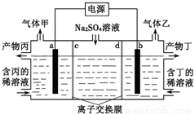
A.a极与电源的负极相连
B.产物丙为硫酸溶液
C.离子交换膜d为阴离子交换膜
D.a电极反应式:2H2O+2e-=H2↑+2OH-
查看答案和解析>>
科目: 来源:2016届宁夏固原一中高三上适应性训练理综化学试卷(解析版) 题型:实验题
亚氯酸钠(NaClO2)是重要漂白剂,探究小组开展如下实验,回答下列问题:
实验Ⅰ:制取NaClO2晶体按如下图装置进行制取。
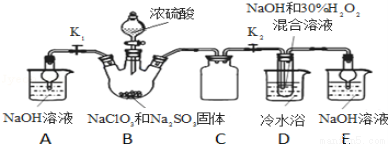
已知:NaClO2饱和溶液在低于38℃时析出NaClO2•3H2O,高于38℃时析出NaClO2,高于60℃时NaClO2分解成NaClO3和NaCl。
(1)装置C的作用是 ;
(2)已知装置B中的产物有ClO2气体,则装置B中反应的方程式为 ;装置D中反应生成NaClO2的化学方程式为 ;反应后的溶液中阴离子除了ClO2﹣、ClO3﹣、Cl﹣、ClO﹣、OH﹣外还可能含有的一种阴离子是 ;检验该离子的方法是 ;
(3)如果撤去D中的冷水浴,可能导致产品中混有的杂质是 ;
实验Ⅱ:样品杂质分析与纯度测定
(4)测定样品中NaClO2的纯度.测定时进行如下实验:
①准确称取所得亚氯酸钠样品m g于烧杯中,加入适量蒸馏水和过量的碘化钾晶体,再滴入适量的稀硫酸,充分反应(已知:ClO2-+4I-+4H+=2H2O+2I2+Cl-);将所得混合液配成250 mL待测溶液。
②移取25.00 mL待测溶液于锥形瓶中,加几滴淀粉溶液,用c mol·L-1 Na2S2O3标准液滴定,至滴定终点。重复2次,测得平均值为V mL(已知:I2+2S2O32-=2I-+S4O62-)。
达到滴定终点时的现象为________________。该样品中NaClO2的质量分数为____________(用含m、c、V的代数式表示)。
查看答案和解析>>
科目: 来源:2016届宁夏固原一中高三上适应性训练理综化学试卷(解析版) 题型:填空题
碳元素在生产生活中具有非常重要的作用,在新物质的制备中也发挥了举足轻重的作用。碳元素的单质有多种形式,下图依次是C60、石墨和金刚石的结构图:
(1)与碳同周期,且基态原子的核外未成对电子数与碳相等的元素,其基态原子的电子排布式为 。
(2)金刚石、石墨、C60、碳纳米管等都是碳元素的单质形式,它们互为 。
(3)金刚石、石墨烯(指单层石墨)中碳原子的杂化形式分别为 、 。常温条件下丙烯是气态,而相对分子质量比丙烯小的甲醇,常温条件下却呈液态,出现这种现象的原因 。
(4)C60属于 晶体(,C60晶体内含有的微粒间作用有 。
(5)金刚石晶胞含有 个碳原子。若碳原子半径为r,金刚石晶胞的边长为a,根据硬球接触模型,则r= a,列式表示碳原子在晶胞中的空间占有率 (不要求计算结果)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com