
科目: 来源:2016届西藏日喀则高级中学高三上期末理综化学试卷(解析版) 题型:选择题
利用实验仪器(规格和数量不限),能完成相应实验的一项是( )
选项 | 实验仪器(省略夹持装置) | 相应实验 |
A | 烧杯、玻璃棒、酒精灯 | CuSO4溶液的浓缩结晶 |
B | 蒸馏烧瓶、冷凝管、酒精灯 | 由工业酒精制无水酒精 |
C | 天平、玻璃棒、胶头滴管、容量瓶 | 配制0.5mol•L-1的溶液100mL |
D | 烧杯、玻璃棒、胶头滴管、分液漏斗 | 用溴水和CCl4除去NaBr溶液中的少量NaI |
查看答案和解析>>
科目: 来源:2016届西藏日喀则高级中学高三上期末理综化学试卷(解析版) 题型:选择题
已知HCO3-+AlO2-+H2O=CO32-+Al(OH)3↓;将足量的KHCO3溶液不断滴入含等物质的量的KOH、Ba(OH)2、KAlO2的混合溶液中,生成沉淀的物质的量与滴入的KHCO3溶液体积的关系可表示为( )
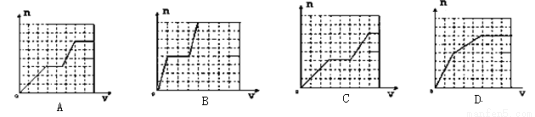
查看答案和解析>>
科目: 来源:2016届西藏日喀则高级中学高三上期末理综化学试卷(解析版) 题型:实验题
[化学选修2—化学与技术]
为了回收利用废钒催化剂(含有V2O5、VOSO4及不溶性残渣),科研人员最新研制了一种离子交换法回收钒的新工艺,主要流程如下:
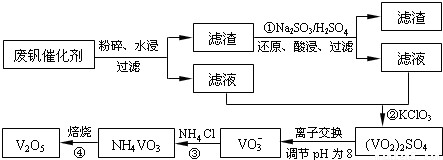
部分含钒物质在水中的溶解性如下:
物质 | VOSO4 | V2O5 | NH4VO3 | (VO2)2SO4 |
溶解性 | 可溶 | 难溶 | 难溶 | 易溶 |
回答下列问题:
(1)工业由V2O5冶炼金属钒常用铝热剂法,该反应的氧化剂为______________;
(2)滤液中含钒的主要成分为____________(填化学式);
(3)该工艺中反应③的沉淀率(又称沉钒率)是回收钒的关键之一,该步反应的离子方程式______________;沉钒率的高低除受溶液pH影响外,还需要控制氯化铵系数(NH4Cl加入质量与料液中V2O5的质量比)和温度.根据下图判断最佳控制氯化铵系数和温度为________、______℃;
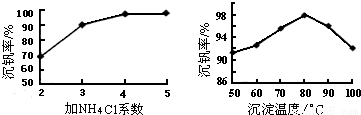
(4)用硫酸酸化的H2C2O4溶液滴定(VO2)2SO4溶液,以测定反应②后溶液中含钒量,反应方程式为:2VO2++H2C2O4+2H+=2VOn++2CO2↑+mH2O,其中n、m分别为_______、______;
(5)全矾液流电池的电解质溶液为VOSO4溶液,电池的工作原理为:VO2++H2O+V3+ 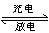 VO2++V2++2H+,电池放电时正极的电极反应式为______________。
VO2++V2++2H+,电池放电时正极的电极反应式为______________。
查看答案和解析>>
科目: 来源:2016届陕西省高三上期末化学试卷(解析版) 题型:选择题
下列说法正确的是( )
A.H2SO4、CH3CH2OH、CH3COONa和CaO分别属于酸、碱、盐和氧化物
B.蔗糖、硫酸钡和水分别属于非电解质、强电解质和弱电解质
C.Mg、Al、Cu可以分别用置换法、直接加热法和电解法冶炼得到
D.日常生活中无水乙醇常用于杀菌消毒
查看答案和解析>>
科目: 来源:2016届陕西省高三上期末化学试卷(解析版) 题型:选择题
设NA为阿伏加罗常数的值,下列说法正确的是( )
A.标准状况下,22.4LCH2Cl2中含有C—Cl键数目为0.2NA
B.常温常压下,3.0g尿素与乙酸的混合物,含氢原子总数为0.2NA
C.常温常压下,10g92%酒精水溶液含氧原子总数为0.2NA
D.常温常压下,0.1molNa2O2与水完全反应转移电子数为0.2NA
查看答案和解析>>
科目: 来源:2016届陕西省高三上期末化学试卷(解析版) 题型:选择题
下列离子方程式书写正确的是( )
A.向铝铵矾NH4Al(SO4)2·12H2O溶液中加入过量Ba(OH)2溶液:
Al3++2SO42-+2Ba2++4OH-═AlO2-+2BaSO4↓+2H2O
B.H218O中投入Na2O2固体:2H218O+2Na2O2=4Na++4OH-+18O2↑
C.碳酸氢钙溶液中加过量澄清石灰水:Ca2++OH-+HCO3-=CaCO3↓+H2O
D.碳酸钠的水解反应:CO32-+H3O+=HCO3-+H2O
查看答案和解析>>
科目: 来源:2016届陕西省高三上期末化学试卷(解析版) 题型:选择题
将一定量的Na2O2和NaHCO3混合后,在密闭容器中加热充分反应,排出气体,冷却后有固体物质剩余,下列选项不正确的是( )
Na2O2/mol | NaHCO3/mol | 气体成分 | |
A | 1 | 2 | Na2CO3 |
B | 1.5 | 2 | Na2O2 Na2CO3 |
C | 2 | 1 | Na2CO3、NaOH、Na2O2 |
D | 2 | 2 | NaOH、Na2CO3 |
查看答案和解析>>
科目: 来源:2016届陕西省高三上期末化学试卷(解析版) 题型:选择题
将一定量的镁和铜组成的混合物加入到稀硝酸中,金属完全溶解(假设反应中还原产物只有NO),向反应后的溶液中加入3mol/LNaOH溶液到沉淀完全,测得生成沉淀的质量比原合金的质量增加 5.1g.下列叙述不正确的是( )
A.当金属全部溶解时,参加反应的硝酸的物质的量一定是0.4mol
B.参加反应的金属的总质量3.6g<m<9.6g
C.当生成的沉淀量达到最大时,消耗NaOH溶液的体积V=100mL
D.当金属全部溶解时收集到NO气体的体积在标况下为2.24L
查看答案和解析>>
科目: 来源:2016届陕西省高三上期末化学试卷(解析版) 题型:实验题
铝元素在自然界中主要存在于铝土矿(主要成分为Al2O3,还含有Fe2O3、FeO、SiO2)中,工业上用铝土矿制备铝的某种化合物的工艺流程如图1.
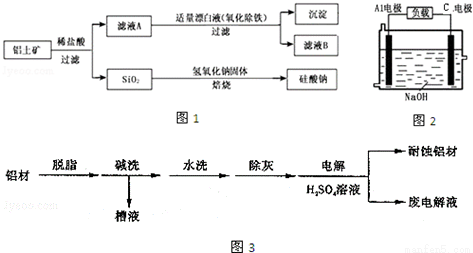
(1)在滤液A中加入漂白液,目的是氧化除铁,所得滤液B显酸性.
①检验滤液B中是否还含有铁元素的方法为______________________(注明试剂、现象);
②由滤液B制备氯化铝晶体涉及的操作为:边滴加浓盐酸边蒸发浓缩、___________ 、_________、洗涤;
(2)新型铝空气电池具有比能量大、质量轻、无毒和危险性等优点.Al电极易被NaOH溶液腐蚀,这是该电池目前未能推广使用的原因之一,电极被腐蚀的离子方程式为
(3)对金属制品进行抗腐蚀处理,可延长其使用寿命.图3为铝材表面处理的一种方法
①碱洗的目的是除去铝材表面的自然氧化膜,原理是___________________________(用离子方程式表示).为将碱洗槽液中铝元素以沉淀形式回收,最好向槽液中加入下列试剂中的___________
a.NH3 b.CO2 c.NaOH d.HNO3
②以铝材为阳极,在H2SO4 溶液中电解,铝材表面形成氧化膜,则阳极电极反应为______________;取少量废电解液,加入NaHCO3,溶液后产生气泡和白色沉淀,产生沉淀的原因是______________.(用离子方程式表示)。
查看答案和解析>>
科目: 来源:2016届山西省高三上12月月考化学试卷(解析版) 题型:选择题
某研究性学习小组讨论甲、乙、丙、丁四种仪器装置的有关用法,其中不合理的是( )
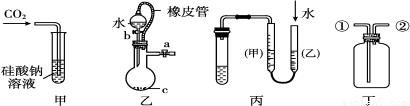
A.甲装置:可用来证明碳的非金属性比硅强
B.乙装置:橡皮管的作用是能使水顺利流下
C.丙装置:用图示的方法不能检查此装置的气密性
D.丁装置:先从①口进气集满二氧化碳,再从②口进气,可收集氢气
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com