
科目: 来源:2015-2016学年江苏省高一上第二次月考化学试卷(解析版) 题型:实验题
金属钠与水的反应是中学化学中的一个重要反应。教材中该实验曾出现过几种不同的演示方法,分别如下图中甲、乙、丙所示:

(1)现按图甲所示的方法,在室温时,向盛有饱和Ca(OH)2溶液的水槽中加入一小块金属钠。下列现象描述正确的是________(填字母).
A.钠浮在液面上,并四处游动,最后消失
B.钠熔化成一个光亮的小球
C.溶液底部有银白色物质生成
D.恢复到室温时,水槽底部有固体物质析出
(2)请补充并完成甲实验从试剂瓶中取出钠到向水槽中投入钠的有关操作:用镊子从试剂瓶中取出一小块钠→__________________→用镊子夹取切好的金属钠投入到盛有Ca(OH)2溶液的水槽中。
(3)通过钠和水反应的实验,我们可以得到钠的物理性质有:____________。
(4)用装满水的矿泉水瓶按图丙所示方法进行实验,用手挤压矿泉水瓶(排出水的体积为16.8mL)再塞紧带有钠的塞子。待钠反应结束后,干瘪的带塞矿泉水瓶恢复成原状,假设瓶内、瓶外均属于标准状况,则所用的钠的质量为________。
查看答案和解析>>
科目: 来源:2015-2016学年江苏省高一上第二次月考化学试卷(解析版) 题型:计算题
将一定质量的铁、氧化铁、氧化铜的混合物粉末放入100mL4.40mol/L盐酸中,充分反应后产生896mLH2(标准状况),残留固体1.28g。过滤,滤液中无Cu2+。将滤液加水稀释到200mL,测得其中c(H+)为0.400mol/L。求原混合物中单质铁的质量。
查看答案和解析>>
科目: 来源:2016届浙江省金丽衢十二校高三上学期第一次联考化学试卷(解析版) 题型:选择题
下列有关物质的性质和该性质的应用均正确的是
A.NH3溶于水后显碱性,在FeCl3饱和溶液中通入足量NH3可制取Fe(OH)3胶体
B.NaHCO3能与碱反应,食品工业上用作焙制糕点的膨松剂
C.Mg(OH)2分解吸热且生成高熔点固体,可用作阻燃剂
D.铜的金属活动性比铝弱,可用铜罐代替铝罐贮运浓硝酸
查看答案和解析>>
科目: 来源:2016届浙江省金丽衢十二校高三上学期第一次联考化学试卷(解析版) 题型:选择题
常温下,下列各组离子在指定溶液中一定能大量共存的是
A.c(H+)/c(OH-)=1×10-12的溶液:K+、Na+、AlO2-、CO32-
B.能溶解Al2O3的溶液:Na+、K+、HCO3-、NO3-
C.饱和氯水中:Cl-、NO3-、Na+、SO32-
D.能使甲基橙显红色的溶液:K+、Fe2+、Cl-、NO3-
查看答案和解析>>
科目: 来源:2016届浙江省金丽衢十二校高三上学期第一次联考化学试卷(解析版) 题型:选择题
已知反应:2NO2(g)+4CO(g) N2(g)+4CO2(g) ΔH<0。将一定量的NO2与CO充入装有催化剂的注射器中后封口。右图是在拉伸和压缩注射器的过程中气体透光率随时间的变化(气体颜色越深,透光率越小)。下列说法不正确的是
N2(g)+4CO2(g) ΔH<0。将一定量的NO2与CO充入装有催化剂的注射器中后封口。右图是在拉伸和压缩注射器的过程中气体透光率随时间的变化(气体颜色越深,透光率越小)。下列说法不正确的是
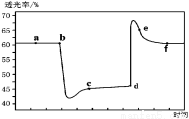
A.b点的操作是快速压缩注射器
B.c点与a点相比,c(NO2)、c(N2)都增大
C.e点: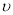 (正) <
(正) <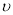 (逆)
(逆)
D.若考虑体系温度变化,且没有能量损失,则平衡常数K(c) >K(f)
查看答案和解析>>
科目: 来源:2016届浙江省金丽衢十二校高三上学期第一次联考化学试卷(解析版) 题型:选择题
下列四位同学设计的实验方案能达到实验目的的是
A.甲同学为测定0.01mol·L-1盐酸的pH值:用湿的玻璃棒蘸取盐酸,点在pH试纸上
B.乙同学要检验(NH4)2Fe(SO4)2·12H2O晶体中的NH4+:取少量晶体溶于水,加入足量浓NaOH溶液并加热,再用湿润的蓝色石蕊试纸检验产生的气体
C.丙同学为检验Fe3O4中+2价铁元素:先用稀盐酸溶解Fe3O4,再滴加KMnO4溶液
D.丁同学要验证FeCl3与KI反应的限度:可将少量的FeCl3溶液与过量的KI溶液混合,充分反应后用CCl4萃取,静置,再滴加KSCN溶液
查看答案和解析>>
科目: 来源:2016届浙江省金丽衢十二校高三上学期第一次联考化学试卷(解析版) 题型:选择题
已知Ka1(H2CO3)>Ka(HClO)>Ka2(HCO3-)。现将0.1 mol·L-1次氯酸溶液与0.1 mol·L-1碳酸钠溶液等体积混合,在所得混合溶液中各种离子浓度关系正确的是
A.c(Na+)>c(ClO-)>c(HCO3-)>c(H+)
B.c(Na+)>c(HCO3-)>c(ClO-)>c(OH-)
C.c(HClO)+c(ClO-)=c(HCO3-)+c(H2CO3)
D.c(Na+)+c(H+)=c(HCO3-)+c(ClO-)+c(OH-)+c(CO32-)
查看答案和解析>>
科目: 来源:2016届浙江省金丽衢十二校高三上学期第一次联考化学试卷(解析版) 题型:填空题
中科院大连化学物理研究所的“煤基甲醇制取低碳烯烃技术(简称DMTO)”荣获2014年度国家技术发明一等奖。DMTO技术主要包括煤的气化、液化、烯烃化三个阶段,相关反应的热化学方程式如下:
(i)煤气化制合成气:C(s)+H2O(g) CO(g)+H2(g)
CO(g)+H2(g)
(ii)煤液化制甲醇:CO(g)+2H2(g) CH3OH(g)
CH3OH(g)
(iii)甲醇制取低碳烯烃:2CH3OH(g) C2H4(g)+2H2O(g) ΔH= -11.72kJ·mol-1……(a)
C2H4(g)+2H2O(g) ΔH= -11.72kJ·mol-1……(a)
3CH3OH(g) C3H6(g)+3H2O(g) ΔH= -30.98kJ·mol-1……(b)
C3H6(g)+3H2O(g) ΔH= -30.98kJ·mol-1……(b)
回答下列问题:
(1)已知:C(s)+CO2(g)=2CO(g) ΔH= +172.5kJ·mol-1,
CO(g)+H2O(g)=CO2(g)+H2(g) ΔH= -41.0kJ·mol-1
反应(i)能自发进行的条件是 (填“高温”、“低温”或“任何温度”)。
(2)反应(ii)中以氢碳[n(H2)∶n(CO)]投料比为2制取甲醇,温度、压强与CO的平衡转化率关系如下图1。
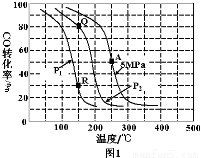
①对于气体参与的反应,表示平衡常数Kp时用气体组分(B)的平衡压强p(B)代替该气体物质的量浓度c(B),则A点时反应(ii)的Kp= (保留两位有效数字,分压=总压×物质的量分数)。
②比较P1 P2,Kp(Q) Kp(R)(填“大于”、“小于”或“等于”)。
③工业上常以铜基催化剂,压强5MPa,温度275℃下发生反应(ii),CO转化率可达到40%左右。为提高CO转化率除了可以适当改变反应温度和压强外,还可以采取的措施有 (写出2个)。
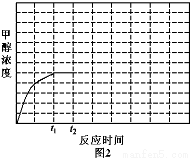
④若反应(ii)在恒容密闭容器内进行,T1温度下甲醇浓度随时间变化曲线如图2所示;不改变其他条件,假定t2时刻迅速降温到T2,t3时刻体系重新达到平衡。试在图中画出t2时刻后甲醇浓度随时间变化趋势图(在图中标出t3)。
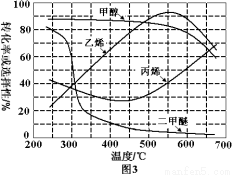
(3)烯烃化阶段:在常压和某催化剂作用下,甲醇的平衡转化率及乙烯、丙烯等物质的选择性(指除了水蒸气以外的产物中乙烯、丙烯等物质的物质的量分数)与反应温度之间的关系如图3。为尽可能多地获得乙烯,控制反应温度为550℃的理由是 。
查看答案和解析>>
科目: 来源:2016届西藏自治区拉萨中学高三上学期第四次月考化学试卷(解析版) 题型:选择题
下列叙述正确的是
A.SO2具有还原性,故可作漂白剂
B.Na的金属活动性比Mg强,故可用Na与MgCl2溶液反应制Mg
C.浓硝酸中的HNO3见光会分解,故有时在实验室看到的浓硝酸呈黄色
D.Fe在Cl2中燃烧生成FeCl3,故在与其它非金属反应的产物中Fe也显+3价
查看答案和解析>>
科目: 来源:2016届西藏自治区拉萨中学高三上学期第四次月考化学试卷(解析版) 题型:选择题
下列反应所得溶液中一定只含一种溶质的是
A.向稀硝酸中加入铁粉
B.向氯化铝溶液中加入过量的氨水
C.向NaOH溶液中通入CO2气体
D.向MgSO4、H2SO4的混合液中加入过量的Ba(OH)2溶液
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com