
科目: 来源:2015-2016学年江西省高二上期中考试化学试卷(解析版) 题型:填空题
市售一次电池品种很多,碱性锌锰电池在日常生活中用量很大。回收废旧锌锰电池并进行重新处理,可以获得MnO2及其他副产品,其工艺流程如下:
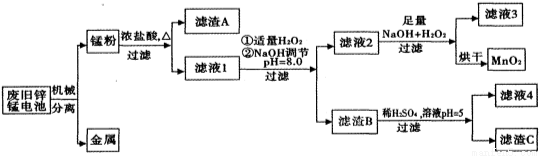
已知:“锰粉”的主要成分有MnO2、Zn(OH)2、MnOOH、碳粉,还含有少量铁盐和亚铁盐。常温下,生成氢氧化物沉淀的pH如下表:
物质 | Fe(OH)3 | Fe(OH)2 | Zn(OH)2 | Mn(OH)2 / Mn(OH)3 |
开始沉淀pH | 2.7 | 7.6 | 5.7 | 8.3 |
完全沉淀pH(c≤1.0×10-5mol/L) | 3.7 | 9.6 | 8.0 | 8.8 |
(1)加入NaOH溶液调节pH=8.0,目的是____________________;计算常温下Zn(OH)2的溶度积常数Ksp[Zn(OH)2]=____________________。
(2)写出滤液2中的Mn2+变成MnO2的离子方程式_________________________。
(3)写出滤渣B与稀硫酸在pH=5时反应的化学方程式______________________。
(4)工艺中还可以将滤液4进行_____________、_____________、_____________、洗涤得到含结晶水的硫酸盐晶体。
(5)MnO2常用来制取KMnO4。在一定条件下将MnO2氧化为K2MnO4,然后用铁作阴极、铂作阳极电解K2MnO4溶液得到KMnO4。电解K2MnO4溶液的总反应方程式为______________________。
查看答案和解析>>
科目: 来源:2015-2016学年湖南省高二上第三次月考化学试卷(解析版) 题型:选择题
下列有关热化学方程式书写正确的是
已知条件 | 热化学方程式 | |
A | 中和热为57.3 kJ/mol | H2SO4(aq)+Ba(OH)2(aq)=BaSO4(s)+2H2O(l) ΔH=-114.6 kJ/mol |
B | 合成氨反应生成0.1 mol NH3时放出a kJ热量 | N2(g)+3H2(g) |
C | H2的燃烧热为285.8 kJ/mol | H2(g)+1/2O2(g)=H2O(g) ΔH=-285.8 kJ/mol |
D | 碳的燃烧热为393.5 kJ/mol | 2C(s)+O2(g)=2CO(g)ΔH=-787 kJ/mol |
查看答案和解析>>
科目: 来源:2015-2016学年湖南省高二上第三次月考化学试卷(解析版) 题型:选择题
下列反应水解方程式正确的是
A.AlCl3+3H2O=Al(OH)3+3HCl
B.Na2CO3+2H2O H2CO3+2NaOH
H2CO3+2NaOH
C.碳酸氢钠溶液:HCO3-+H2O H2CO3+OH—
H2CO3+OH—
D.NH4Cl溶于D2O中:NH4++D2O NH3·D2O+H+
NH3·D2O+H+
查看答案和解析>>
科目: 来源:2015-2016学年湖南省高二上第三次月考化学试卷(解析版) 题型:选择题
某温度下,对于反应N2(g)+3H2(g) 2NH3(g) ΔH=-92.4kJ/mol。N2的平衡转化率(α)与体系总压强(p)的关系如图所示。下列说法正确的是
2NH3(g) ΔH=-92.4kJ/mol。N2的平衡转化率(α)与体系总压强(p)的关系如图所示。下列说法正确的是
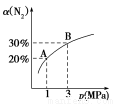
A.将1 mol氮气、3 mol氢气,置于1 L密闭容器中发生反应,放出的热量为92.4 kJ
B.平衡状态由A变到B时,平衡常数K(A)<K(B)
C.上述反应在达到平衡后,增大压强,H2的转化率增大
D.升高温度,平衡向逆反应方向移动,说明逆反应速率增大,正反应速率减小
查看答案和解析>>
科目: 来源:2015-2016学年湖南省高二上第三次月考化学试卷(解析版) 题型:选择题
室温下向10mL0.1 mol·L-1NaOH溶液中加入0.1 mol·L-1的一元酸HA溶液pH的变化曲线如图所示。下列说法正确的是
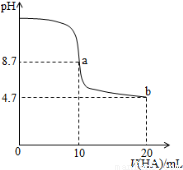
A.a点所示溶液中c(Na+)>c(A—)>c(H+)>c(HA)
B.a、b两点所示溶液中水的电离程度相同
C.pH=7时,c(Na+)= c(A—)+ c(HA)
D.b点所示溶液中c(A—)> c(HA)
查看答案和解析>>
科目: 来源:2015-2016学年湖南省高二上第三次月考化学试卷(解析版) 题型:填空题
FeCl3 具有净水作用,但腐蚀设备,而聚合氯化铁是一种新型的絮凝剂,处理污水比FeCl3 高效,且腐蚀性小。(已知25℃Ksp[Fe(OH)3]=4.0×10﹣38 lg2=0.3)
请回答下列问题:
(1)FeCl3 净水的原理是____________ 。(用离子方程式表示),Fe3+水解生成的Fe(OH)3胶体粒子能吸附水中的悬浮杂质,常温下此反应的平衡常数为_________________(填写数值)。
(2)将FeCl3 溶液与NaHCO3 溶液混合,其离子方程式为 _______________。
(3)25℃时pH=3的溶液中,c(Fe3+)= mol•L﹣1要使Fe3+ 沉淀完全,pH应大于________。
(4)FeCl3 在溶液中分三步水解:
Fe3++H2O  Fe(OH)2++H+ K1
Fe(OH)2++H+ K1
Fe(OH)2++H2O Fe(OH)2++H+ K2
Fe(OH)2++H+ K2
Fe(OH)++H2O Fe(OH)3+H+ K3
Fe(OH)3+H+ K3
以上水解反应的平衡常数K1、K2、K3由大到小的顺序是 。
通过控制条件,以上水解产物聚合,生成聚合氧化铁,离子方程式为:
xFe3++yH2O Fex(OH)y(3x-y)++yH+ 欲使平衡正向移动可采用的方法是(填序号) 。
Fex(OH)y(3x-y)++yH+ 欲使平衡正向移动可采用的方法是(填序号) 。
a.降温 b.加水稀释 c.加入NH4Cl d.加入NaHCO3
(5) FeCl3溶液可腐蚀印刷电路板,其反应为Cu +2FeCl3=CuCl2+2FeCl2 要将此反应设计在原电池中进行,则正极反应式为__________。
查看答案和解析>>
科目: 来源:2015-2016学年福建省高一上第二次月考化学试卷(解析版) 题型:选择题
下列变化过程中,需要加入还原剂的是
A.MnO2→MnO4- B.Al(OH)4-→Al(OH)3 C.SO32-→SO42- D.MnO2→MnCl2
查看答案和解析>>
科目: 来源:2015-2016学年福建省高一上第二次月考化学试卷(解析版) 题型:选择题
某无色溶液中,可大量共存的离子组是
A.Na+、HCO3-、SO42-、Cl- B.Cu3+、NO3-、Cl-、SO42-
C.H+、Cl-、Na+、CO32- D.Fe3+、Na+、OH-、NO3-
查看答案和解析>>
科目: 来源:2015-2016学年福建省高一上第二次月考化学试卷(解析版) 题型:选择题
下列物质分类的正确组合是
碱 | 酸 | 盐 | 酸性氧化物 | |
A | 纯碱 | 硝酸 | 烧碱 | 二氧化硫 |
B | 烧碱 | 硫酸 | 食盐 | 一氧化碳 |
C | 苛性钠 | 醋酸 | 石灰石 | 水 |
D | 苛性钾 | 碳酸 | 碳酸氢钠 | 二氧化碳 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com