
科目: 来源:2016届河北省衡水市高三上一轮复习检测二化学试卷(解析版) 题型:选择题
下列说法不正确的是( )
A.Na与H2O的反应是熵增的放热反应,该反应能自发进行
B.饱和Na2SO4溶液或浓硝酸均可使蛋白质溶液产生沉淀,但原理不同
C.FeCl3和MnO2均可加快H2O2分解,同等条件下二者对H2O2分解速率的改变相同
D.Mg(OH)2固体在溶液中存在平衡:Mg(OH)2(s) Mg2+(aq)+2OH—(aq),该固体可溶于NH4Cl溶液
Mg2+(aq)+2OH—(aq),该固体可溶于NH4Cl溶液
查看答案和解析>>
科目: 来源:2016届河北省衡水市高三上一轮复习检测二化学试卷(解析版) 题型:选择题
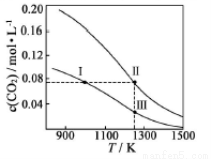
在体积均为1.0L的两个恒容密闭容器中加入足量的相同的碳粉,再分别加入0.1molCO2和0.2molCO2,在不同温度下反应CO2(g)+C(s)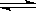 2CO(g)达到平衡,平衡时CO2的物质的量浓度c(CO2)随温度的变化如图所示(图中Ⅰ、Ⅱ、Ⅲ点均处于曲线上)。下列说法正确的是( )
2CO(g)达到平衡,平衡时CO2的物质的量浓度c(CO2)随温度的变化如图所示(图中Ⅰ、Ⅱ、Ⅲ点均处于曲线上)。下列说法正确的是( )
A.反应CO2(g)+c(s)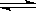 2CO(g) △S>0、△H<0
2CO(g) △S>0、△H<0
B.体系的总压强P总:P总(状态Ⅱ)>2P总(状态Ⅰ)
C.体系中c(CO):c(CO,状态Ⅱ) >2c(CO,状态Ⅲ)
D.逆反应速率V逆:V逆(状态Ⅰ)>V逆(状态Ⅲ)
查看答案和解析>>
科目: 来源:2016届河北省衡水市高三上一轮复习检测二化学试卷(解析版) 题型:填空题
I.氨是合成硝酸、铵盐和氮肥的基本原料,回答下列问题:
(1)氨的水溶液显弱碱性,其原因为 (用离子方程式表示),0.1 mol·L-1的氨水中加入少量的NH4Cl固体,溶液的PH (填“升高”或“降低”);若加入少量的明矾,溶液中的NH4+的浓度 (填“增大”或“减小”)。
(2)硝酸铵加热分解可得到N2O和H2O,250℃时,硝酸铵在密闭容器中分解达到平衡,该分解反应的化学方程式为 ,平衡常数表达式为 ;
Ⅱ.25℃,在0.10mol·L-1H2S溶液中,通入HCl气体或加入NaOH固体以调节溶液pH,溶液pH与c(S2-) 关系如右图(忽略溶液体积的变化、H2S的挥发)。

①pH=13时,溶液中的c(H2S)+c(HS-)= mol·L-1.
②某溶液含0.020 mol·L-1Mn2+、0.10 mol·L-1H2S,当溶液pH= 时,Mn2+开始沉淀。[已知:Ksp(MnS)=2.8×10-13]
查看答案和解析>>
科目: 来源:2016届甘肃省高三上学期第四次月考理综化学试卷(解析版) 题型:选择题
下列有关操作或说法正确的是
A.浓硫酸溅到皮肤上时立即用稀氢氧化钠溶液冲洗
B.金属汞一旦洒落到实验室地面或桌面时,必须尽可能收集,并深埋处理
C.金属钠着火时用泡沫灭火器灭火
D.加工后具有吸水性的植物纤维可用作食品干燥剂
查看答案和解析>>
科目: 来源:2016届甘肃省高三上学期第四次月考理综化学试卷(解析版) 题型:选择题
下列说法正确的是
A.(NH4)2Fe(SO4)2溶液与过量NaOH溶液反应制Fe(OH)2:Fe2++2OH-===Fe(OH)2↓
B.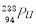 与
与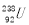 互为同位素
互为同位素
C.H3O+和NH4+具有的电子数相同
D.用BaCl2溶液鉴别AgNO3溶液和K2SO4溶液
查看答案和解析>>
科目: 来源:2016届甘肃省高三上学期第四次月考理综化学试卷(解析版) 题型:填空题
铁及其化合物在日常生活、生产中应用广泛。
(1)高铁酸钠(Na2FeO4)是水处理过程中的一种新型净水剂,工业上利用NaClO 和NaOH的混合溶液将2Fe(OH)3氧化性制备高铁酸钠,反应的化学方程式为 ;高铁酸钠能用作新型净水剂的原理是 ;
(2)氧化铁红颜料跟某些油料混合,可以制成防锈油漆。以黄铁矿为原料制硫酸产生的硫酸渣中含Fe2O3、SiO2、Al2O3、MgO等,用硫酸渣制备铁红(Fe2O3)的过程如下:
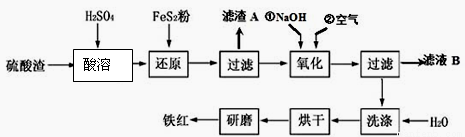
①酸溶过程中发生反应的化学方程式为 , , ;“滤渣A”主要成份的化学式为 。
②还原过程中加入FeS2的目的是将溶液中的Fe3 +还原为Fe2 +,而本身被氧化为H2SO4,请写出该反应的离子方程式 ;
③氧化过程中,O2、NaOH与Fe2+反应的离子方程式为 。
④为了确保铁红的质量和纯度,氧化过程需要调节溶液的pH的范围是 ,
沉淀物 | Fe(OH)3 | Al(OH)3 | Fe(OH)2 | Mg(OH)2 |
开始沉淀pH | 2.7 | 3.8 | 7.6 | 9.4 |
完全沉淀pH | 3.2 | 5.2 | 9.7 | 12.4 |
如果pH过大,可能引起的后果是 。
查看答案和解析>>
科目: 来源:2016届甘肃省高三上学期第四次月考理综化学试卷(解析版) 题型:填空题
【化学一选修3:物质结构与性质】
随原子序数的递增,八种短周期元素(用字母X表示)原子半径的相对大小、最高正价或最低负价的变化如下图所示。
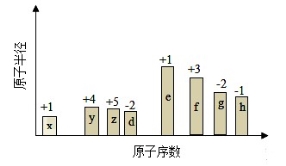
根据判断出的元素回答问题:
(1)f在元素周期表的位置是____。
(2)比较d、e常见离子的半径的小(用化学式表示,下同)_ _>____;比较g、h的最高价氧化物对应的水化物的酸性强弱是:__ _>_ _。
(3)任选上述元素组成一种四原子共价化合物,写出其电子式__________。
(4)已知1mole的单质在足量d2中燃烧,恢复至室温,放出255.5kJ热量,写出该反应的热化学方程式:___________________。
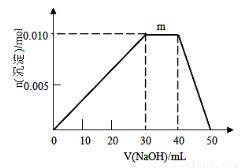
(5)上述元素可组成盐R:zx4f(gd4)2,向盛有10mL1mol·L-1R溶液的烧杯中滴加1mol·L-1NaOH溶液,沉淀物质的量随NaOH溶液体积变化示意图如下:①R离子浓度由大到小的顺序是:______ _。②写出m点反应的离子方程_ 。③若R溶液改加20mL1.2 mol·L-1Ba(OH)2溶液,充分反应后,溶液中产生沉淀的物质的量为__________mol。
查看答案和解析>>
科目: 来源:2015-2016学年吉林省高一上期末(理)化学试卷(解析版) 题型:选择题
实验室保存下列物质的方法中,错误的是
A.氢氧化钠溶液盛装在用橡胶塞的试剂瓶中
B.氢氟酸盛装在细口玻璃瓶中
C.硫酸亚铁溶液存放在加有少量铁粉的试剂瓶中
D.金属钠保存在石蜡油或煤油中
查看答案和解析>>
科目: 来源:2015-2016学年吉林省高一上期末(理)化学试卷(解析版) 题型:选择题
下列反应中既是离子反应,又是氧化还原反应的是
A.Fe + CuSO4 = Cu + FeSO4 B.2Na + Cl2 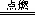 2 NaCl
2 NaCl
C.NaCl + AgNO3 = AgCl↓+ NaNO3 D.2KClO3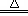 2KCl + 3O2↑
2KCl + 3O2↑
查看答案和解析>>
科目: 来源:2015-2016学年吉林省高一上期末(理)化学试卷(解析版) 题型:选择题
下列离子方程式书写正确的是
A.铝粉投入到NaOH溶液中:2Al+2OH-══ 2AlO2-+H2↑
B.过量Ba(OH)2溶液与少量的NaHCO3溶液混合:Ba2++2OH-+2HCO3-=BaCO3↓+CO32-+2H2O
C.石英溶于NaOH溶液:Si4++2O2-+2OH-=SiO32-+H2O
D.硅酸钠溶液中滴加盐酸:SiO32—+2H+= H2SiO3↓
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com