
科目: 来源:2015-2016学年江西省高一下期中化学试卷(解析版) 题型:选择题
哈伯因发明了由氮气和氢气合成氨气的方法而获得1918年诺贝尔化学奖.现向一密闭容器中充入1mol N2和3mol H2,在一定条件下使该反应发生.下列有关说法正确的是( )
A.达到化学平衡时,N2将完全转化为NH3
B.达到化学平衡时,N2、H2和NH3的物质的量浓度一定相等
C.达到化学平衡时,正反应和逆反应的速率都为零
D.达到化学平衡时,N2、H2和NH3的物质的量浓度不再变化
查看答案和解析>>
科目: 来源:2015-2016学年江西省高一下期中化学试卷(解析版) 题型:选择题
对于反应A2+3B2===2C来说,以下化学反应速率的表示中,反应速率最快的是( )
A.v(B2)=0.8 mol/(L·s) B.v(A2)=0.5 mol/(L·s)
C.v(C)=0.6 mol/(L·s) D.v(B2)=1.2 mol/(L·s)
查看答案和解析>>
科目: 来源:2015-2016学年江西省高一下期中化学试卷(解析版) 题型:填空题
有下列四种微粒:①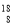 O、②
O、②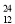 Mg、③2311Na、④
Mg、③2311Na、④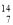 N,
N,
(1)按原子半径由大到小顺序排列的是_____________________(用序号填空)
(2)微粒中质子数小于中子数的是______________________________(用序号填空)
(3)在化合物中呈现的化合价的数值最多的是____________________(用序号填空)
(4)能形成X3Y2型化合物的是___________(用序号填空);
写出形成X2Y2型化合物的电子式_________________。
查看答案和解析>>
科目: 来源:2015-2016学年江西省高一下期中化学试卷(解析版) 题型:填空题
下列反应:
①氢氧化钠与硫酸,②一氧化碳与氧气,③八水合氢氧化钡与氯化铵,④金属铜与硝酸银。
(1)属于复分解反应的放热反应的是____________________________。(用序号填空)
(2)属于吸热反应的是_____________________________________________。(用序号填空)
(3)能设计成原电池的反应是_______________________________________。(用序号填空)
(4)能设计成燃料电池的反应是_____________________________________。(用序号填空)
(5) 写出③发生反应的化学方程式___________________________________。
写出④发生反应的离子方程式___________________________________。
查看答案和解析>>
科目: 来源:2015-2016学年江西省高一下期中化学试卷(解析版) 题型:填空题
意大利科学家使用普通氧分子和带正电的氧离子作用,制出了新型的氧分子O4,它的结构很复杂,可能具有与S4相似的长方形结构,是一种高能量分子。
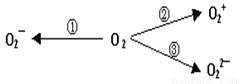
(1)下列有关O4的说法正确的是:
A.O4分子内存在极性共价键
B.合成O4的反应可看作核聚变反应,不属于化学变化
C.O4与O3、O2都是氧的同素异形体
D.O4将来可用作更强有力的火箭推进的氧化剂
(2)制备含O2-、O22-甚至O2+的化合物都是可能的,通常它们是在氧分子进行下列各种反应时生成的:上述变化中, (填序号)相当于氧分子被氧化; _______(填序号)相当于氧分子被还原。
(3)写出O22—的电子式: (4) O2+、O2-中的电子数分别为: ; __。
查看答案和解析>>
科目: 来源:2015-2016学年江西省高一下期中化学试卷(解析版) 题型:填空题
元素在周期表中的位置反映了元素的原子结构和元素的性质。下是元素周期表的一部分。
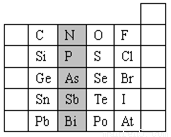
(1)阴影部分元素N在元素周期表中的位置为 。
根据元素周期律,请你预测:H3AsO4、H3PO4 的酸性强弱:H3AsO4 H3PO4。(用“>”、“<”或“=”表示)
(2)元素S的最高正价和最低负价分别为 、 ,在一定条件下,S与H2反应有一定限度(可理解为反应进行的程度),请判断在相同条件下Se与H2反应的限度(选填“更大”、“更小”或“相同”) 。
查看答案和解析>>
科目: 来源:2015-2016学年江西省高一下期中化学试卷(解析版) 题型:填空题
某同学为验证元素周期表中元素性质的递变规律,利用右图装置可验证同主族非金属性的变化规律。设计了如下系列实验。
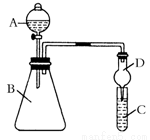
(1)向Na2S溶液中通入氯气出现淡黄色浑浊,可证明Cl的非金属性比S强,反应的离子方程式为____________________________________________。
(2)仪器A的名称为____________________,
(3)若要证明非金属性:Cl>I,则A中加浓盐酸,B中加KMnO4, (KMnO4 与浓盐酸常温下反应生成氯气),C中加淀粉碘化钾混合溶液,观察到混合溶液 的现象,即可证明。从环境保护的观点考虑,此装置缺少尾气处理装置,可用______________ 溶液吸收尾气。
(4)若要证明非金属性:C>Si,则在A中加盐酸、B中加CaCO3,C中加Na2SiO3 溶液观察到C中溶液_____________的现象,即可证明。但有的同学认为盐酸具有挥发性,应用__________溶液除去。
查看答案和解析>>
科目: 来源:2015-2016学年江西省高一下期中化学试卷(解析版) 题型:填空题
由Zn—Cu—硫酸溶液组成的原电池,工作一段时间后,锌片的质量减少了6.5 g。回答下列问题:
(1)上述原电池的正极是:___________,负极的电极反应式:__________________________________。
(2)若将电解质溶液改为硫酸铜溶液,负极是:________,正极的电极反应式:_________________。当电池输出相同的电量时,电池两极的质量差为______________。
查看答案和解析>>
科目: 来源:2015-2016学年湖北省襄阳市高一5月月考化学试卷(解析版) 题型:选择题
W、X、Y、Z是短周期元素,其部分性质如下表:

下列说法不正确的是( )
A.第一电离能:Y>Z
B.离子半径:W>Z
C.X、Y形成的化合物XY4是离子化合物
D.工业上利用电解熔融Z的氧化物生产Z金属单质
查看答案和解析>>
科目: 来源:2015-2016学年湖北省襄阳市高一5月月考化学试卷(解析版) 题型:选择题
下列实验事实:
①常温下S为固体,而Cl2为气体;
②Cl2与H2混合,强光照射剧烈反应,而S与H2反应需较高温度;
③Cl2与Fe反应,Cl2生成FeCl3,而S与Fe生成FeS;
④盐酸是强酸,而氢硫酸是弱酸;
⑤将Cl2通入氢硫酸中可置换出S
能说明Cl的非金属性比S强的事实有()
A.①③⑤ B.②③④ C.②③⑤ D.②③④⑤
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com