
科目: 来源:2016届河北省高三下学期猜题理综化学试卷(解析版) 题型:推断题
甲苯是一种重要的化工原料,可以参与合成很多物质。下图为以甲苯为原料得到药物苯佐卡因的合成路线。

已知:i.苯环上连有甲基时,再引入其他基团主要进入甲基的邻位或对位;苯环上连有羧基时,再引入其他基团主要进入羧基的间位;
Ⅱ.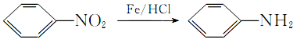 (有弱碱性,易被氧化)。
(有弱碱性,易被氧化)。
请回答下列问题:
(1)化合物C中官能团的结构简式为____________,检验反应③进行程度的试剂有____________。
(2)合成路线中反应类型属于取代反应的有____________个
(3)反应①的化学方程式为____________,该反应要控制好低温条件,否则会生成一种新物质F,该物质是一种烈性炸药,F的名称为____________。
(4)反应⑤的化学方程式为____________。
(5)甲苯的链状且仅含碳碳三键的同分异构体有____________种,其中满足下列条件的同分异构体的结构简式为____________。
①核磁共振氢谱只有两个吸收峰②峰面积之比为1:3
(6)化合物 是一种药物中间体,请写出以甲苯为主要原料制备该中间体的合成路线流程图:
是一种药物中间体,请写出以甲苯为主要原料制备该中间体的合成路线流程图:
提示:①合成过程中无机试剂任选:②合成路线流程图示例如下:

查看答案和解析>>
科目: 来源:2016届湖北省高三5月模拟三理综化学试卷(解析版) 题型:选择题
下列说法中不正确的是
A.无机非金属材料中不可能含有金属元素
B.铝盐、铁盐有净水作用,向浑浊的水中加入少量明矾或硫酸铁溶液,搅拌,过一段时间,水的底部会出现很多絮状不溶物,水变澄清透明
C.氯化物在化学工业领域有重要应用,例如SiCl4、GeCl4、TiCl4分别是制取高纯硅、锗和钛的重要中间物质
D.地球上存在的天然二氧化硅形态有结晶形和无定形两大类统称硅石
查看答案和解析>>
科目: 来源:2016届湖北省高三5月模拟三理综化学试卷(解析版) 题型:选择题
NA表示阿伏加德罗常数的值,下列有关说法正确的是
A.1L1mol/L的甲醇水溶液中含有氢原子总数为4NA
B.50mL18.4mol/L浓硫酸与足量铜微热反应,生成SO2分子的数目为0.46NA
C.反应KIO3+6HI=KI+3H2O+3I2中,生成3molI2转移电子的总数为5NA
D.12g石墨和C60的混合物中质子总数为12NA
查看答案和解析>>
科目: 来源:2016届湖北省高三5月模拟三理综化学试卷(解析版) 题型:选择题
W、X、Y、Z均为短周期主族元素,Y的原子序数是W和Z的原子序数之和的一半,Y原子的最外层电子数与核外电子总数之比为2:7;W和Z形成的可溶性化合物WZ溶于水中不能促进水的电离;W、X、Z三种元素形成的某种化合物能消毒杀菌。下列说法正确的是
A.四种元素原子中,原子半径最大的是Z
B.X、Y形成的化合物能溶于盐酸
C.Z的最高价氧化物对应水化物的酸性强于Y
D.1mol W单质与足量X单质反应,转移的电子数为2NA
查看答案和解析>>
科目: 来源:2016届湖北省高三5月模拟三理综化学试卷(解析版) 题型:选择题
醛或酮与氰化钠、氯化铵反应,生成氨基腈,经水解生成氨基酸盐,是制备氨基酸盐的一种简便方法,反应过程如下:

下列有关该反应说法不合理的是( )
A.反应①是加成反应
B.反应②需要在酸性环境中进行
C.反应②为碱性环境时,产物结构简式是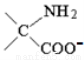
D.经过上述反应,苯乙醛可以制得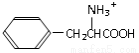
查看答案和解析>>
科目: 来源:2016届湖北省高三5月模拟三理综化学试卷(解析版) 题型:选择题
下列根据实验操作和现象所得出的结论或相应的解释错误的是( )
选项 | 实验操作 | 实验现象 | 结论或解释 |
A | 向盛有0.5mol•L-1 Fe(NO3)2溶液的试管中加入0.5mol•L-1 H2SO4溶液 | 在试管口处出现红棕色气体 | 溶液中NO3-被Fe2+还原为NO2 |
B | 向PbI2饱和溶液中滴加几滴0.1mol•L-1 KI溶液 | 出现黄色沉淀 | 说明 PbI2饱和溶液中有Pb2+存在 |
C | 向白色ZnS沉淀上滴加0.1mol•L-1 CuSO4溶液,振摇 | 沉淀变为黑色 | ZnS沉淀转化为CuS沉淀 ZnS(s)+Cu2+(aq) |
D | 相同条件下,用1mol•L-1醋酸溶液和1mol•L-1盐酸分别做导电性实验 | 醋酸溶液对应的灯泡较暗 | 醋酸是弱电解质 |
查看答案和解析>>
科目: 来源:2016届湖北省高三5月模拟三理综化学试卷(解析版) 题型:选择题
瓦斯爆炸是煤矿开采中的重大危害,一种瓦斯分析仪(图甲)能够在煤矿巷道中的甲烷浓度达到一定浓度时,可以通过传感器显示.该瓦斯分析仪工作原理类似燃料电池的工作原理,其装置如图乙所示,其中的固体电解质是Y2O3-Na2O,O2-可以在其中自由移动.下列有关叙述正确的是

A.瓦斯分析仪工作时,电池内电路中电子由电极b流向电极a
B.电极b是正极,O2-由电极a流向电极b
C.电极a的反应式为:CH4+4O2--8e-=CO2+2H2O
D.当固体电解质中有1mol O2-通过时,电子转移4mol
查看答案和解析>>
科目: 来源:2016届湖北省高三5月模拟三理综化学试卷(解析版) 题型:选择题
利用CO和H2在催化剂的作用下合成甲醇,发生的反应如下:CO(g)+2H2(g) CH3OH(g).在体积一定的密闭容器中按物质的量之比1:2充入CO和H2,测得平衡混合物中CH3OH的体积分数在不同压强下随温度的变化如图所示.下列说法正确的是
CH3OH(g).在体积一定的密闭容器中按物质的量之比1:2充入CO和H2,测得平衡混合物中CH3OH的体积分数在不同压强下随温度的变化如图所示.下列说法正确的是
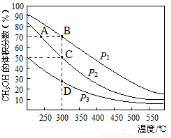
A.该反应的△H<0,且p1<p2
B.反应速率:ν逆(状态A)>ν逆(状态B)
C.在C点时,CO转化率为75%
D.在恒温恒压条件下向密闭容器中充入不同量的CH3OH,达平衡时CH3OH的体积分数也不同
查看答案和解析>>
科目: 来源:2016届湖北省高三5月模拟三理综化学试卷(解析版) 题型:实验题
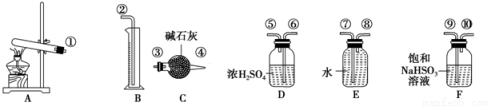
硫酸铜受热分解生成氧化铜和气体,加热温度不同,气体成分也不同.气体成分可能含SO2、SO3和O2中的一种、两种或三种.某化学课外活动小组通过设计探究性实验,测定反应产生的SO2、SO3和O2的物质的量,并计算确定各物质的化学计量数,从而确定CuSO4分解的化学方程式.实验用到的仪器如下图所示:
【提出猜想】
Ⅰ.所得气体的成分可能只含SO3一种;
Ⅱ.所得气体的成分可能含有________两种;
Ⅲ.所得气体的成分可能含有________三种.
【实验探究】
实验操作过程略.
已知实验结束时,硫酸铜完全分解.
(1)请你组装探究实验的装置,按从左至右的方向,各仪器接口的连接顺序为:
①→⑨→⑩→⑥→⑤→________→________→________→________→②(填接口序号).
(2)若实验结束时B中量筒没有收集到水,则证明猜想________正确.
(3)有两个实验小组进行该实验,由于加热时的温度不同,实验结束后测得相关数据也不同,数据如下:
实验小组 | 称取CuSO4的质量/g | 装置C增加的质量/g | 量筒中水的体积折算成标准状况下气体的体积/mL |
一 | 6.4 | 2.56 | 448 |
二 | 6.4 | 2.56 | 224 |
请通过计算,推断出第一小组和第二小组的实验条件下CuSO4分解的化学方程式.
第一小组:______________________________________________;
第二小组:_______________________________________________.
查看答案和解析>>
科目: 来源:2016届湖北省高三5月模拟三理综化学试卷(解析版) 题型:实验题
为回收利用废钒催化剂(含有V2O5、VOSO4及不溶性残渣),科研人员最新研制了一种离子交换法回收钒的新工艺,主要流程如下:
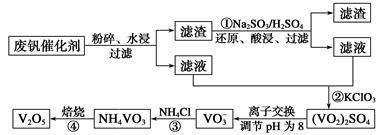
部分含钒物质在水中的溶解性如下:
物质 | VOSO4 | V2O5 | NH4VO3 | (VO2)2SO4 |
溶解性 | 可溶 | 难溶 | 难溶 | 易溶 |
回答下列问题:
(1)工业由V2O5冶炼金属钒常用铝热剂法,写出该反应的化学方程式 .
(2)图中所示滤液中含钒的主要成分为 (写化学式).
有学者建议将滤液进行如下处理后再用KClO3氧化
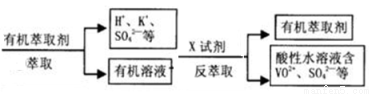
上图中的萃取与反萃取的变化过程可简化为(下式R表示VO2+,HA表示有机萃取剂).
RSO4(水层)+ 2HA(有机层) RA2(有机层)+H2SO4(水层),上图中的X试剂为 _____;这种萃取与反萃取过程有别于用CCl4萃取碘水中的碘,二者的相同点是__________________,不同点是_______________
RA2(有机层)+H2SO4(水层),上图中的X试剂为 _____;这种萃取与反萃取过程有别于用CCl4萃取碘水中的碘,二者的相同点是__________________,不同点是_______________
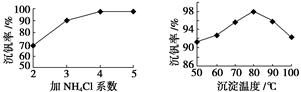
(3)该工艺中反应③的沉淀率(又称沉钒率)是回收钒的关键之一,该步反应的离子方程式_____________ ;沉钒率的高低除受溶液pH影响外,还需要控制氯化铵系数(NH4Cl加入质量与料液中V2O5的质量比)和温度.根据下图判断最佳控制氯化铵系数和温度为 、 .
(4)用硫酸酸化的H2C2O4溶液滴定(VO2)2SO4溶液,以测定反应②后溶液中含钒量,完成反应的离子方程式为□VO2++□H2C2O4+□_____=□VO2++□CO2↑+□H2O.
(5)全矾液流电池的电解质溶液为VOSO4溶液,电池的工作原理为:
VO2++V2++2H+  VO2++H2O+V3+
VO2++H2O+V3+
电池充电时阳极的电极反应式为__________________.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com