
科目: 来源:2016届黑龙江省高三考前训练一理综化学试卷(解析版) 题型:选择题
下列说法正确的是( )
A.按系统命名法,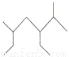 的名称为2-甲基-3,5-二乙基己烷
的名称为2-甲基-3,5-二乙基己烷
B.用Na2CO3溶液能区分CH3COOH、CH3CH2OH、苯和硝基苯四种物质
C.等质量的甲烷、乙烯、1,3一丁二烯分别充分燃烧,所消耗氧气的量依次增加
D.葡萄糖、蔗糖、油脂和蛋白质在一定条件下都能水解
查看答案和解析>>
科目: 来源:2016届黑龙江省高三考前训练一理综化学试卷(解析版) 题型:选择题
室温下,关于下列溶液的说法正确的是( )

A.25℃时①10﹣3mol/L的盐酸;②pH=3的NH4Cl溶液;③pH=11的氨水中,水的电离程度为:②>③>①
B.pH=1的NaHSO4溶液:c(H+)=c(SO42-)+c(OH-)
C.pH=8.0的KHS溶液中,c(K+)>c(HS﹣)>c(OH﹣)>c(S2﹣)>c(H+)
D.图中a点溶液中各离子浓度的关系是:c(OH﹣)=c(H+)+c(CH3COO﹣)+c(CH3COOH)
查看答案和解析>>
科目: 来源:2016届黑龙江省高三考前训练一理综化学试卷(解析版) 题型:选择题
有关下图及实验的描述正确的是( )
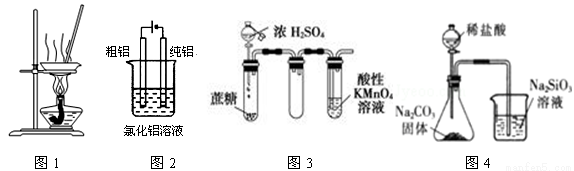
A.用图1装置蒸发FeCl3溶液制备无水FeCl3
B.用图2装置精炼铝
C.用图3装置证明浓硫酸具有脱水性和强氧化性
D.用图4装置可比较氯、碳、硅三种元素的非金属性强弱
查看答案和解析>>
科目: 来源:2016届黑龙江省高三考前训练一理综化学试卷(解析版) 题型:选择题
短周期主族元素X﹑Y﹑Z﹑W﹑Q的原子序数逐渐增大,X原子核外最外层电子数是次外层电子数的2倍,Y的氟化物YF3分子中各原子均达到8电子稳定结构,Z﹑W是常见金属,Z是同周期中原子半径最大的元素,W的简单离子是同周期中离子半径最小的,X和Z原子序数之和与Q的原子序数相等。下列说法正确的是( )
A.相同质量的Z和W单质分别与足量稀盐酸反应时,Z的单质获得的氢气多
B.气态氢化物的稳定性:X>Y>Q
C.Z﹑W﹑Q三种元素最高价氧化物对应的水化物之间两两均可反应生成盐和水
D.X与Q形成的化合物和Z与Q形成的化合物的化学键类型相同
查看答案和解析>>
科目: 来源:2016届黑龙江省高三考前训练一理综化学试卷(解析版) 题型:填空题
第21届联合国气候大会于2015年11月30日在巴黎召开,会议的主题是减少温室气体排放量。
Ⅰ.CO2 加氢合成甲醇是合理利用 CO2 的有效途径。由 CO2 制备甲醇过程可能涉及反应如下:
反应①:CO2(g)+3H2(g)  CH3OH(g)+H2O(g)△H1=﹣49.58kJ•mol﹣1
CH3OH(g)+H2O(g)△H1=﹣49.58kJ•mol﹣1
反应②:CO2(g)+H2(g)  CO (g)+H2O(g)△H2
CO (g)+H2O(g)△H2
反应③:CO(g)+2H2(g)  CH3OH(g)△H3=﹣90.77kJ•mol﹣1,回答下列问题:
CH3OH(g)△H3=﹣90.77kJ•mol﹣1,回答下列问题:
(1)反应②的△H2= ,反应 ① 自发进行条件是 (填“较低温”、“较高温”或“任何温度”)。
(2)某温度下,在体积为2 L的恒容密闭容器中,按如下方式加入反应物,仅发生反应①。一段时间后达到平衡。
容器 | 甲 | 乙 |
反应物投入量 | 2mol CO2、6mol H2 | a mol CO2、b mol H2 c mol CH3OH(g)、c mol H2O(g) |
测得甲中CO2和CH3OH(g)的浓度随时间变化如图所示。
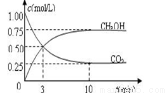
①前3min内,平均反应速率v(H2)= mol·L-1·min-1。此温度下该反应的平衡常数为
(结果保留两位小数) 。
②下列措施中,既能使反应速率加快,又能使n(CH3OH)/n(CO2)增大是 。
A.升高温度 B.充入惰性气体
C.将H2O(g)从体系中分离 D.再充入1mol H2
E.再充入1 mol CO2 F.加入催化剂
③反应达到平衡后,若向反应体系再加入CO2(g)、H2(g) 、CH3OH(g)、H2O(g)各1mol,化学平衡
(填“正向”、“逆向”或“不”)移动。
④要使平衡后乙与甲中相同组分的体积分数相等,且起始时维持化学反应向逆反应方向进行,则c的取值范围为 。
Ⅱ.工业上可用CO2与NH3合成制尿素的原料氨基甲酸铵(H2NCOONH4)。氨基甲酸铵极易发生:H2NCOONH4+2H2O  NH4HCO3+NH3·H2O,该反应酸性条件下更彻底。25℃,向l L 0.1 mol·L-1的盐酸中逐渐加入氨基甲酸铵粉末至溶液呈中性(忽略溶液体积变化),共用去0.052 mol氨基甲酸铵。若此时溶液中几乎不含碳元素,则该溶液中 c(NH4+)=____________,NH4+水解常数Kh=________。
NH4HCO3+NH3·H2O,该反应酸性条件下更彻底。25℃,向l L 0.1 mol·L-1的盐酸中逐渐加入氨基甲酸铵粉末至溶液呈中性(忽略溶液体积变化),共用去0.052 mol氨基甲酸铵。若此时溶液中几乎不含碳元素,则该溶液中 c(NH4+)=____________,NH4+水解常数Kh=________。
查看答案和解析>>
科目: 来源:2016届黑龙江省高三考前训练一理综化学试卷(解析版) 题型:填空题
醋酸亚铬水合物[Cr(CH3COO)2]2·2H2O(相对分子质量为376)是一种深红色晶体。不溶于冷水,微溶于乙醇,不溶于乙醚(易挥发的有机溶剂)是常用的氧气吸收剂。实验室中以锌粒、三氯化铬溶液、醋酸钠溶液和盐酸为主要原料制备醋酸亚铬水合物,其装置如右图所示,且仪器2中预先加入锌粒。已知二价铬不稳定,极易被氧气氧化,不与锌反应。制备过程中发生的相关反应如下:
Zn(s)+ 2HCl(aq)= ZnCl2(aq)+ H2(g)
2CrCl3(aq)+ Zn(s) = 2CrCl2(aq)+ ZnCl2(aq)
2Cr2+(aq)+ 4CH3COO-(aq)+ 2H2O(l)= [Cr(CH3COO)2]2·2H2O(s)
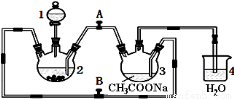
请回答下列问题:
(1)仪器1的名称是 。
(2)往仪器2中加盐酸和三氯化铬溶液的顺序最好是 (选下面的A、B或C);目的是 。
A.盐酸和三氯化铬溶液同时加入
B.先加三氯化铬溶液一段时间后再加盐酸
C.先加盐酸一段时间后再加三氯化铬溶液
(3)为使生成的CrCl2溶液与CH3COONa溶液顺利混合,应关闭阀门 (填“A”或“B”,下同),打开阀门 。
(4)当仪器3中出现大量深红色晶体时,关闭分液漏斗的旋塞。将装置3中混合物快速过滤、洗涤和干燥。洗涤产品时,为了去除可溶性杂质和水分,下列试剂的正确使用顺序是 (填标号)。
a.乙醚 b.去氧、冷的蒸馏水 c.无水乙醇
(5)已知其它反应物足量,实验时取用的CrCl3溶液中含溶质9.51g,取用的醋酸钠溶液为1.5L0.1mol/L;实验后得干燥纯净的[Cr(CH3COO)2]2·2H2O 9.4g,则该实验所得产品的产率为
(不考虑溶解的醋酸亚铬水合物)。
(6)铬的离子会污染水,常温下要除去上述实验中多余的Cr2+,最好往废液中通入足量的 ,再加入碱液,调节pH至少为 才能使铬的离子沉淀完全(铬的离子浓度应小于10-5mol/L)。
【已知Cr(OH)3的溶度积为6.3×10-31 ,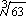 ≈4,lg2≈0.3】
≈4,lg2≈0.3】
查看答案和解析>>
科目: 来源:2016届黑龙江省高三考前训练一理综化学试卷(解析版) 题型:实验题
废弃物的综合利用既有利于节约资源,又有利于保护环境。工业上利用铅浮渣(主要成分是PbO、Pb还含有少量的Ag、CaO)可制备硫酸铅。制备流程图如下:

下表是25℃ 时某些盐的浓度积常数:
化学式 | CaSO4 | Ag2SO4 | PbSO4 |
Ksp | 4.9×10-5 | 1.2×10-5 | 1.6×10-8 |
(1)实验室用75%的硝酸来配制15%的硝酸溶液,不需用到的玻璃仪器有 (填标号)。
A.烧杯 B.量筒 C.容量瓶 D.锥形瓶 E.玻璃棒
(2)步骤I有NO产生,浸出液中含量最多的金属阳离子为 Pb2+,写出Pb参加反应的化学方程式 ,为防止Ag被溶解进入溶液,步骤I操作时应注意 。
(3)母液可循环利用于步骤I,其溶质主要是 (填一种物质化学式),若母液中残留的 SO42-过多,循环利用时可能出现的问题是 。
(4)粗PbSO4 产品含有的杂质是____________,需用 溶液多次洗涤,以得到纯净的PbSO4。
(5)铅蓄电池放电时正极的电极反应式为 。如果用铅蓄电池做电源电解饱和食盐水制取Cl2,已知某铅蓄电池中硫酸溶液的体积为0.80 L,电解前硫酸溶液浓度为4.50 mol·L-1,当制得4.48 LCl2时(在标准状况下),求理论上电解后电池中硫酸溶液的浓度为(假设电解前后硫酸溶液的体积不变)_________ mol·L-1。
查看答案和解析>>
科目: 来源:2016届黑龙江省高三考前训练一理综化学试卷(解析版) 题型:实验题
姜黄素具有搞突变和预防肿瘤的作用,其合成路线如下:
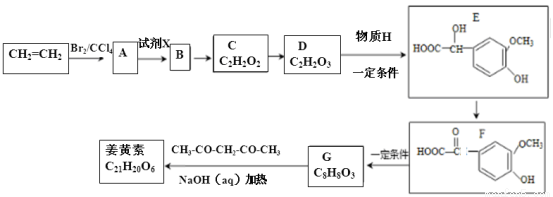
已知:①
②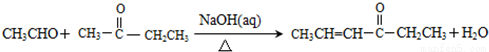
请回答下列问题:
(1)D中含有的官能团名称是 。
(2)反应A→B的反应条件为 ;已知D→E转化中原子利用率100%,则H的结构简式为 。
(3)姜黄素的结构简式为 。
(4)D的催化氧化产物与B可以反应生成一种高分子化合物,其化学方程式为 。
(5)下列有关E的叙述不正确的是 (填正确答案编号)。
a.1molE与浓溴水反应最多消耗3mol的Br2
b.E能发生氧化、加成、取代和缩聚反应
c.1molE最多能与3molNaOH发生反应
d. E能与FeCl3溶液发生显色反应
(6)G(C8H8O3)的同分异构体中,符合下列条件的共有 种。
①苯环上的一取代物只有2种;②1mol该物质与烧碱溶液反应,最多消耗3molNaOH.
其中核磁共振氢谱中有4组吸收峰的同分异构体的结构简式为 。
查看答案和解析>>
科目: 来源:2016届黑龙江省高三第三次模拟理综化学试卷(解析版) 题型:选择题
化学与生产、生活和社会可持续发展密切相关,下列有关叙述正确的是( )
A.在食品袋中放入装有硅胶、生石灰的透气小袋,可防止食物受潮、氧化变质
B.天然气、酒精和汽油分别属于化石能源、不可再生能源和二次能源
C.夏天雷雨过后会使人感觉空气清新,这是因为空气中产生了少量的二氧化氮
D.酸雨样品露天放置一段时间pH减小,是由于酸雨所含成分被氧化的原因
查看答案和解析>>
科目: 来源:2016届黑龙江省高三第三次模拟理综化学试卷(解析版) 题型:选择题
下列叙述正确的是( )
A.测定相同温度下盐酸和醋酸溶液的pH,可证明盐酸是强酸、醋酸是弱酸
B.改变温度能改变任何可逆反应的平衡状态
C.离子反应的结果是自由移动的离子浓度减小
D.Fe(OH)3胶体和饱和FeCl3溶液都呈红褐色,可通过丁达尔效应区分二
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com