
科目: 来源:2016-2017学年湖北沙市高二上第一次双周练化学卷(解析版) 题型:实验题
己知:KI溶液在酸性条件下能被空气中的O2氧化。
(1)写出发生反应的离子方程式_______________________。
(2)某化学小组为探究不同条件对上述反应速率的影响,设计如下实验,完成下表中①和②的内容。
(限选试剂:0.1 L mol/L硫酸、0.2 mol/L硫酸、1 mol/L KOH溶液、淀粉溶液)
组别 | 温度 | KI溶液 | H2SO4溶液 | 淀粉溶液 | 实验目的 | ||
c(KI) | Υ | c(H2SO4) | Υ | ||||
1 | 298K | 1 mol/L | 5 mL | 0.1mol/L | 5 mL | 3滴 | l组和2组探究②__________对该反应速率的影响;1组和3组探究反应物浓度对该反应速率的影响 |
2 | 308K | 1 mol/L | 5 mL | 0.1mol/L | 5 mL | 3滴 | |
3 | 298K | 1 mol/L | 5 mL | ①___________ | 5 mL | 3滴 | |
(3)在上述实验中,三种溶液混合的顺序最合理的是_______(选填下列选项);应记录的是_________所需的时间。
A.先将硫酸溶液与淀粉溶液混合,然后再加入KI溶液
B.先将KI溶液与硫酸溶液混合,然后再加 入淀粉溶液
入淀粉溶液
C.先将KI溶液与淀粉溶液混合,然后再加入硫酸溶液
查看答案和解析>>
科目: 来源:2016-2017学年湖北沙市高二上第一次双周练化学卷(解析版) 题型:实验题
KMnO4在实验室和工业生产中有广泛用途。
Ⅰ.某小组拟用酸性KMnO4溶液与H2C2O4溶液(弱酸)的反应(此反应为放热反应)来探究“条件对化学反应速率的影响”,并设计了如下的方案记录实验结果(忽略溶液混合体积变化)。限选试剂和仪器:0.20 mol/L H2C2O4溶液、0.010 mol/L KMnO4溶液(酸性)、蒸馏水、试管、量筒、秒表、恒温水浴槽。(已知:2KMnO4+5H2C2O4+3H2SO4=K2SO4+2MnSO4+10CO2↑+8H2O)
物理量 编号 | V(0.20 mol/L H2C2O4溶液)/mL | V(蒸馏水)/mL | V(0.010 mol/L KMnO4溶液) | m(MnSO4固体)/g | T/℃ | 乙 |
① | 2.0 | 0 | 4.0 | 0 | 50 | |
② | 2.0 | 0 | 4.0 | 0 | 25 | |
③ | 1.0 | a | 4.0 | 0 | 25 | |
④ | 2.0 | 0 | 4.0 | 0.1 | 25 |
回答下列问题:
(1)完成上述反应原理的离子反应方程式_______________________。
(2)上述实验①②是探究____________对化学反应速率的影响;若上述实验②③是探究浓度对化学反应速率的影响,则a为___________;乙是实验需要测量的物理量,则表格中“乙”应填写___________;上述实验②④是探究_________对化学反应速率的影响。

Ⅱ.某化学小组利用如图装置进行实验证明氧化性:KMnO4>Cl2>Br2。限选试剂:KBr溶液、KMnO4、浓盐酸、浓硫酸。
(3)装置d中观察到的现象为____________________;此实验装置的不足之处是无尾气吸收装置,请写出处理尾气的离子方程式_____________________。
查看答案和解析>>
科目: 来源:2016-2017学年湖北沙市高二上第一次双周练化学卷(解析版) 题型:填空题
回答下列问题:
(1)已知下列反应:SO2 (g)+2OH–(aq) =SO32–(aq)+H2O(l) ΔH1;
ClO–(aq)+SO32–(aq)=SO42–(aq)+Cl–(aq) ΔH2;
CaSO4(s)=Ca2+(aq)+SO42–(aq) ΔH3。
则反应SO2(g)+Ca2+(aq)+ClO–(aq)+2OH–(aq)=CaSO4(s)+H2O(l)+Cl–(aq)的ΔH=______________。(用ΔH1、ΔH2、ΔH3表示)
(2)合成气(CO和H2为主的混合气体)不但是重要的燃料也是重要的化工原料,制备合成气的方法有多种,用甲烷制备合成气的反应为:①2CH4(g)+O2(g)=2CO(g)+4H2(g) ΔH1=-72 kJ·mol﹣1;
②CH4(g)+H2O(g)=CO(g)+3H2(g) ΔH2=+216 kJ·mol﹣1。现 有1 mol由H2O(g)与O2组成的混合气,且O2的体积分数为x,将此混合气与足量CH4充分反应。
有1 mol由H2O(g)与O2组成的混合气,且O2的体积分数为x,将此混合气与足量CH4充分反应。
若x=0.2时,反应①放出的能量为________kJ;
若x=_________时,反应①与②放出(或吸收)的总能量为0。
(3)一定条件,在水溶液中1 mol Cl-和1 mol ClOx(x=1,2,3,4)的能量(kJ)相对大小如图所示。

①D是________(填离子符号)。
②B→A+C反应的热化学方程式为_______________(用离子符号表示)。
查看答案和解析>>
科目: 来源:2016-2017学年湖北沙市高二上第一次双周练化学卷(解析版) 题型:推断题
X、Y、Z 为不同短周期非金属元素的气态单质。在一定条件下能发生如下反应:
Y+X→甲(g),Y+Z→乙(g)。甲为10电子分子,Z为黄绿色气体。甲、乙可化合生成离子化合物。
(1)X 的电子式是______________。
(2)写出Y+X→甲(g)的化学方程式_____________________。
(3)向一定浓度的 BaCl2溶液中通入 SO2气体,未见沉淀生成,若在通入 SO2气体的同时加入或通入某纯净物(从X、Y、Z、甲、乙中选择),即可生成白色沉淀,该纯净物的化学式为________,生成的白色沉淀的化学式为___________。

(4)已知常温下,PCl3为液体,PCl5为固体。白磷(P4)在Z气体中燃烧生成液态丙分子,白磷固体和 Z 气体反应,生成1 mol液态丙时,能量变化如图所示,写出该反应的热化学方程式_______________。
已知1 mol白磷固体和Z气体反应,生成固态丁时,放热b kJ,则1 mol固态丁转化为液态丙时的反应热ΔH=_____________。
查看答案和解析>>
科目: 来源:2016-2017学年湖北沙市高二上第一次双周练化学卷(解析版) 题型:填空题
氢、氧两种元素组成的常见物质有H2O和H2O2,二者在一定条件下均可分解。
(1)已知:
化学键 | 断开1mol化学键所需的能量(kJ) |
H-H | 436 |
O-H | 463 |
O=O | 498 |
①H2O的电子式是________________。
②H2O(g)分解的热化学方程式是________________________。
③11.2 L(标准状况)的H2完全燃烧,生成气态水,放出__________kJ的热量。
(2)某同学以H2O2分解为例,探究浓度与溶液酸碱性对反应速率的影响。常温下,按照如表所示的方案完成实验。
实验编号 | 反应物 | 催化剂 | |
a | 50 mL5%H2O2溶液 | 1 mL0.1 mol·L-1FeCl3溶液 | |
b | 50 mL5%H2O2溶液 | 少量浓盐酸 | 1 mL0.1 mol·L-1FeCl3溶液 |
c | 50 mL5%H2O2溶液 | 少量浓NaOH溶液 | 1 mL 0.1 mol·L-1FeCl3溶液 |
d | 50 mL5%H2O2溶液 | MnO2 | |
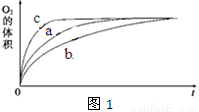
① 测得实验a、b、c中生成氧气的体积随时间变化的关系如图1所示。由该图能够得出的实验结论是______________________。
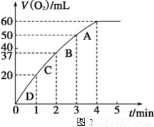
② 测得实验d在标准状况下放出氧气的体积随时间变化的关系如图2所示。解释反应速率变化的原因________________;计算H2O2的初始物质的量浓度为________________ (保留两位有效数字)。
查看答案和解析>>
科目: 来源:2016-2017学年湖北沙市高二上第一次双周练化学卷(解析版) 题型:填空题
2SO2(g)+O2(g) 2SO3(g),反应过程的能量变化如图所示。已知1 mol SO2(g)氧化为1 mol SO3(g)的ΔH=-99 kJ/mol。请回答下列问题:
2SO3(g),反应过程的能量变化如图所示。已知1 mol SO2(g)氧化为1 mol SO3(g)的ΔH=-99 kJ/mol。请回答下列问题:

(1)E的大小对该反应的反应热________影响?(填“有或无”)。该反应通常用V2O5作催化剂,加V2O5会使图中B点______(填“升高或降低”);
(2)图中ΔH=__________kJ/mol;
(3)如果反应速率υ(SO2)为0.05 mol/(L·min),则υ(O2)=___________mol/(L·min);
(4)1 mol SO2(g)氧化为1 mol SO3(g)的反应热ΔH1___________1 mol SO2(g)氧化为1 mol SO3(l)的反应热ΔH2。(填“>、<或=”)
(5)已知单质硫的燃烧热为296 kJ/mol,计算由S(s)生成3 mol SO3(g)的ΔH=____________。
查看答案和解析>>
科目: 来源:2016-2017学年湖北沙市高一上第一次双周练化学卷(解析版) 题型:选择题
关于摩尔的说法是正确的是( )
A.摩尔是表示物质数量的单位
B.摩尔是表示物质多少的单位
C.摩尔是既表示物质所含粒子数的数量,又能表示物质的质量具有双重意义的单位
D.摩尔是巨大数目的粒子集合体,表示物质的量的国际单位
查看答案和解析>>
科目: 来源:2016-2017学年湖北沙市高一上第一次双周练化学卷(解析版) 题型:选择题
①烧杯 ②坩埚 ③蒸发皿 ④试管 ⑤蒸馏烧瓶 ⑥锥形瓶 ⑦燃烧匙
A. ③⑥⑦ B. ①⑤⑥ C. ①⑤ D. ⑤⑥⑦
查看答案和解析>>
科目: 来源:2016-2017学年湖北沙市高一上第一次双周练化学卷(解析版) 题型:选择题
下列叙述正确的是
A.1 mol H2O的质量为18g/mol
B.3.01×1023个SO2分子的质量为32g
C.CH4的摩尔质量为16g
D.标准状况下,1 mol任何物质体积均为22.4L
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com