
科目: 来源:2017届江西省等六校高三上学期第一次联考化学试卷(解析版) 题型:选择题
根据下列实验现象,所得结论正确的是( )
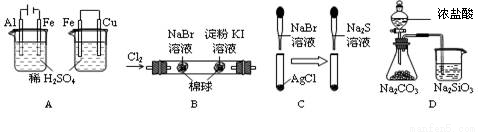
实验 | 实验现象 | 结论 |
A | 左烧杯中铁表面有气泡,右边铜表面有气泡 | 活动性:Al>Fe>Cu |
B | 左边棉花变为橙色,右边棉花变为蓝色 | 还原性:Cl-<Br-<I- |
C | 白色固体先变为淡黄色,后变为黑色 | 溶解性AgCl<AgBr<Ag2S |
D | 锥形瓶中有气体产生,烧杯中液体变浑浊 | 不能说明非金属性:Cl>C>Si |
查看答案和解析>>
科目: 来源:2017届江西省等六校高三上学期第一次联考化学试卷(解析版) 题型:选择题
几种短周期元素的原子半径及主要化合价如下表:

下列叙述不正确的是( )
A. 一定条件下,Z单质与W的常见单质直接生成ZW
B. X最高价氧化物对应的水化物与Y的最高价氧化物对应的水化物能反应
C. Y的最高价氧化物对应的水化物不能溶于稀氨水
D. 一定条件下,w单质可以将z单质从其氢化物中置换出来
查看答案和解析>>
科目: 来源:2017届江西省等六校高三上学期第一次联考化学试卷(解析版) 题型:选择题
向100 mL0.04 mol / L的Ca(OH)2溶液中通入CO2气体,当得到0.1g沉淀时,通入CO2的物质的量是:( )
A.0.014 mol B.0.01 mol C.0.007 mol D.0.005 mol
查看答案和解析>>
科目: 来源:2017届江西省等六校高三上学期第一次联考化学试卷(解析版) 题型:选择题
某温度下,将Cl2通入NaOH溶液中,反应得到NaCl、NaClO、NaClO3的混合液,经测定ClO—与ClO3—的浓度之比为1︰5,则Cl2与NaOH溶液反应时被氧化的氯原子与被还原的氯原子的物质的量之比为( )
A.1︰1 B.5︰1 C.3︰13 D.4︰15
查看答案和解析>>
科目: 来源:2017届江西省等六校高三上学期第一次联考化学试卷(解析版) 题型:选择题
某不纯的烧碱样品,含Na2CO3 1.06%(质量百分含量)、H2O 3.6%、NaOH 95.34%, 。取m g样品溶于2 mol/L盐酸40 mL得溶液A(假设生成的气体全部逸出),用20mL2 mol/L NaOH溶液恰好中和剩余的酸,则A溶液中含溶质氯化钠的质量为 ( )
A.4.68 g B.6..68 g
C.2.34 g D.由于m未知,无法计算
查看答案和解析>>
科目: 来源:2017届江西省等六校高三上学期第一次联考化学试卷(解析版) 题型:选择题
在右图中A,B,C,D,4条线表示Na,Mg,Al,Fe,4种金属和定量的Cl2反应时消耗金属的质量(用纵坐标表示)和消耗Cl2的质量(用横坐标表示)之间的关系,其中表示Fe和Cl2反应的是 ( )

查看答案和解析>>
科目: 来源:2017届江西省等六校高三上学期第一次联考化学试卷(解析版) 题型:选择题
甲、乙、丙、丁四种易溶于水的物质,分别由NH4+、Ba2+、Mg2+、H+、OH-、Cl-、HCO3-、SO42-中的不同阳离子和阴离子各一种组成。已知:①将甲溶液分别与其它三种物质的溶液混合,均有白色沉淀生成;② 0.1mol/L乙溶液中c(H+)>0.1mol/L;③ 向丙溶液中滴入AgNO3溶液有不溶于稀HNO3的白色沉淀生成。下列结论正确的是( )
A.甲为氯化钡 B.乙溶液含有Cl-
C.丙溶液含有 SO42- D.丁溶液含有NH4+
查看答案和解析>>
科目: 来源:2017届江西省等六校高三上学期第一次联考化学试卷(解析版) 题型:选择题
在1200℃时,天然气脱硫工艺中会发生下列反应
H2S(g)+  O2(g)=SO2(g)+H2O(g) △H1
O2(g)=SO2(g)+H2O(g) △H1
2H2S(g)+SO2(g)= S2(g)+2H2O (g) △H2
S2(g)+2H2O (g) △H2
H2S(g)+ O2(g)=S(g)+H2O(g) △H3
O2(g)=S(g)+H2O(g) △H3
2S(g) =S2(g) △H4
则△H4的正确表达式为 ( )
A. △H4= (△H1+△H2+3△H3 )
(△H1+△H2+3△H3 )
B.△H4= (3△H3-△H1-△H2)
(3△H3-△H1-△H2)
C.△H4= (△H1+△H2-3△H3)
(△H1+△H2-3△H3)
D.△H4= (△H1-△H2-3△H3)
(△H1-△H2-3△H3)
查看答案和解析>>
科目: 来源:2017届江西省等六校高三上学期第一次联考化学试卷(解析版) 题型:填空题
⑴已知碳酸二级电离较偏铝酸的电离容易,而石炭酸的电离介于碳酸的一级电离与二级电离之间。下面的推论正确的是_________________:
①将CO2通入偏铝酸钠溶液中,溶液变浑浊,并生成碳酸钠或碳酸氢钠;②将CO2通入C6H5ONa溶液中,离子反应式为CO2+H2O+2C6H5O— 2 C6H5OH+CO32—;
2 C6H5OH+CO32—;
③HCO3—在溶液中既能与AlO2—又能与Al3+反应,且都发生双水解;④往含有大量CO32—的溶液中加入C6H5OH得到澄清溶液,放出CO2气体;⑤向Al(OH)3的混浊液中加入Na2CO3溶液得不到澄清溶液;⑥相同温度,相同浓度的Na2CO3、C6H5ONa、NaHCO3、NaAlO2的稀溶液PH依次增大。
(2)浅绿色的Fe(NO3)2溶液中,存在如下平衡:Fe2++2H2O Fe(OH) 2+2H+若在此溶液中加入盐酸后,用文字说明溶液颜色的变化及原因__________________.
Fe(OH) 2+2H+若在此溶液中加入盐酸后,用文字说明溶液颜色的变化及原因__________________.
⑶一个完整的氧化还原反应方程式可以拆开,写成两个“半反应式”,一个是“氧化反应式”,一个是“还原反应式”。如2Fe3++Cu=2Fe2++Cu2+,可拆写为氧化反应式:Cu-2e-=Cu2+,还原反应式:2Fe3++2e-=2Fe2+。据此,回答下列问题:
①将反应3 Cu+8H+ +2NO3-=3Cu2++2NO↑+4H2O拆写为两个“半反应式”:
还原反应式: 。
②已知某反应的两个“半反应式”为:
CH4+10 OH--8e-=CO32-+7H2O, O2+2H2O+4e-= 4OH-,
则氧化还原反应方程式为 。
③此原理可用于电化学。锌—锰碱性电池广泛应用于日常生活。电池的总反应式为Zn(s)+2MnO2(s)+2H2O(l)===Zn(OH)2(s)+2MnOOH(s)。
该电池的正极反应式为 。
查看答案和解析>>
科目: 来源:2017届江西省等六校高三上学期第一次联考化学试卷(解析版) 题型:推断题
下图中,A、C是工业上用途很广的两种重要化工原料,B为日常生活中常见的金属,H、G是正四面体结构的非极性分子,H是一种重要的能源,J是一种耐高温材料,K是由两种常见元素组成的化合物(图中部分反应物或生成物没有列出)。
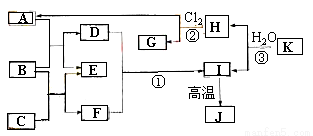
请按要求回答下列问题:
⑴写出B元素在周期表中的位置 K的化学式______________ 。
⑵反应①的离子方程式为_______________ 。
⑶将D的溶液蒸干且将所得的固体物质灼烧得到___________固体(写化学式),若要由D得溶液得到无水的D的固体,请简述其处理方法______________
⑷反应②进行的条件通常是 ,H和Cl2反应产物中有一种产物M的结构能证明G一定为正四面体结构请写出M的电子式 。
⑸J与焦炭在高温的情况下可以生成K和二氧化碳,请写出该反应的方程式____________ ;在此反应中氧化剂与还原剂的质量之比为____________
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com