
科目: 来源:2017届江苏省苏州市高三上学期期初调研化学试卷(解析版) 题型:选择题
阿克拉酮是合成某种抗癌药的重要中间体,其结构如图所示。下列关于阿克拉酮的性质的描述,正确的是
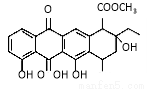
A.阿克拉酮的分子式为C22H22O8
B.分子中含有4个手性碳原子
C.该分子一定条件下能发生取代、氧化、消去反应
D.1 mol该物质最多可与3 mol NaOH反应
查看答案和解析>>
科目: 来源:2017届江苏省苏州市高三上学期期初调研化学试卷(解析版) 题型:选择题
常温下,下列各组离子在指定溶液中一定能大量共存的是
A.在0.01 mol·L-1Ba(OH)2溶液中:Al3+、NH4+ 、NO、HCO
B.0.1 mol/L的FeCl2溶液中:H+、Al3+、SO42-、ClO-
C.滴加KSCN溶液显红色的溶液:NH4+、K+、Cl-、I-
D.由水电离产生的c(H+)=1×10-13mol·L-1的溶液中:Na+、Ba2+、NO、Cl-
查看答案和解析>>
科目: 来源:2017届江苏省苏州市高三上学期期初调研化学试卷(解析版) 题型:选择题
下列根据实验操作和现象所得到的结论正确的是
选项 | 实验操作和现象 | 结论 |
A | 向浓度均为0.1 mol·L-1的NaCl和NaI混合溶液中滴加少量AgNO3溶液,先出现黄色沉淀 | Ksp(AgCl)<Ksp(AgI) |
B | 向苯酚浊液中加入Na2CO3溶液,溶液变澄清 | 酸性:苯酚> HCO3— |
C | 向蓝色石蕊试纸上滴加新制氯水,试纸边缘呈红色、中间为白色 | 氯水既有酸性又有还原性 |
D | 淀粉与稀硫酸混和一段时间后,滴加银氨溶液并水浴加热,无银镜出现 | 淀粉没有水解 |
查看答案和解析>>
科目: 来源:2017届江苏省苏州市高三上学期期初调研化学试卷(解析版) 题型:选择题
25℃时,下列有关溶液中微粒的物质的量浓度关系正确的是
A.0.1 mol·L-1 (NH4)2Fe(SO4)2溶液中:c(SO42-)>c(NH4+)>c(Fe2+)>c(H+)
B.pH=11的氨水和pH=3的盐酸溶液等体积混合,所得溶液中:
c(Cl-)>c(NH4+)>c(OH-)>c(H+)
C.在0.1 mol·L-1 Na2CO3溶液中:2c(Na+)=c(CO)+c(HCO)+c(H2CO3)
D.0.1 mol·L-1的醋酸钠溶液20 mL与0.1 mol·L-1盐酸10 mL混合后溶液显酸性:
c(CH3COO-)>c(Cl-)>c(CH3COOH)>c(H+)
查看答案和解析>>
科目: 来源:2017届江苏省苏州市高三上学期期初调研化学试卷(解析版) 题型:选择题
一定温度下,在三个体积均为2.0 L的恒容密闭容器中发生如下反应:PCl5(g) PCl3(g)+Cl2(g)
PCl3(g)+Cl2(g)
编号 | 温度(℃) | 起始物质的量 (mol) | 平衡物质的量 (mol) | 达到平衡所需时间 (s) | |
PCl5(g) | PCl3(g) | Cl2(g) | |||
Ⅰ | 320 | 0.40 | 0.10 | 0.10 | t1 |
Ⅱ | 320 | 0.80 | t2 | ||
Ⅲ | 410 | 0.40 | 0.15 | 0.15 | t3 |
下列说法正确的是
A.平衡常数K:容器Ⅱ>容器Ⅲ
B.反应到达平衡时,PCl5的转化率:容器Ⅱ<容器Ⅰ
C.反应到达平衡时,容器I中的平均速率为v(PCl5)=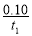 mol·L-1·s-1
mol·L-1·s-1
D.起始时向容器Ⅲ中充入PCl5 0.30 mol、PCl3 0.45 mol和Cl2 0.10 mol,则反应将向逆反应方向进行
查看答案和解析>>
科目: 来源:2017届江苏省苏州市高三上学期期初调研化学试卷(解析版) 题型:实验题
粉煤灰是燃煤电厂的废渣,主要成分为SiO2、Al2O3、Fe2O3和C等。实验室模拟工业从粉煤灰提取活性Al2O3,其流程如下图:

已知烧结过程的产物主要是:NaAlO2、Ca2SiO4、NaFeO2和Na2SiO3等。
(1)写出烧结过程中铝元素转化的化学方程式 。
(2)操作a为冷却、研磨,其中研磨的目的是 。
(3)浸出过程中,NaFeO2可完全水解,水解反应的离子方程式为 。
(4)操作b的名称是 ,所用的玻璃仪器有 、 和烧杯。
(5)“碳化”时生成沉淀,沉淀的化学式为 。
(6)上述过程中循环使用的物质是 。
查看答案和解析>>
科目: 来源:2017届江苏省苏州市高三上学期期初调研化学试卷(解析版) 题型:推断题
酮洛芬是一种良好的抗炎镇痛药,可以通过以下方法合成:

(1)酮洛芬中含氧官能团的名称为 和 。
(2)化合物E的结构简式为 ;由C→D的反应类型是 。
(3)写出B→C的反应方程式 。
(4)写出同时满足下列条件的A的一种同分异构体的结构简式 。
①能发生银镜反应;②与FeCl3发生显色反应;③分子中含有5种不同化学环境的氢。
(5)请写出以甲苯和乙醇为原料制备化合物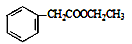 的合成路线流程图(无机试剂可任选)。合成路线流程图示例如图:
的合成路线流程图(无机试剂可任选)。合成路线流程图示例如图:
查看答案和解析>>
科目: 来源:2017届江苏省苏州市高三上学期期初调研化学试卷(解析版) 题型:计算题
镁铝碱式碳酸盐[MgaAlb(OH)c(CO3)d·x H2O]阻燃剂具有阻燃、消烟、填充等功能,是一种不溶于水的新型无机阻燃剂。
(1)将MgaAlb(OH)c(CO3)d·x H2O表示成氧化物形式 。
(2)为确定镁铝碱式碳酸盐的组成,进行如下实验:
准确称取15.050 g样品进行灼烧至恒重,生成CO2 0.560 L(已换算成标准状况下)。分析测得残留物中MgO为6.000 g,Al2O3为2.550 g,通过计算确定该镁铝碱式碳酸盐的化学式。(写出计算过程)
(3)该镁铝碱式碳酸盐可以由MgCl2、NaAlO2、NaOH和Na2CO3反应制备,制备的化学方程式为 。
查看答案和解析>>
科目: 来源:2017届江苏省苏州市高三上学期期初调研化学试卷(解析版) 题型:实验题
碘化钠是实验室中常见的分析试剂,常用于医疗和照相业。工业上通常用水合肼(N2H4·H2O,100℃以上分解)还原法制取碘化钠,工艺流程如下:

(1)合成过程的反应产物中含有IO3-,写出合成过程的离子方程式 。
(2)还原过程必须保持反应温度在60~70℃,这个温度既能保证反应的快速进行,又能 。工业上也可以用Na2S或Fe屑还原制备碘化钠,但水合肼还原法制得的产品纯度更高,原因是 。
(3)请补充完整检验还原液中是否含有IO3-的实验方案:取适量还原液, 。实验中可供选择的试剂:稀盐酸、淀粉溶液、FeCl3溶液。
(4)测定产品中NaI含量的实验步骤如下:
a. 称取4.000g样品、溶解,在250mL容量瓶中定容;
b. 量取25.00mL待测液于锥形瓶中;
c. 用0.1000mol·L-1AgNO3溶液滴定至终点,记录消耗AgNO3溶液的体积;
d. 重复b、c操作2~3次,记录相关实验数据。
①滴定过程中,AgNO3溶液应放在 中;步骤d的目的是 。
②若用上述方法测定产品中的NaI含量偏低(忽略测定过程中的误差),其可能的原因是 。
查看答案和解析>>
科目: 来源:2017届江苏省苏州市高三上学期期初调研化学试卷(解析版) 题型:填空题
CO和联氨(N2H4)的性质及应用的研究是能源开发、环境保护的重要课题。
(1)①用CO、O2和KOH溶液可以制成碱性燃料电池,则该电池反应的离子方程式为 。
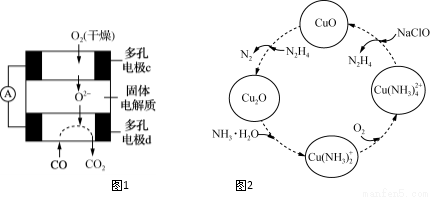
②用CO、O2和固体电解质还可以制成如下图1所示的燃料电池,则电极d的电极反应式为 。
(2)联氨的性质类似于氨气,将联氨通入CuO浊液中,有关物质的转化如图2所示。
①在图示2的转化中,化合价不变的元素是 (填元素名称)。
②在转化过程中通入氧气发生反应后,溶液的pH将 (填“增大”、“减小”或“不变”)。转化中当有1 mol N2H4参与反应时,需要消耗O2的物质的量为 。
③加入NaClO时发生的反应为:
Cu(NH3) +2ClO-+2OH-=Cu(OH)2↓+2N2H4↑+2Cl-+2H2O
+2ClO-+2OH-=Cu(OH)2↓+2N2H4↑+2Cl-+2H2O
该反应需在80℃以上进行,其目的除了加快反应速率外,还有 、 。
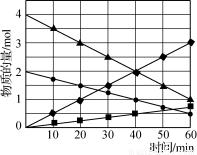
图3
(3)CO与SO2在铝矾土作催化剂、773 K条件下反应生成CO2和硫蒸气,该反应可用于从烟道气中回收硫,反应体系中各组分的物质的量与反应时间的关系如图3所示,写出该反应的化学方程式: 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com