
科目: 来源:2017届四川省校高三上学期第二次月考化学试卷(解析版) 题型:选择题
纯碱被视作“碱”用于油污清洗,溶液碱性较强。下列有关分析不正确的是
A.纯碱主要成分是Na2CO3 B.热的纯碱溶液去污效果更好
C.纯碱有利于油污水解 D.纯碱常用于治疗胃酸过多
查看答案和解析>>
科目: 来源:2017届四川省校高三上学期第二次月考化学试卷(解析版) 题型:选择题
由分类思想,下列说法正确的是
A.氢氧化钠溶液、盐酸都为强电解质
B.铁生锈、食物腐败都涉及有氧化还原反应
C.漂白粉、冰醋酸、氢氧化铁胶体均为混合物
D.二氧化氮、二氧化硅都是酸性氧化物
查看答案和解析>>
科目: 来源:2017届四川省校高三上学期第二次月考化学试卷(解析版) 题型:选择题
设NA为阿伏加德罗常数的值,下列说法正确的是
A.0.2 mol Na2O2和Na2S的混合物中共含有离子数目为0.6 NA
B.1 mol Cl2溶于水的过程中有NA个电子转移
C.常温下,pH=12的氢氧化钠溶液中OH—数目为0.01 NA
D.1.0 mol/L FeCl3溶液全部转化成氢氧化铁胶体所得胶粒数目为NA
查看答案和解析>>
科目: 来源:2017届四川省校高三上学期第二次月考化学试卷(解析版) 题型:选择题
下列离子方程式正确的是
A.向硫酸铝溶液中加入过量氨水:Al3++4NH3·H2O=AlO- 2+4NH+ 4+2H2O
B.少量双氧水滴入酸性KI溶液:2H2O2+2I-+4H+=4H2O+I2
C.磁性氧化铁溶于稀硝酸:3Fe2++4H++NO- 3=3Fe3++NO↑+2H2O
D.碱性锌锰电池正极反应:2MnO2+2H2O+2e-=2MnOOH+2OH-
查看答案和解析>>
科目: 来源:2017届四川省校高三上学期第二次月考化学试卷(解析版) 题型:选择题
下列对如图两烧杯溶液分析一定正确的是
A.甲、乙两烧杯中水电离出的H+浓度:甲<乙
B.分别稀释相同倍数,溶液pH变化:甲=乙
C.相同条件下,AgCl(s)在甲中溶解度大于在乙中
D.向甲烧杯加入NaOH使溶液中性后一定存在:c(Na+)= c(CH3COO-)+ c(CH3COOH)
查看答案和解析>>
科目: 来源:2017届四川省校高三上学期第二次月考化学试卷(解析版) 题型:选择题
下列三个化学反应的平衡常数(K1、K2、K3)与温度的关系分别如下表所示:
化学反应 | 平衡常数 | 温度 | |
973K | 1173K | ||
①Fe(s)+CO2(g) FeO(s)+CO(g) △H1 | K1 | 1.47 | 2.15 |
②Fe(s)+H2O(g) FeO(s)+H2(g) △H2 | K2 | 2.38 | 1.67 |
③CO(g)+H2O(g) CO2(g)+H2(g) △H3 | K3 | ? | ? |
则下列说法正确的是
A.△H1<0,△H2>0
B.反应①②③的反应热满足关系:△H2-△H1=△H3
C.反应①②③的平衡常数满足关系:K1·K2=K3
D.要使反应③在一定条件下建立的平衡向正反应方向移动,可采取升温措施
查看答案和解析>>
科目: 来源:2017届四川省校高三上学期第二次月考化学试卷(解析版) 题型:填空题
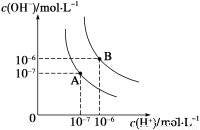
(1)水的电离平衡曲线如图所示,若A点、B点分别表示25 ℃和100 ℃时水的电离达平衡时的离子浓度。则表示25 ℃的是___________(填“A”或“B”)。100 ℃时,在1 mol·L-1的NaOH溶液中,由水电离出的c(H+)=__________mol·L-1。100 ℃时,5×10-5 mol·L-1的H2SO4溶液与pH=9的Ba(OH)2溶液混合后pH=7,则混合前H2SO4溶液与Ba(OH)2溶液的体积比为 。
(2)电离平衡常数是衡量弱电解质电离程度强弱的量。已知如表数据。
化学式 | 电离平衡常数(25 ℃) |
HCN | K=4.9×10-10 |
CH3COOH | K=1.8×10-5 |
H2CO3 | K1=4.3×10-7、K2=5.6×10-11 |
①25℃时,有等浓度的NaHCO3溶液、NaCN溶液、Na2CO3溶液、CH3COONa溶液,四种溶液的pH由大到小的顺序为_________________________。
②25℃时,等浓度的CH3COOH溶液和NaOH溶液等体积混合,所得溶液显碱性,则c(Na+)__________c(CH3COO-)(填“>”、“<”或“=”)。
③向NaCN溶液中通入少量CO2,所发生反应的离子方程式为_______________________。
(3)在化学分析中采用K2CrO4为指示剂,以AgNO3标准溶液滴定溶液中的Cl?,利用Ag+与CrO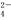 生成砖红色沉淀,指示到达滴定终点。当溶液中Cl?恰好完全沉淀(浓度等于1.0×10?5 mol·L?1)时,溶液中c(Ag+)为___________mol·L?1,此时溶液中c(CrO
生成砖红色沉淀,指示到达滴定终点。当溶液中Cl?恰好完全沉淀(浓度等于1.0×10?5 mol·L?1)时,溶液中c(Ag+)为___________mol·L?1,此时溶液中c(CrO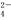 )等于__________ mol·L?1。(已知Ag2CrO4、AgCl的Ksp分别为2.0×10?12和2.0×10?10)。
)等于__________ mol·L?1。(已知Ag2CrO4、AgCl的Ksp分别为2.0×10?12和2.0×10?10)。
查看答案和解析>>
科目: 来源:2017届四川省校高三上学期第二次月考化学试卷(解析版) 题型:填空题
汽车尾气排放的NO和CO都是有毒的气体,科学家正在研究利用催化技术将尾气中的NO和CO转变成无毒的CO2和N2,减少污染。
(1)已知:N2(g)+O2(g)=2NO(g) △H=+180.0 kJ/mol
2C(s)+O2(g)=2CO(g) △H=-221.0 kJ/mol
2C(s)+2O2(g)=2CO2(g) △H=-787.0 kJ/mol
则尾气转化反应:2NO(g)+2CO(g) N2(g)+2CO2(g) △H=
N2(g)+2CO2(g) △H=  。
。
(2)对于反应2NO(g)+2CO(g) N2(g)+2CO2(g),为了测定
N2(g)+2CO2(g),为了测定 在某种催化剂作用下的
在某种催化剂作用下的 反应速率,用气体传感器测得不同时间的NO和CO浓度如下表
反应速率,用气体传感器测得不同时间的NO和CO浓度如下表
时间/s | 0 | 1 | 2 | 3 | 4 | 5 |
c(NO)/×10-4 mol/L | 3.00 | 2.25 | 1.75 | 1.36 | 1.00 | 1.00 |
c(CO)/×10-4 mol/L | 4.00 | 3.25 | 2.75 | 2.36 | 2.00 | 2.00 |
请回答下列问题(均不考虑温度变化对催化剂催化效率的影响):
①前2s内的平均反应速率 υ(CO2)= mol/(L•s)。
②在该温度下,反应的平衡常数K= 。
(3)假设在恒容密闭容器中发生上述反应,下列有关说法正确的是 。
A.选用更有效的催化剂能提高尾气的转化率
B.升高反应体系的温度能提高反应速率, 提高尾气的转化率
C.相同温度下,若NO和CO的起始浓度分别为1.50×10-4 mol/L和2.00×10-4 mol/L,平衡时N2的体积分数比原平衡体系中N2的体积分数低
D.单位时间内消耗NO的物质的量等于生成CO2的物质的量时即达平衡状态
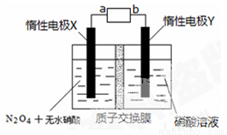
(4)用尾气NO2为原料可制新型硝化剂N2O5,原理:先将NO2转化为N2O4,再采用电解法制备N2O5,装置如右图所示则电源b极是__________极(填“正”“负”),生成N2O5电极反应式为 ,电解一段时间后硝酸溶液的pH (填“增大”“减小”“不变”)。
查看答案和解析>>
科目: 来源:2017届四川省校高三上学期第二次月考化学试卷(解析版) 题型:实验题
纳米级Fe粉是新型材料,具有超强磁性、高效催化性。某化学小组探究用氢气和碳酸亚铁制取纳米级铁粉。其实验设计如图(加热、支持装置省略)
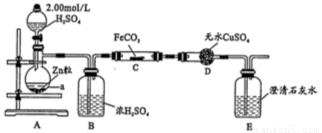
(1)a的名称是________________;浓硫酸的作用是________________。
(2)打开分液漏斗活塞,一段时间后再对C装置加热,这样操作的目的是_______________;反应一段时间后D中变蓝,E中溶液变浑浊,C中发生反应的化学方程式为______________。
(3)反应中若观察到B装置中气泡产生过快,则应进行的操作是_____________________。
(4)反应一段时间后,B中产生气泡太慢,再滴加硫酸反应速率略有加快但不明显;若向硫酸中加少量硫酸铜再滴入与Zn反应,反应速率明显加快,原因是____________________。
(5)检验碳酸亚铁中含有铁元素的实验方法是______________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com