
科目: 来源:2016-2017学年四川省高二上10月月考化学试卷(解析版) 题型:选择题
某体积可变的密闭容器,盛有适量的A和B的混合气体,在一定条件下发生反应:A(g) +3B(g)  2C(g)。若维持温度和压强不变,当达到平衡时容器的体积为V,其中C气体的体积占10%。下列推断正确的是
2C(g)。若维持温度和压强不变,当达到平衡时容器的体积为V,其中C气体的体积占10%。下列推断正确的是
A.原混合气体的体积为1.2V B.原混合气体的体积为1.1V
C.反应达平衡时气体B消耗掉0.05V D.反应达到平衡时气体A消耗掉0.05V
查看答案和解析>>
科目: 来源:2016-2017学年四川省高二上10月月考化学试卷(解析版) 题型:选择题
向密闭容器中充入1.0 mol CO和2.0 mol H2O(g)发生反应:CO(g)+H2O(g) CO2(g)+H2(g)。当反应达平衡时,CO的体积分数为α。若维持容器的体积和温度不变,起始物质按下列四种配比充入该容器中,达平衡时CO的体积分数小于α的是
CO2(g)+H2(g)。当反应达平衡时,CO的体积分数为α。若维持容器的体积和温度不变,起始物质按下列四种配比充入该容器中,达平衡时CO的体积分数小于α的是
A.0.5 mol CO+2.0 mol H2O(g)+1.0 mol CO2+1.0 mol H2
B.1.0 mol CO+2.0 mol H2O(g)+0.5 mol He
C.1.0 mol CO+1.0 mol H2O(g)+1.0 mol CO2+1.0 mol H2
D.0.5 mol CO+1.5 mol H2O(g)+0.4 mol CO2+0.4 mol H2
查看答案和解析>>
科目: 来源:2016-2017学年四川省高二上10月月考化学试卷(解析版) 题型:选择题
700℃时,H2(g)+CO2(g)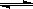 H2O(g)+CO(g)。该温度下,在甲、乙、丙三个恒容密闭容器中,投入H2和CO2,起始浓度如下表所示。其中甲经2min达平衡时,v(H2O)为0.025mol/(L·min),下列判断不正确的是
H2O(g)+CO(g)。该温度下,在甲、乙、丙三个恒容密闭容器中,投入H2和CO2,起始浓度如下表所示。其中甲经2min达平衡时,v(H2O)为0.025mol/(L·min),下列判断不正确的是
起始浓度 | 甲 | 乙 | 丙 |
c(H2)/mol/L | 0.10 | 0.20 | 0.20 |
c(CO2)/mol/L | 0.10 | 0.10 | 0.20 |
A.平衡时,乙中CO2的转化率大于50%
B.当反应平衡时,丙中c(CO2)是甲中的2倍
C.温度升至800℃,上述反应平衡常数为25/16,则正反应为吸热反应
D.其他条件不变,若起始向容器乙中充入0.10mol/L H2和0.20 mol/L CO2,到达平衡时c (CO)与乙不同
查看答案和解析>>
科目: 来源:2016-2017学年四川省高二上10月月考化学试卷(解析版) 题型:选择题
已知2SO2(g)+O2(g)  2SO3(g) ΔH=-197 kJ·mol-1.向同温、同体积的三个密闭容器中分别充入气体:(甲)2 mol SO2和1 mol O2;(乙)1 mol SO2和0.5 mol O2;(丙)2 mol SO3.恒温、恒容下反应达平衡时,下列关系一定正确的是
2SO3(g) ΔH=-197 kJ·mol-1.向同温、同体积的三个密闭容器中分别充入气体:(甲)2 mol SO2和1 mol O2;(乙)1 mol SO2和0.5 mol O2;(丙)2 mol SO3.恒温、恒容下反应达平衡时,下列关系一定正确的是
A.容器内压强P:P甲=P丙>2P乙
B.SO2的质量m:m甲=m丙>2m乙
C.c(SO2)与c(O2)之比k:k甲=k丙=2k乙
D.甲乙中SO2的转化率分别为??甲、??乙,丙中SO3的转化率为??丙:??甲>??乙,??甲+??丙=1
查看答案和解析>>
科目: 来源:2016-2017学年四川省高二上10月月考化学试卷(解析版) 题型:选择题
一定条件下存在反应:CO(g)+H2O(g)  CO2(g)+H2(g),其正反应放热。现有三个相同的2 L恒容绝热(与外界没有热量交换)密闭容器Ⅰ、Ⅱ、Ⅲ,在Ⅰ中充入1 mol CO和1 mol H2O,在Ⅱ中充入1 mol CO2和1 mol H2,在Ⅲ中充入2 mol CO和2 mol H2O,700 ℃条件下开始反应。达到平衡时,下列说法正确的是
CO2(g)+H2(g),其正反应放热。现有三个相同的2 L恒容绝热(与外界没有热量交换)密闭容器Ⅰ、Ⅱ、Ⅲ,在Ⅰ中充入1 mol CO和1 mol H2O,在Ⅱ中充入1 mol CO2和1 mol H2,在Ⅲ中充入2 mol CO和2 mol H2O,700 ℃条件下开始反应。达到平衡时,下列说法正确的是
A.容器Ⅰ中CO的转化率与容器Ⅱ中CO2的转化率之和小于1
B.容器Ⅰ、Ⅲ中反应的平衡常数相同
C.容器Ⅰ中CO的物质的量比容器Ⅱ中的多
D.容器Ⅰ、Ⅱ中正反应速率相同
查看答案和解析>>
科目: 来源:2016-2017学年四川省高二上10月月考化学试卷(解析版) 题型:填空题
甲小组以H2O2分解为例,探究外界条件对反应速率的影响。在常温下按照下表所示的方案完成实验。
实验编号 | 反应物 | 催化剂 |
① | 10 mL 2% H2O2溶液 | 无 |
② | 10 mL 5% H2O2溶液 | 无 |
③ | 10 mL 5% H2O2溶液 | 1 mL 0.1 mol·L-1 FeCl3溶液 |
(1)实验①和②的目的是 。进行实验时没有观察到明显现象而无法得出结论。资料显示,通常条件下H2O2稳定,不易分解。为了达到实验目的,你对原实验方案的改进方法是 (填一种即可)。
(2)利用实验②和③可知加入FeCl3溶液可以催化H2O2分解,已知FeCl3溶液中含有H2O、Fe3+和Cl-三种粒子,为探究哪种粒子具有催化作用,有如下三种猜想:
猜想1:真正催化分解H2O2的是FeCl3溶液中的H2O
猜想2:真正催化分解H2O2的是FeCl3溶液中的Fe3+
猜想3:真正催化分解H2O2的是FeCl3溶液中的Cl-
你认为最不可能的是猜想 ;理由是 。
(3)同学们又对余下的两种猜想进行了实验探究,请你帮助他们填写下表:
实验步骤 | 实验现象 | 实验结论 |
向盛有5 mL 15%的H2O2溶液的试管中加入少量的HCl,然后把带火星的木条伸入试管中。 | 无明显现象 | ① |
向盛有5 mL 15%的H2O2溶液的试管中加入少量的FeCl3固体,然后把带火星的木条伸入试管中。 | ② | ③ |
乙小组通过Na2S2O3与0.1 mol·L-1 H2SO4反应溶液浑浊的时间,研究外界条件对化学反应速率的影响。设计实验如下:
实验编号 | 温度/℃ | Na2S2O3 | V(H2SO4)/mL | V(H2O)/mL | |
c/mol·L-1 | V/mL | ||||
① | 25 | 0.1 | 5.0 | 10.0 | a |
② | 25 | 0.1 | 10.0 | 10.0 | 0 |
③ | 25 | 0.1 | 5.0 | 5.0 | b |
(4)已知:反应中除生成淡黄色沉淀外还会生成刺激性气味的气体,写出反应离子方程式: ;
(5)若同时选择实验①②、实验①③,测定混合液变浑浊的时间,可分别探究Na2S2O3浓度和H2SO4的浓度对化学反应速率的影响,则表中b为 mL。
查看答案和解析>>
科目: 来源:2016-2017学年四川省高二上10月月考化学试卷(解析版) 题型:填空题
合成氨对化学工业和国防工业具有重要意义。
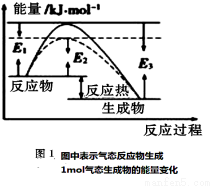

(1)根据图1请写出合成氨的热化学方程式 (热量用E1、E2或E3表示)
(2)向合成塔中按物质的量之比l:4充入N2、H2进行氨的合成,图2为T℃时平衡混合物中氨气的体积分数与压强(p)的关系图。
①图2中氨气的体积分数为15%时,H2的转化率为 。
②图3中T=450℃,则温度为500℃时对应的曲线是 (填“a”或“b”)。
(3)合成氨所需的氢气可由甲烷与水反应制得,反应的热化学方程式为CH4(g)+H2O(g) CO(g)+3H2(g) △H>0,一定温度下,在体积为2 L的恒容容器中发生上述反应,各物质的物质的量变化如下表:
CO(g)+3H2(g) △H>0,一定温度下,在体积为2 L的恒容容器中发生上述反应,各物质的物质的量变化如下表:
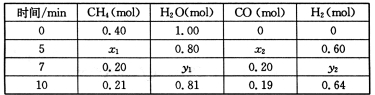
①分析表中数据,判断5 min时反应是否处于平衡状态? (填“是”或“否”),前5 min反应的平均反应速率v(CH4) = 。
②在相同实验条件下,若改为加入CH4 0.1mol,若要求平衡后H2在反应混合气中质量分数不变,则还需加入的物质及其物质的量为
③反应在7~10 min内,CO的物质的量减少的原因可能是 (填字母)。
a.减少CH4的物质的量 b.降低温度 c.升高温度 d.充入H2
④下列方法中可以证明上述已达平衡状态的是
a.单位时间内生成3n mol H2的同时生成n mol CO
b.容器内压强不再变化
c.混合气体密度不再变化
d.混合气体的平均相对分子质量不再变化
e.CH4的质量分数不再变化
⑤已知碳的气化反应在不同温度下平衡常数的对数值(lgK)如下表:

则反应CO(g)+H2O(g)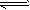 CO2(g)+H2(g)在900K时,该反应平衡常数的对数值(lgK)=_________.
CO2(g)+H2(g)在900K时,该反应平衡常数的对数值(lgK)=_________.
查看答案和解析>>
科目: 来源:2016-2017学年四川省高二上10月月考化学试卷(解析版) 题型:实验题
硫酸铁铵aFe2(SO4) 3·b(NH4) 2SO4·cH2O]广泛用于城镇生活饮用水、工业循环水的净化处理等。某化工厂以硫酸亚铁(含少量硝酸钙)和硫酸铵为原料,设计了如下工艺流程制取硫酸铁铵。

请回答下列问题:
(1)硫酸亚铁溶液加H2SO4酸化的主要目的是_________________,滤渣A的主要成分是_______________。
(2)下列物质中最适合的氧化剂B是________;反应的离子方程式 。
a.NaClO b.H2O2 c.KMnO4 d.K2Cr2O7
(3)操作甲、乙的名称分别是:甲______________,乙___________________。
(4)上述流程中,氧化之后和加热蒸发之前,需取少量溶液检验Fe2+是否已全部被氧化,所加试剂 能否用酸性的KMnO4溶液? (填“能”或“不能”)理由是: 。(可用语言或方程式说明)
(5)检验硫酸铁铵中NH4+的方法是____________________________。
(6)称取14.00 g样品,将其溶于水配制成100 mL溶液,分成两等份,向其中一份中加入足量NaOH溶液,过滤洗涤得到2.14 g沉淀;向另一份溶液中加入0.05 mol Ba (NO3) 2溶液,恰好完全反应。则该硫酸铁铵的化学式为______________________。
查看答案和解析>>
科目: 来源:2016-2017学年云南省曲靖市高二上第一次月考化学卷(解析版) 题型:选择题
已知25℃、101kPa条件下:①4Al (s) + 3O2 (g) = 2Al2O3 (s) △H = - 2834.9 kJ/mol; ②4Al (s) + 2O3 (g) = 2Al2O3 (s) △H = - 3119.91kJ/mol。由此得出的结论正确的是( )
A.等质量的O2比O3能量低,由O2变O3 为吸热反应
B.等质量的O2比O3能量低,由O2变O3 为放热反应
C.O3比O2稳定,由O2变O3 为吸热反应
D.O 2比O3稳定,由O2变O3 为
2比O3稳定,由O2变O3 为 放热反应
放热反应
查看答案和解析>>
科目: 来源:2016-2017学年云南省曲靖市高二上第一次月考化学卷(解析版) 题型:选择题
白磷与氧可发生如下反 应:P4+5O2=P4O10。已知断裂下列化学键需要吸收的能量分别为:P—P akJ·mol—1、P—O bkJ·mol—1、P=O ckJ·mol—1、O=O dkJ·mol—1。
应:P4+5O2=P4O10。已知断裂下列化学键需要吸收的能量分别为:P—P akJ·mol—1、P—O bkJ·mol—1、P=O ckJ·mol—1、O=O dkJ·mol—1。

根据图示的分子结构和有关数据估算该反应的△H,其中正确的是( )
A.(6a+5d-4c-1 2b)kJ·mol—1 B.(4c+12b-6a-5d)kJ·mol—1
2b)kJ·mol—1 B.(4c+12b-6a-5d)kJ·mol—1
C.(4c+12b-4a-5d)kJ·mol—1 D.(4a+5d-4c-12b)kJ·mol—1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com