
科目: 来源: 题型:解答题
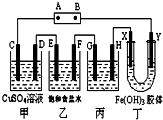 课题式研究性学习是培养学生创造思维的良好方法,某研究性学习小组将下列装置如图连接,C、D、E、F、X、Y 都是惰性电极.将电源接通后,向乙中滴入酚酞试液,在F极附近显红色.试回答下列问题:
课题式研究性学习是培养学生创造思维的良好方法,某研究性学习小组将下列装置如图连接,C、D、E、F、X、Y 都是惰性电极.将电源接通后,向乙中滴入酚酞试液,在F极附近显红色.试回答下列问题:查看答案和解析>>
科目: 来源: 题型:选择题
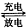 VO2++2H++V2+..下列说法正确的是( )
VO2++2H++V2+..下列说法正确的是( )| A. | 放电时正极反应为:VO${\;}_{2}^{+}$+2H++e-═VO2++H2O | |
| B. | 充电过程中,H+由阴极区向阳极区迁移 | |
| C. | 放电过程中电子由负极经外电路移向正极,再由正极经电解质溶液移向负极 | |
| D. | 充电时阴极反应为:V2+-e-═V3+ |
查看答案和解析>>
科目: 来源: 题型:填空题
查看答案和解析>>
科目: 来源: 题型:填空题
 重庆市对大气进行监测,发现该市首要污染物为可吸入颗粒物PM2.5(直径小于等于2.5μm的悬浮颗粒物),其主要来源为燃煤、机动车尾气等.因此,对PM2.5、SO2、NOx等进行研究具有重要意义.请回答下列问题:
重庆市对大气进行监测,发现该市首要污染物为可吸入颗粒物PM2.5(直径小于等于2.5μm的悬浮颗粒物),其主要来源为燃煤、机动车尾气等.因此,对PM2.5、SO2、NOx等进行研究具有重要意义.请回答下列问题:| 离子 | K+ | Na+ | NH4+ | SO42- | NO3- | Cl- |
| 浓度/mol•L-1 | 4×10-6 | 6×10-6 | 2×10-5 | 4×10-5 | 3×10-5 | 2×10-5 |
查看答案和解析>>
科目: 来源: 题型:选择题
| t/s | 0 | t1 | t2 | t3 | t4 |
| n(SO3)/mol | 0 | 0.8 | 1.4 | 1.8 | 1.8 |
| A. | 反应在前t1s的平均速率v(O2)=0.4/t1mol•L-1•s-1 | |
| B. | 保持其他条件不变,体积压缩到1.0L,平衡常数将增大 | |
| C. | 保持温度不变,向该容器中再充入0.3 molSO2、0.1molO2和0.2molSO3,则此时V正>V逆 | |
| D. | 相同温度下,起始时向容器中充入4mol SO3,达到平衡时,SO3的转化率大于10% |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. |  如图反应:若p1>p2,则此反应只能在高温下自发进行 | |
| B. | 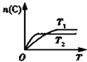 如图反应:此反应的△H<0,且T1<T2 | |
| C. | 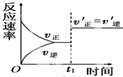 如图反应:表示t1时刻一定是使用催化剂对反应速率的影响 | |
| D. | 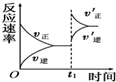 如图反应:表示t1时刻增大B的浓度对反应速率的影响 |
查看答案和解析>>
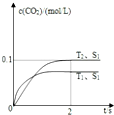
科目: 来源: 题型:选择题
| A. | z=2 | B. | 2s后,容器内的压强是初始的$\frac{7}{8}$倍 | ||
| C. | 2s时C的体积分数为$\frac{2}{7}$ | D. | 2s后,B的浓度为0.5mol/L |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 水解平衡正向移动 | B. | 各微粒浓度均变小 | ||
| C. | 溶液中离子数目增多 | D. | c(Al3+)与c(SO42-)的比值减小 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 使甲基橙变红的溶液:Fe2+、K+、SO42-、NO3- | |
| B. | 中性溶液中:Fe3+、Na+、NO3-、Cl- | |
| C. | 0.1mol•L-1NaAlO2溶液:K+、OH-、Cl-、NO3- | |
| D. | 水电离出的c(H+)=10-12mol•L-1的溶液:Na+、K+、NH4+、[Ag(NH3)2]+ |
查看答案和解析>>
科目: 来源: 题型:选择题

| A. | ${\;}_{2}^{3}$He核聚变是化学变化 | |
| B. | ${\;}_{2}^{3}$He和42He互为同素异形体 | |
| C. | ${\;}_{2}^{3}$He原子核内含仅含有1个中子 | |
| D. | ${\;}_{2}^{4}$He的最外层电子数为2,所以易失电子 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com