
科目: 来源: 题型:选择题
| A. | 常温下,pH值等于14与pH值等于12的两种NaOH溶液等体积混和后,c(H+)=$\frac{1{0}^{-14}+1{0}^{-10}}{2}$ | |
| B. | 常温下,浓度为1×10-10mol/L的KOH溶液的pH值最接近于4 | |
| C. | 氨水加水稀释,溶液中除水以外的所有粒子的浓度都减小 | |
| D. | 常温下,相同温度下pH值等于1的盐酸溶液中水的电离程度与pH值等于13的Ba(OH)2溶液中水的电离程度相等 |
查看答案和解析>>
科目: 来源: 题型:解答题
 如图是实验室中制备气体或验证气体性质的装置图.回答下列问题:
如图是实验室中制备气体或验证气体性质的装置图.回答下列问题:查看答案和解析>>
科目: 来源: 题型:填空题
查看答案和解析>>
科目: 来源: 题型:解答题
 氧化亚铜(Cu2O)作为一种重要的无机化工原料,在涂料、有色玻璃和催化剂等领域有着广泛的用途.回答下列问题:
氧化亚铜(Cu2O)作为一种重要的无机化工原料,在涂料、有色玻璃和催化剂等领域有着广泛的用途.回答下列问题:查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 20mL0.1mol/L CH3COONa溶液与10mL0.1 mol/L HCl溶液混合后溶液呈酸性,所得溶液中:c(CH3COO-)>c(Cl-)>c(CH3COOH)>c(H+) | |
| B. | 含等物质的量的NaHC2O4和Na2C2O4的混合溶液:2c(Na +)=3[c(HC2O4-)+c(C2O42-)+c(H2C2O4)] | |
| C. | PH=1的NaH SO4溶液:c(H+)=c(SO42-)+c(OH -) | |
| D. | CO2的水溶液:c(H+)>c(HCO3-)=2c(CO32-) |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 途径①反应中体现了浓硝酸的强氧化性和酸性 | |
| B. | 途径②的第二步反应在实际生产中可以通过增大O2浓度来提高产率 | |
| C. | 由途径①和②分别制取1mol H2SO4,理论上各消耗1mol S,各转移6mol电子 | |
| D. | 途径②与途径①相比更能体现“绿色化学”理念,是因为途径②比途径①污染相对小且原子利用率高 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 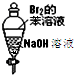 振荡后静置,溶液不再分层,且保持无色透明 | |
| B. |  铁片最终完全溶解,且高锰酸钾溶液变无色 | |
| C. |  微热稀HNO3片刻,溶液中有气泡产生,广口瓶内出现红棕色气体 | |
| D. |  当溶液至红褐色,停止加热,液体变为黄色 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | Na2CO3可溶,NaHCO3难溶 | |
| B. | 可用Ca(OH)2溶液鉴别Na2CO3和NaHCO3两种溶液 | |
| C. | Na2CO3中的NaHCO3可通过加热的方法除去 | |
| D. | Na2CO3不能转化成与NaHCO3,而NaHCO3能转化为Na2CO3 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 光导纤维的主要成分是硅 | |
| B. | 硅很活泼,在自然界中没有游离态形式 | |
| C. | 硅酸钠可用于木材防火 | |
| D. | SiO2与烧碱和氢氟酸都能反应,是两性氧化物 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com