
科目: 来源: 题型:填空题
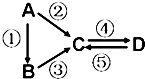 A、B、C、D均为中学化学常见的纯净物,A是单质.它们之间有如下的反应关系:
A、B、C、D均为中学化学常见的纯净物,A是单质.它们之间有如下的反应关系:查看答案和解析>>
科目: 来源: 题型:填空题
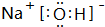 ,其中存在的化学键类型为离子键、共价键.
,其中存在的化学键类型为离子键、共价键.查看答案和解析>>
科目: 来源: 题型:解答题
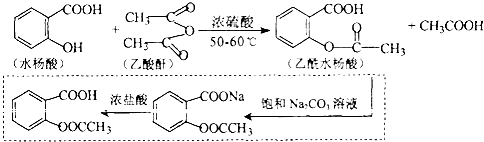


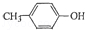 也能与乙酸酐发生类似反应,请写出化学反应方程式,可不写条件:
也能与乙酸酐发生类似反应,请写出化学反应方程式,可不写条件: .
.查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:选择题
 pH=2的X、Y、Z三种酸的溶液各1mL,分别稀释到1000mL,其pH与溶液体积(V)的变化关系如图所示,下列正确的是 ( )
pH=2的X、Y、Z三种酸的溶液各1mL,分别稀释到1000mL,其pH与溶液体积(V)的变化关系如图所示,下列正确的是 ( )| A. | X、Y和Z都是弱酸 | B. | 稀释前的浓度大小为c(Z)>c(X)>c(Y) | ||
| C. | 稀释前电离程度大小为X>Y>Z | D. | pH=2时,X、Y、Z都是稀溶液 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | $\frac{(4{×10}^{-9}+1{×10}^{-12})}{5}$ | B. | $\frac{(8{×10}^{-9}+1{×10}^{-12})}{5}$ | ||
| C. | 5×10-10 | D. | 5×10-12 |
查看答案和解析>>
科目: 来源: 题型:解答题

查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com