
科目: 来源: 题型:解答题

查看答案和解析>>
科目: 来源: 题型:解答题
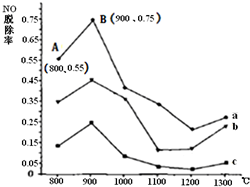 尿素[CO(NH2)2]在一定条件下能有效将NO转化为N2.如图为CO(NH2)2与某种烟气(主要为N2、NO)中NO的物质的量比值分别为1:2、2:1、3:1时,NO脱除率(NO的消耗量与NO的原始量的比值)随温度变化的曲线图.
尿素[CO(NH2)2]在一定条件下能有效将NO转化为N2.如图为CO(NH2)2与某种烟气(主要为N2、NO)中NO的物质的量比值分别为1:2、2:1、3:1时,NO脱除率(NO的消耗量与NO的原始量的比值)随温度变化的曲线图.查看答案和解析>>
科目: 来源: 题型:多选题

| A. | X分子中有2个手性碳原子 | |
| B. | Y分子中所有原子可能在同一平面内 | |
| C. | 可用FeCl3溶液或NaHCO3溶液鉴别X和Y | |
| D. | 在NaOH溶液中,1molM最多可与5molNaOH发生反应 |
查看答案和解析>>
科目: 来源: 题型:解答题
| 起始温度T1/℃ | 终止温度T2/℃ | 温度差(T2-T1)/℃ | |||
| HCl | NaOH | 平均值 | |||
| 1 | 25.5 | 25.0 | 25.25 | 28.5 | 3.25 |
| 2 | 24.5 | 24.5 | 24.50 | 27.5 | 3.00 |
| 3 | 25.0 | 24.5 | 24.75 | 26.5 | 1.75 |
查看答案和解析>>
科目: 来源: 题型:填空题
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:填空题
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | Na+、SO42-、Cl-、NO3- | B. | Na+、HCO3-、Ca2+、Cl- | ||
| C. | Na+、Cl-、NO3-、Fe3+ | D. | K+、Cl、CO32-、NO3- |
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:选择题

| A. | 反应物的键能总和比生成物的键能总和高 | |
| B. | E1为反应物的平均能量与过渡态的能量差,称为正反应的活化能 | |
| C. | 正反应的热效应为△H=E1-E2,且E2>E1,所以正反应为放热反应 | |
| D. | 使用合适的催化剂能同时降低E1和E2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com