
科目: 来源: 题型:选择题
| A. | ① | B. | ② | C. | ③ | D. | ④ |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 常温下,0.1mol•L-1Na2S溶液中存在;c(OH-)═c(H+)+c(HS-)+2c(H2S) | |
| B. | 常温下,HA溶液与0.1 mol•L-1NaOH溶液正好完全反应时,溶液中一定存在:c(Na+)═c(A-)>c(OH-)=c(H+) | |
| C. | 常温下,向0.1 mol•L-1CH3COOH 溶液加水稀释,当溶液的pH从3.0升到4.0时,溶液中$\frac{c(C{H}_{3}CO{O}^{-})}{c(C{H}_{3}COOH)}$的值增大到原来的10倍 | |
| D. | 常温下,pH=7的CH3COONa和CH3COOH混合溶液中:c(Na+)=0.1 mol•L-1;c(Na+)═c(CH3COOH)>c(CH3COO-)>c(H+)=c(OH-) |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 甲酸钠溶液和盐酸反应:HCOO-+H+═HCOOH | |
| B. | 硫化钠的第一步水解:S2-+2H2O?H2S+2OH- | |
| C. | 醋酸钡溶液和硫酸反应:Ba2++SO42-═BaSO4↓ | |
| D. | 碳酸氢钠的水解:HCO3-+H2O═H3O++CO32- |
查看答案和解析>>
科目: 来源: 题型:解答题
 一定温度下,某容积为2L的密闭容器内,某一反应中M、N的物质的量随反应时间变化的曲线如图,依图所示:
一定温度下,某容积为2L的密闭容器内,某一反应中M、N的物质的量随反应时间变化的曲线如图,依图所示:查看答案和解析>>
科目: 来源: 题型:解答题
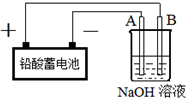 Cu2O是一种半导体材料,实验室用铅酸蓄电池电解一定浓度的NaOH溶液制备Cu2O,方程式为2Cu+H2O$\frac{\underline{\;电解\;}}{\;}$Cu2O+H2↑装置如图所示,回答下列问题
Cu2O是一种半导体材料,实验室用铅酸蓄电池电解一定浓度的NaOH溶液制备Cu2O,方程式为2Cu+H2O$\frac{\underline{\;电解\;}}{\;}$Cu2O+H2↑装置如图所示,回答下列问题查看答案和解析>>
科目: 来源: 题型:解答题
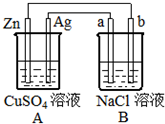 如图所示的装置中电极a、b均为碳棒,两烧杯中所盛溶液均为500mL 1.0mol/L.
如图所示的装置中电极a、b均为碳棒,两烧杯中所盛溶液均为500mL 1.0mol/L.查看答案和解析>>
科目: 来源: 题型:解答题
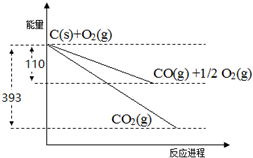 完成下列方程式
完成下列方程式查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 50% | B. | 80% | C. | 88% | D. | 95% |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 电镀时,待镀金属连接电源负极,发生氧化反应 | |
| B. | 工业上电解NaCl水溶液制备钠,电解熔融态Al2O3制备Al | |
| C. | 往往将铁闸门与直流电源的负极相连,这是牺牲阳极的阴极保护法 | |
| D. | 电解精炼铜时,电解液选用硫酸酸化的硫酸铜,精炼过程中,Cu2+浓度降低 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 浓硫酸和NaOH溶液反应,生成 l mol水时放热57.3 kJ | |
| B. | 含l molH2SO4的稀硫酸与足量稀NaOH溶液中和后,放热为57.3 kJ | |
| C. | 1L 0.l mol/L CH3COOH与1L 0.l mol/L NaOH溶液反应后放热为5.73 kJ | |
| D. | 1L 0.l mol/L HNO3与 1L 0.l mol/L NaOH溶液反应后放热为 5.73 kJ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com