
科目: 来源: 题型:选择题
| A. | OH-的电子式: | |
| B. | 乙酸的分子式C2H4O2 | |
| C. | 硫离子结构示意图 | |
| D. | 氢氧化钡电离方程式:Ba(OH)2═Ba2++OH2- |
查看答案和解析>>
科目: 来源: 题型:解答题

| 实验编号 | 待测液体积 (mL) | 消耗盐酸体积(mL) | |
| 初读数 | 末读数 | ||
| 1 | 20.00 | 0.00 | 25.02 |
| 2 | 20.00 | 0.20 | 28.80 |
| 3 | 20.00 | 1.30 | 26.28 |
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 从海水中富集含微量元素的化合物 | B. | 使含微量元素的离子沉淀 | ||
| C. | 对含微量元素的混合物进行提纯 | D. | 从化合物中冶炼这些单质 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 向硝酸银溶液中加盐酸:Ag++Cl-═AgCl↓ | |
| B. | 碳酸氢钙溶液跟盐酸反应:Ca(HCO3)2+2H+═Ca2++2H2O+2CO2↑ | |
| C. | 盐酸跟氢氧化镁反应:H++OH-═H2O | |
| D. | 碳酸镁跟硫酸反应:MgCO3+H+═Mg2++H2O+CO2↑ |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | CO2(SO2):通过饱和Na2CO3溶液,洗气 | |
| B. | Cl2(HCl):通过NaOH固体,吸收 | |
| C. | BaCl2溶液(HCl):加入足量BaCO3,过滤 | |
| D. | FeCl3溶液(CuCl2):通入足量Fe,过滤 |
查看答案和解析>>
科目: 来源: 题型:选择题
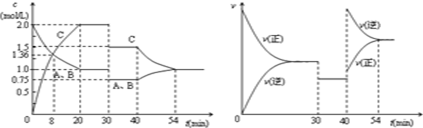
| A. | 30min时降低温度,40min时升高温度 | |
| B. | 8min时反应平衡 | |
| C. | 反应方程式中的x=1,正反应为放热反应 | |
| D. | 该反应20~30min的平衡常数比30~40min的平衡常数大 |
查看答案和解析>>
科目: 来源: 题型:多选题
| 弱酸 | HCOOH | HCN | H2CO3 |
| 电离平衡常数 (25°C)) | Ki=1.77×10-4 | Ki=4.9×10-18 | Ki1=4.3×10-7 Ki2=5.6×10-11 |
| A. | CN-+H2O+CO2→HCN+HCO3- | |
| B. | 2HCOOH+CO32-→2HCOO-+H2O+CO2↑ | |
| C. | 中和等体积、等pH的HCOOH和HCN消耗NaOH的量前者大于后者 | |
| D. | 等体积、等浓度的HCOONa和NaCN溶液中所含离子总数前者小于后者 |
查看答案和解析>>
科目: 来源: 题型:选择题

| A. | SO2(g)+2CO(g)═S(s)+2CO2(g)△H=-(2b-a)kJ•mol-1 | |
| B. | SO2(g)+2CO(g)═S(s)+2CO2(g)△H=-(b-a)kJ•mol-1 | |
| C. | SO2(g)+2CO(g)═S(s)+2CO2(g)△H=(2b-a)kJ•mol-1 | |
| D. | SO2(g)+2CO(g)═S(s)+2CO2(g)△H=-(2b+a)kJ•mol-1 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 0.1 mol•L -1 NaHC2O4溶液与0.1 mol•L -1KOH溶液等体积混合,所得溶液中:c(Na+)>c(K+)>c(C2O42-)>c(OH-)>c(HC2O4-) | |
| B. | 20mL 0.1 mol•L -1NH4Cl溶液与10mL 0.1 mol•L -1NaOH溶液混合后溶液呈碱性,所得溶液中:c(Cl-)>c(NH4+)>c(Na+)>c(OH-)>c(H+) | |
| C. | 常温下,pH=2的HF溶液与pH=12的氢氧化钠溶液等体积混合,所得溶液中:c(Na+)+c(OH-)>c(H+)+c(F-) | |
| D. | 0.1 mol•L -1NH3•H2O溶液与0.1 mol•L -1HNO3溶液等体积混合,所得溶液中:c(H+)>c(OH-)+c(NH3•H2O) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com