
科目: 来源: 题型:选择题
| A. | 与铝反应产生大量氢气的溶液:Na+、K+、CO32-、NO3- | |
| B. | 0.1mol•L-1的NaOH溶液:K+、Na+、SO42-、CO32- | |
| C. | 0.1mol•L-1FeCl3溶液:K+、NH4+、SO42-、SCN- | |
| D. | 使紫色石蕊试液变红的溶液:Ca2+、Na+、ClO-、NO3- |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 在标准状况下,22.4L SO3的分子数约为NA个 | |
| B. | 58.5g NaCl溶于1 L水中,所得溶液中溶质的物质的量浓度为1 mol/L | |
| C. | 常温、常压下,48g臭氧含有的氧原子数为3NA | |
| D. | 5.6g Fe与足量的盐酸反应失去的电子数为0.3NA |
查看答案和解析>>
科目: 来源: 题型:解答题
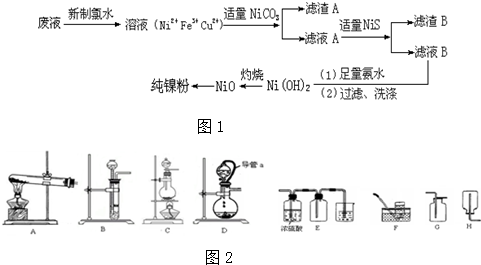
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | PM 2.5、二氧化碳都属于空气质量日报的内容 | |
| B. | 向煤中加入适量CaSO4,可大大减少燃烧产物中SO2的量 | |
| C. | 对“地沟油”进行分馏可得到汽油;玻璃、水泥和陶瓷都属于传统硅酸盐材料 | |
| D. | “光化学烟雾”、“硝酸型酸雨”的形成都与氮氧化台物有关 |
查看答案和解析>>
科目: 来源: 题型:解答题

查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:解答题
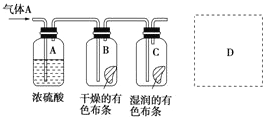
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 40mL | B. | 72mL | C. | 80mL | D. | 128mL |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 将浓硝酸保存在无色玻璃瓶中 | |
| B. | 金属钠和钾保存在煤油中 | |
| C. | Na2CO3可以保存在玻璃塞的玻璃瓶中 | |
| D. | NaOH固体放在滤纸上称量 |
查看答案和解析>>
科目: 来源: 题型:解答题
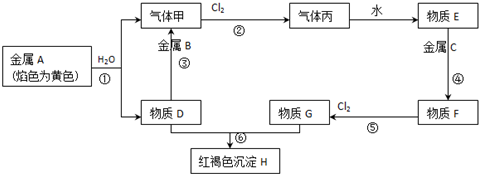
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com