
科目: 来源: 题型:解答题
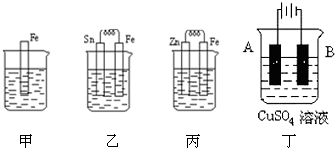
查看答案和解析>>
科目: 来源: 题型:解答题

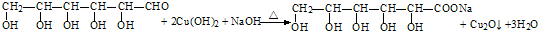
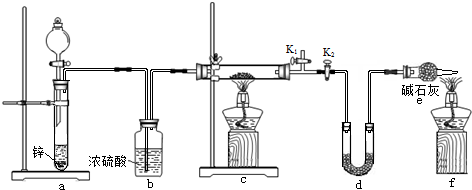
查看答案和解析>>
科目: 来源: 题型:解答题
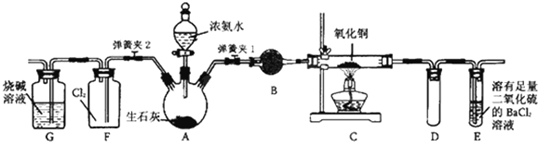
查看答案和解析>>
科目: 来源: 题型:解答题
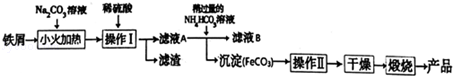
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 甘油可作护肤保湿剂 | |
| B. | 无水氯化钙可用作食品干燥剂 | |
| C. | 包装用材料聚乙烯和聚氯乙烯都属于烃 | |
| D. | 使用含钙离子浓度较大的地下水洗衣服,肥皂去污能力减弱 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 升高温度 | B. | 使用催化剂 | C. | 增大H2浓度 | D. | 减小压强 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 负极反应为:O2+2H2O+4e-═4OH- | |
| B. | 负极反应为:2H2+4OH--4e-═4H2O | |
| C. | 电池工作时溶液中的阴离子移向正极 | |
| D. | 电池工作时负极区pH升高,正极区pH下降 |
查看答案和解析>>
科目: 来源: 题型:解答题
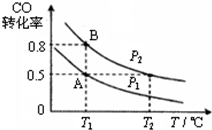 “C1化学”是指以碳单质或分子中含1个碳原子的物质(如CO、CO2、CH4、CH3OH等)为原料合成工业产品的化学工艺,对开发新能源和控制环境污染有重要意义.
“C1化学”是指以碳单质或分子中含1个碳原子的物质(如CO、CO2、CH4、CH3OH等)为原料合成工业产品的化学工艺,对开发新能源和控制环境污染有重要意义.| 容器 编号 | 温度(℃) | 起始的物质的量(mol) | 平衡的物质的量(mol) | |
| CH3OH(g) | CH3OCH3(g) | H2O(g) | ||
| I | 387 | 0.20 | 0.080 | 0.080 |
| Ⅱ | 387 | 0.40 | ||
| Ⅲ | 207 | 0.20 | 0.090 | 0.090 |
| 物质 | CO2 | H2 | CH3OH | H2O |
| 起始投料/mol | 1 | 3 | 2 | 0 |
查看答案和解析>>
科目: 来源: 题型:选择题

| A. | 气体W为氧气 | |
| B. | b极与电源的正极相连 | |
| C. | 离子交换膜c为阳离子交换膜 | |
| D. | a极的电极反应为SO2+2H2O-2e-=SO42-+4H+. |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com