
科目: 来源: 题型:选择题
| A. | NaCl溶液(CaCO3):加热 | B. | NaHCO3溶液(Na2CO3):加热 | ||
| C. | H2O(NaCl):蒸馏 | D. | 苯(水):萃取 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 空气中的二氧化硫超标 | B. | 空气中的氮氧化物超标 | ||
| C. | 空气中可吸入颗粒物超标 | D. | 空气中的二氧化碳超标 |
查看答案和解析>>
科目: 来源: 题型:解答题
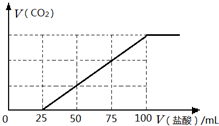 钠及其化合物在生产和生活中有广泛的应用.完成下列计算:
钠及其化合物在生产和生活中有广泛的应用.完成下列计算:| 氢氧化钠质量(g) | 氯化钠质量(g) | |
| ① | 2.40 | 3.51 |
| ② | 2.32 | 2.34 |
| ③ | 3.48 | 3.51 |
查看答案和解析>>
科目: 来源: 题型:解答题
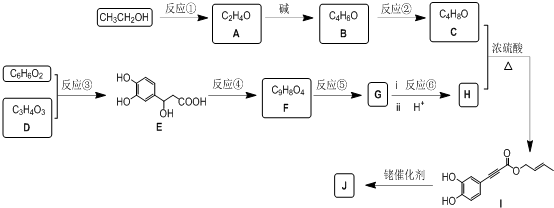
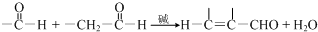
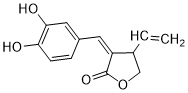
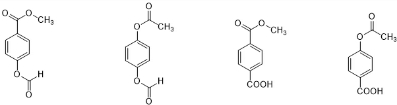 任意一种.
任意一种.查看答案和解析>>
科目: 来源: 题型:解答题
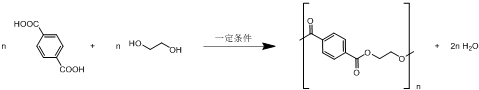 .
. .
.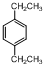 .
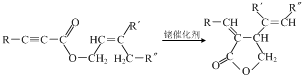
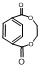
.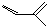 ,两分子该单体发生“Diels-Alder反应”,写出两种不同结构的产物
,两分子该单体发生“Diels-Alder反应”,写出两种不同结构的产物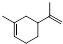 、
、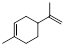 .
.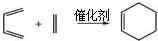
查看答案和解析>>
科目: 来源: 题型:解答题
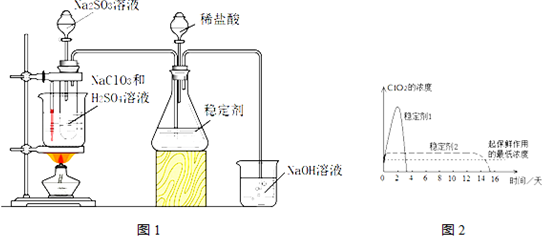
查看答案和解析>>
科目: 来源: 题型:解答题
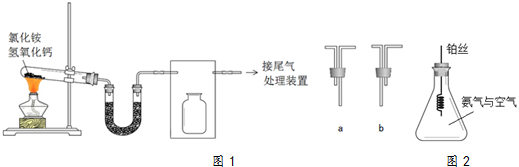
 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com