
科目: 来源: 题型:选择题
| A. | 除去苯中混有的少量苯酚:加入适量浓溴水,振荡、静置后过滤 | |
| B. | 实验室制备乙酸丁酯:水浴加热 | |
| C. | 分离乙酸乙酯和饱和碳酸钠溶液:分液 | |
| D. | 检验FeCl3溶液中是否含有Fe2+:取少量溶液先滴加氯水,再滴加KSCN溶液 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 分子式为C5H12的烷烃,含有3个甲基结构的同分异构体有2种 | |
| B. | 乙烷、乙醇、乙酸、苯、纤维素、油脂、蛋白质均能发生取代反应 | |
| C. | 甲烷、苯都属于烃,都不存在同分异构体 | |
| D. | 相同质量的甲烷和乙烷完全燃烧,乙烷耗氧量多 |
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:选择题
| A | B | C | D |
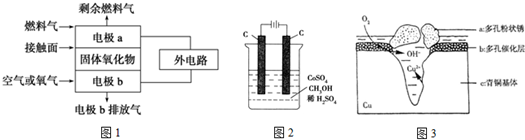
| 通电一段时间后,搅拌均匀,溶液的pH增大 | 甲电极上的电极反应为: 2Cl--2e-═Cl2↑ | Pt电极上的电极反应为: O2+2H2O+4e-═4OH- | 总反应的离子方程式为: 2Fe3++Cu═Cu2++2Fe2+ |
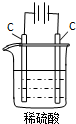 | 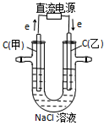 | 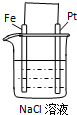 | 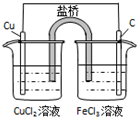 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目: 来源: 题型:多选题
| A. | 平衡向正反应方向移动 | B. | (a+b)<(c+d) | ||
| C. | Z的体积分数变小 | D. | X的转化率变大 |
查看答案和解析>>
科目: 来源: 题型:解答题

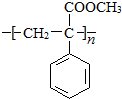 、
、 .
. +2NaOH$\stackrel{△}{→}$
+2NaOH$\stackrel{△}{→}$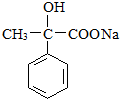 +NaBr+H2O.
+NaBr+H2O.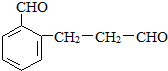 等.
等.查看答案和解析>>
科目: 来源: 题型:解答题

查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:选择题
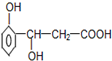 某有机物的结构简式如图所示,它可以发生反应的类型有( )
某有机物的结构简式如图所示,它可以发生反应的类型有( )| A. | ①②③④ | B. | ①②④⑤ | C. | ①②⑤⑥ | D. | ③④⑤⑥ |
查看答案和解析>>
科目: 来源: 题型:解答题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com