
科目: 来源: 题型:解答题
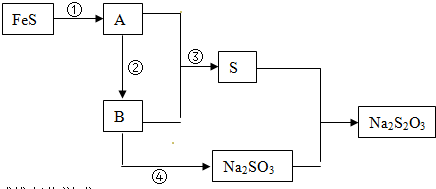
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 加入硝酸酸化了的硝酸钡溶液,有白色沉淀生成 | |
| B. | 加入盐酸酸化了的氯化钡溶液,有白色沉淀生成 | |
| C. | 先加硝酸酸化,无沉淀,再加硝酸钡溶液,有白色沉淀生成 | |
| D. | 先加盐酸酸化,无现象,再加氯化钡溶液,有白色沉淀生成 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | Na+ Cl- Mg2+ SO42- | B. | K+ Cu2+ I- SO42- | ||
| C. | NO3- K+ Cl- OH- | D. | Al3+ Na+ S2- Cl- |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | c(H+)随着温度升高而降低 | B. | 在35℃时,c(H+)>c(OH-) | ||
| C. | 蒸馏水中通HCl,Kw增大 | D. | 温度升高有利于水的电离 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | ABC | B. | CBA | C. | BCA | D. | BAC |
查看答案和解析>>
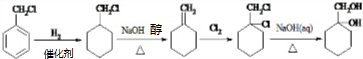
科目: 来源: 题型:解答题
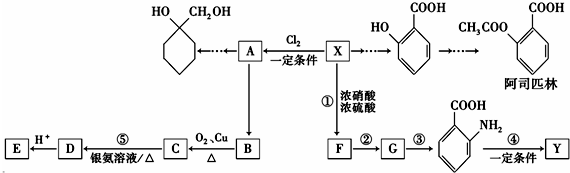

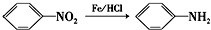 (苯胺,易被氧化)
(苯胺,易被氧化)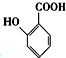 中官能团名称为酚羟基、羧基;
中官能团名称为酚羟基、羧基; ;
; $\stackrel{一定条件下}{→}$
$\stackrel{一定条件下}{→}$  +(n-1)H2O;
+(n-1)H2O; 的合成路线(无机试剂任用).合成路线流程图示例如下:CH3CH2OH$→_{170℃}^{浓硫酸}$H2C=CH2
的合成路线(无机试剂任用).合成路线流程图示例如下:CH3CH2OH$→_{170℃}^{浓硫酸}$H2C=CH2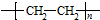
 .
.查看答案和解析>>
科目: 来源: 题型:解答题
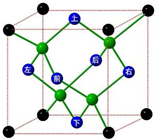 A、B、C、D、E、F六种元素的原子序数依次递增.已知:
A、B、C、D、E、F六种元素的原子序数依次递增.已知:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com