
科目: 来源: 题型:填空题

查看答案和解析>>
科目: 来源: 题型:解答题
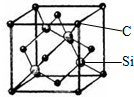 铜、镓、硒、硅等元素的化合物是生产第三代太阳能电池的重要材料.请回答:
铜、镓、硒、硅等元素的化合物是生产第三代太阳能电池的重要材料.请回答:查看答案和解析>>
科目: 来源: 题型:解答题
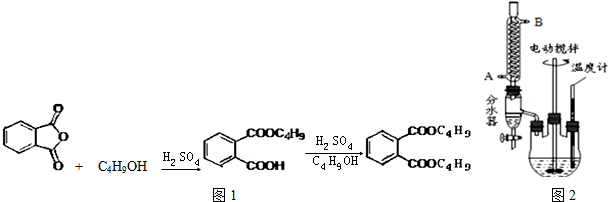
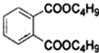 +2NaOH$\stackrel{△}{→}$
+2NaOH$\stackrel{△}{→}$ +2CH3CH2CH2CH2OH.
+2CH3CH2CH2CH2OH.查看答案和解析>>
科目: 来源: 题型:解答题
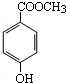 .
. ,其中包含的反应类型有取代反应或水解反应、中和反应.
,其中包含的反应类型有取代反应或水解反应、中和反应.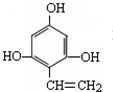 、
、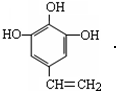 .
.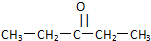
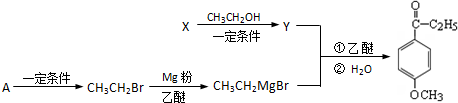
 .
.查看答案和解析>>
科目: 来源: 题型:解答题
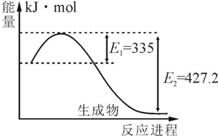 氮是地球上含量丰富的一种元素,氮及其化合物在工农业生产、生活中有着重要作用.请回答下列问题:
氮是地球上含量丰富的一种元素,氮及其化合物在工农业生产、生活中有着重要作用.请回答下列问题:| t/K | 298 | 398 | 498 | … |
| K/(mol•L-1)-2 | 4.1×106 | K1 | K2 | … |
查看答案和解析>>
科目: 来源: 题型:解答题
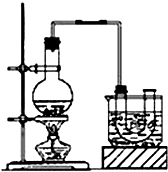 已知:CH3CH2OH+NaBr+H2SO4(浓)$\stackrel{△}{→}$ CH3CH2Br+NaHSO4+H2O.
已知:CH3CH2OH+NaBr+H2SO4(浓)$\stackrel{△}{→}$ CH3CH2Br+NaHSO4+H2O.查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:选择题
 将等物质的量浓度的CuSO4溶液和NaCl溶液等体积混合后,用石墨电极进行电解,电解中溶液pH随时间t变化的曲线如图,则下列说法正确的是( )
将等物质的量浓度的CuSO4溶液和NaCl溶液等体积混合后,用石墨电极进行电解,电解中溶液pH随时间t变化的曲线如图,则下列说法正确的是( )| A. | 阳极产物一定是Cl2,阴极产物一定是Cu | |
| B. | BC段表示在阴极上是H+放电产生了H2 | |
| C. | CD段表示电解水 | |
| D. | CD段表示阳极上OH-放电破坏了水的电离平衡,产生了H+ |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 淀粉和纤维素的化学式相同,两者互为同分异构体 | |
| B. | 苯能和氢气发生加成反应,是由于其结构中有碳碳双键 | |
| C. | 紫外线杀菌是在紫外线条件下,蛋白质发生盐析杀死细菌 | |
| D. | 乙醇和乙酸都能与金属钠反应放出氢气 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | NaClO 溶液中通入过量SO2 ClO -+SO2+H2O═HClO+HSO3- | |
| B. | 甲醇、氧气和氢氧化钾溶液组成的燃料电池的负极反应CH3OH+H2O-6e-═CO2↑+6H+ | |
| C. | AlCl3 溶液中投入过量Na:Al3++4Na+2H2O═AlO2 -+4Na++2H2↑ | |
| D. | 向明矾溶液中滴加Ba(OH)2,恰好使SO42- 沉淀完全:2Al3++3SO4 2-+3Ba2++6OH -═2Al(OH)3↓+3BaSO4↓ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com