
科目: 来源: 题型:选择题
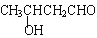
| A. | ①③④ | B. | ②④⑤ | C. | ①③⑤ | D. | ①②⑤ |
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:解答题

查看答案和解析>>
科目: 来源: 题型:解答题
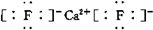 ;若 XY2其结构式为:S=C=S.为共价化合物时,
;若 XY2其结构式为:S=C=S.为共价化合物时,查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 锌粒与稀 HNO3反应制备 H2 | B. | 加热分解 NH4Cl 固体制 NH3 | ||
| C. | 大理石与稀 H2SO4反应制备 CO2 | D. | 亚硫酸钠与浓 H2SO4反应制备 SO2 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 元素 Y的单质与氢氧化钠溶液或盐酸反应均有氢气生成 | |
| B. | 元素 X与 W形成的共价化合物有很多种 | |
| C. | 元素 W、X的氯化物中,各原子均满足 8 电子的稳定结构 | |
| D. | 元素 Z 可与元素 X 形成共价化合物 XZ2 |
查看答案和解析>>
科目: 来源: 题型:多选题
| A. | 它是一种共价化合物 | |
| B. | 在加热时此化合物可以分解为 PH3和 HI 或 H2和 I2 | |
| C. | 这种化合物能跟碱反应 | |
| D. | 该化合物可以由 PH3 和 HI 化合而成 |
查看答案和解析>>
科目: 来源: 题型:选择题
| 温度/℃ | 起始物成质的量/mol | 平衡物质的两/mol | |||
| 容器编马 | CO | Cl2 | COCl2 | COCl2 | |
| Ⅰ | 500 | 1.0 | 1.0 | 0 | 0.8 |
| Ⅱ | 500 | 1.0 | a | 0 | 0.5 |
| Ⅲ | 600 | 0.5 | 0.5 | 0.5 | 07 |
| A. | 容器I中前5min的平均反应速率v(CO)=0.16mol•L-1•min-1 | |
| B. | 该反应正反应为吸热反应 | |
| C. | 容器Ⅱ中起始时Cl2的物质的量为0.55mol | |
| D. | 若起始时向容器I加入CO0.8mol,Cl20.8mol,达到平衡时CO转化率大于80%. |
查看答案和解析>>
科目: 来源: 题型:解答题
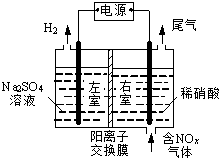 电解法处理含氮氧化物废气,可回收硝酸,具有较高的环境效益和经济效益.实验室模拟电解法吸收NOx的装置如图所示(图中电极均为石墨电极).
电解法处理含氮氧化物废气,可回收硝酸,具有较高的环境效益和经济效益.实验室模拟电解法吸收NOx的装置如图所示(图中电极均为石墨电极).查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 向Ag(NH3)2NO3溶液中加人盐酸:Ag(NH3)++2H+═Ag++2NH4+ | |
| B. | 向 Na202 中加人足量水:2Na202+2H20═4Na++40H-+02↑ | |
| C. | 向Al2(SO4)3溶液中加入过量氨水:Al3++30H-═Al(0H)3↓ | |
| D. | 向 Ca(HC03)2溶液中加入澄淸石灰水:Ca2++2HC03-+20H-═CaC03↓+C032-+2H20 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com