
科目: 来源: 题型:选择题
| A. | 用物质A表示的反应的平均速率为0.6 mol•(L•s)-1 | |
| B. | 2 s时物质B的浓度为1.4 mol•L-1 | |
| C. | 2 s时物质A的转化率为70% | |
| D. | 2 s时物质A的体积分数为$\frac{14}{27}$ |
查看答案和解析>>
科目: 来源: 题型:解答题
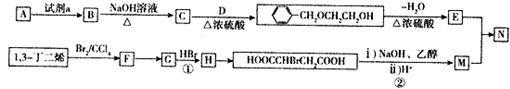
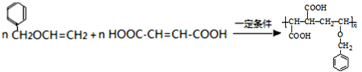 .
.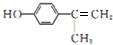 .
.查看答案和解析>>
科目: 来源: 题型:解答题
 )中六元钚结构与苯环类似,它与硝基苯的相对分子质量之差为3,其熔点为354℃,硝基苯的熔点是5.7℃.
)中六元钚结构与苯环类似,它与硝基苯的相对分子质量之差为3,其熔点为354℃,硝基苯的熔点是5.7℃.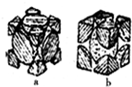
查看答案和解析>>
科目: 来源: 题型:解答题
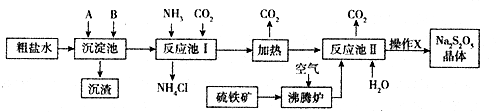
查看答案和解析>>
科目: 来源: 题型:解答题
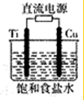 铜是人类最早利用的金属之一,铜能形成多种重要的化合物.
铜是人类最早利用的金属之一,铜能形成多种重要的化合物.查看答案和解析>>
科目: 来源: 题型:解答题
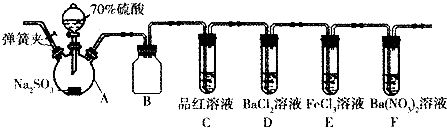
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 加水稀释后,溶液中$\frac{c(O{H}^{-})}{c(Cl{O}^{-})}$增大 | |
| B. | 溶液中c(ClO-)>c(HClO)>c(OH-)>c(H+) | |
| C. | 溶液中2c(Ca2+)+c(H+)=c(ClO-)+c(OH-) | |
| D. | 若溶液的pH=l2,则c(ClO-)的水解百分率约为9.1% |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 室温下,测得0.1 mol/L 的氨水的pH为11:NH3•H2O?NH4++OH- | |
| B. | 酸性介质中KMnO4氧化H2O2:2MnO4-+5H2O2+6H+═2Mn2++5O2↑+8H2O | |
| C. | 向 NaAlO2溶液中通入过量CO2 制 Al(OH)3:CO2+AlO2-+2H20=HC03-+Al(OH)3↓ | |
| D. | 铅酸蓄电池在充电时的正极反应:PbO2+4H++SO42-+2e-═PbSO4+2H2O |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | Z的氢化物稳定性可能较差 | B. | Q、P中均含有非极性键 | ||
| C. | 对应单质失去电子的能力:W>Y>Z | D. | 单质熔点:Y>X>W |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 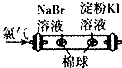 比较Cl2、Br2、I2的氧化性相对强弱 | B. | 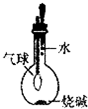 探究烧缄溶解时的热效应 | ||
| C. | 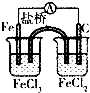 将化学能转化为电能 | D. |  配制一定物质的量浓度的溶液 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com