
科目: 来源: 题型:解答题

查看答案和解析>>
科目: 来源: 题型:解答题
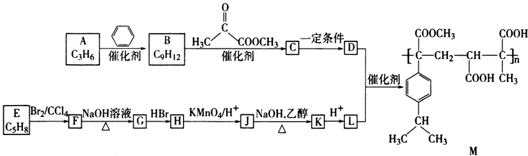
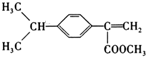 、
、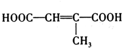 (写结构简式).
(写结构简式).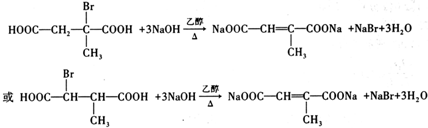 .
.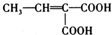 (写结构简式).
(写结构简式).查看答案和解析>>
科目: 来源:2016-2017学年重庆市高一上10月月考化学试卷(解析版) 题型:选择题
将15mL 2mol/LNa2CO3溶液逐滴加入到40mL 1.5mol/LMCln盐溶液中,恰好将溶液中的Mn+完全沉淀为碳酸盐,则MCln中n值是()
A.4 B.3 C.2 D.l
查看答案和解析>>
科目: 来源:2016-2017学年重庆市高一上10月月考化学试卷(解析版) 题型:实验题
高纯氧化锌广泛应用于电子工业,某研究小组设计如下流程制备高纯氧化锌。
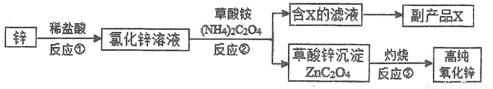
(1)反应①的化学方程式为___________________。
(2)反应②的基本反应类型是_____________。
(3)副产品X的化学式为:______________。从含X的滤液中获取固体X的实验操作步骤是:___________、____________、过滤。
(4)反应③属于分解反应,除得到氧化锌外还生成2种常见气体,其化学式为_________、________。
(5)若用纯度为97.5%的1kg粗锌制备高纯氧化锌,理论上最多可生产出氧化锌的物质的量为:_________mol。
查看答案和解析>>
科目: 来源: 题型:解答题
 A、B、C、D、E、F为前四周期元素,它们的原子序数依次增大.A、C的基态原子的电子排布中L能层都有两个未成对电子,C、D同主族,E的基态原子的电子排布中有4个未成对电子,F原子除最外能层只有1个电子外,其余各能层均为全充满.
A、B、C、D、E、F为前四周期元素,它们的原子序数依次增大.A、C的基态原子的电子排布中L能层都有两个未成对电子,C、D同主族,E的基态原子的电子排布中有4个未成对电子,F原子除最外能层只有1个电子外,其余各能层均为全充满. .
. .DAB-的水溶液可以用于实验室中E3+离子的定性检验,形成配合物的颜色为血红色.
.DAB-的水溶液可以用于实验室中E3+离子的定性检验,形成配合物的颜色为血红色.查看答案和解析>>
科目: 来源: 题型:解答题
| 化学键 | O=O | C-O | O-H | C-H |
| 键能(kJ•mol-1) | 498 | 351 | 465 | 413 |
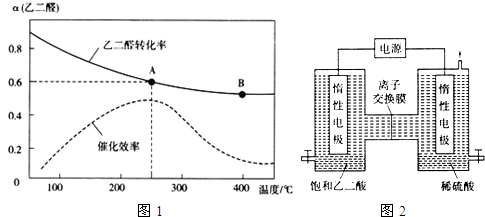
查看答案和解析>>
科目: 来源: 题型:选择题
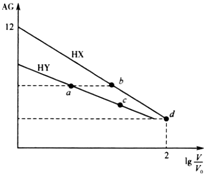 常温下,浓度均为0.10mol•L-1、体积均为V0的HX和HY溶液,分别加水稀释至体积V,AG[AG=$\frac{c({H}^{+})}{c(O{H}^{-})}$]随1g$\frac{V}{{V}_{0}}$的变化如图所示.下列叙述正确的是( )
常温下,浓度均为0.10mol•L-1、体积均为V0的HX和HY溶液,分别加水稀释至体积V,AG[AG=$\frac{c({H}^{+})}{c(O{H}^{-})}$]随1g$\frac{V}{{V}_{0}}$的变化如图所示.下列叙述正确的是( )| A. | a、b溶液中导电离子数目相等 | |
| B. | 水的电离程度:a<b<c | |
| C. | d点所示溶液的AG=8 | |
| D. | 与等浓度的NaOH溶液中和时,c点消耗NaOH溶液的体积大于a点 |
查看答案和解析>>
科目: 来源:2016-2017学年重庆市高一上10月月考化学试卷(解析版) 题型:实验题
实验室里需用纯净的KCl固体,但目前只有含K2SO4、(NH4)2CO3杂质的KCl。某学生设计了如图所示方案进行提纯。
已知:1.(NH4)2CO3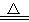 2NH3↑+CO2↑+H2O
2NH3↑+CO2↑+H2O
2.K2SO4、KCl热稳定性好,KCl溶解度随温度变化不大;
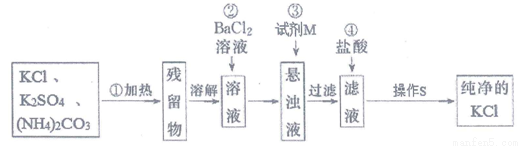
根据以上信息,回答下列问题:
(1)步骤①加热的目的是:______________;此操作可选择在______________(填仪器名称)中进行;
(2)步骤②不用硝酸钡溶液,其理由是_________________;
(3)进行步骤②时,简述判断SO42-是否除尽的实验操作、现象和结论:____________;
(4)步骤③所加试剂M为:_______________,其目的是_________________;
(5)操作S的名称是__________________。
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 1.8g H218O中含有的中子数为NA | |
| B. | 1mol Fe与足量的浓硫酸反应,生成SO2的分子数为NA | |
| C. | 7.1g Cl2溶于水所得溶液中含有的Cl-数目为0.1NA | |
| D. | 丙烷燃料电池负极消耗2.24L(标准状况)气体时,电路中转移电子数为2NA |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 朴硝和消石加强热都不分解 | |
| B. | 朴硝和消石都属于强电解质 | |
| C. | 朴硝和消石都既含有离子键又含有共价键 | |
| D. | “紫青烟起”是由于消石中的K+在火焰上灼烧时呈现出特殊颜色 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com