
科目: 来源: 题型:选择题
| A. | 氨气具有还原性,可用于检查HCl泄漏 | |
| B. | 浓硫酸具有吸水性,可用于干燥CO2 | |
| C. | 铝具有高熔点,可用于生产耐火砖 | |
| D. | 硅有导电性,可用作光导纤维 |
查看答案和解析>>
科目: 来源: 题型:解答题
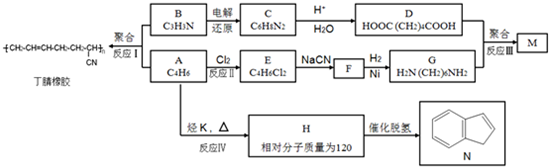
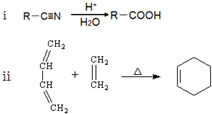
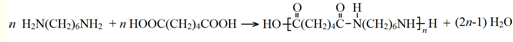 .
.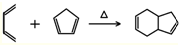 .
.查看答案和解析>>
科目: 来源: 题型:解答题
| 实验装置 | 电解质溶液 | 实验现象 | |
 | 5mol/L NaCl溶液 | a极附近 | b极附近 |
| 开始时,产生白色浑浊并逐渐增加,当沉入U形管底部时部分沉淀变为橙黄色;随后a极附近沉淀自下而上也变为橙黄色 | 产生无色气泡 | ||
| ①氯化亚铜(CuCl)为白色粉末,微溶于水; ②氢氧化亚铜(CuOH)为黄色不溶于水的固体,易脱水分解为红色的Cu2O; ③Cu+水溶液中不稳定,酸性条件下易歧化为Cu2+和Cu; ④氢氧化铜可以溶于浓NaOH得到蓝色溶液. |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 硫的非金属性比碳强 | |
| B. | SO2气体依次通过NaHCO3溶液、澄清石灰水,澄清石灰水变浑浊 | |
| C. | SO2和CO2气体分别通入水中至饱和,测定两溶液的pH,前者小于后者 | |
| D. | 室温下测定均为0.1mol/L的NaHSO3和NaHCO3溶液的pH,前者小于后者 |
查看答案和解析>>
科目: 来源: 题型:选择题
| 选项 | 实验操作 | 现象 | 解释 |
| A | 向AlCl3溶液中逐滴加入NaOH溶液并振荡 | 产生白色沉淀,后沉淀逐渐溶解 | 铝元素具有一定的非金属性 |
| B | 将Fe(NO3)2固体溶于稀硫酸,滴加KSCN溶液 | 溶液变红 | 稀硫酸将Fe2+氧化为Fe3+ |
| C | 向KBrO3溶液中加入少量CCl4,然后通入少量Cl2,充分振荡,静置 | 下层呈橙色 | 氧化性:Cl2>Br2 |
| D | 将充有NO2的玻璃球放入热水中 | 红棕色加深 | 2NO2?N2O4△H>0 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 开发氢能替代化石燃料 | |
| B. | 工业含氮废水经处理达标后排放 | |
| C. | 农作物秸秆等露天焚烧制肥料 | |
| D. | 金属、塑料、玻璃、纸类等制品应分类回收处理 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 麦芽糖和蔗糖的水解产物相同 | |
| B. | 用新制的氢氧化铜可区分乙醇、乙醛 | |
| C. | 用高锰酸钾酸性溶液可以区分苯、甲苯 | |
| D. | 用饱和溴水可区分苯酚溶液、己烷、1-己烯 |
查看答案和解析>>
科目: 来源: 题型:选择题
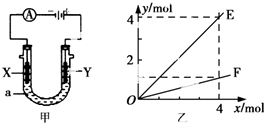
| A. | 若此装置用于电解精炼铜,则X为纯铜、Y为粗铜,电解的溶液a可以是硫酸铜或氯化铜溶液 | |
| B. | 按图甲装置用惰性电极电解AgN03溶液,若图乙横坐标x表示流入电极的电子的物质的量,则E可表示反应生成硝酸的物质的量,F表示电解生成气体的物质的量 | |
| C. | 按图甲装置用惰性电极电解一定浓度的硫酸铜溶液,通电一段时间后,加入0.5mol的碳酸铜刚好恢复到通电前的浓度和pH,则电解过程中转移的电子为2.0 mol | |
| D. | 若X、Y为铂电极.a溶液为500 mL KCl和KNO3的混合液,经过一段时间后,两极均得到标准状况下11.2 L气体,则原混合液中KCl的物质的量浓度至少为2.0 molL-1 |
查看答案和解析>>
科目: 来源: 题型:解答题
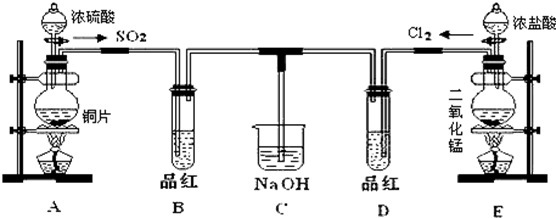

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com