
科目: 来源: 题型:选择题
| A. | 分子中3个碳原子在同一直线上 | |
| B. | 分子中所有原子都在同一平面上 | |
| C. | 分子中共价键的夹角为120° | |
| D. | 分子中共价键数为8,其中有一个碳碳双键 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 向NaClO溶液中通入过量SO2:ClO-+SO2+H2O═HClO+HSO3- | |
| B. | 向AlCl3溶液中投入过量Na:Al3++4Na+2H2O═AlO2-+4Na++2H2↑ | |
| C. | 向FeBr2溶液中通入少量Cl2:2Fe2++4Br-+3Cl2═2Fe3++2Br2+6Cl- | |
| D. | 向明矾溶液中滴加Ba(OH)2溶液,恰好使SO42-完全沉淀:2Al3++3SO42-+3Ba2++6OH-═2Al(OH)3↓+3BaSO4 |
查看答案和解析>>
科目: 来源: 题型:选择题
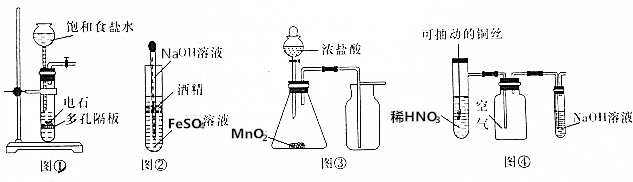
| A. | 用图①所示装置制取少量纯净的乙烯气体 | |
| B. | 用图②所示装置制备Fe(OH)2并能保持长时间观察到白色 | |
| C. | 用图③所示装置制取并收集干燥纯净的Cl2 | |
| D. | 用图④所示装置制取NO并验证其性质 |
查看答案和解析>>
科目: 来源: 题型:选择题
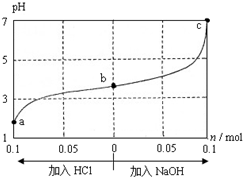 25℃时,将1.0L w mol•L-1 CH3COOH溶液与0.1mol NaOH固体混合,充分反应后向混合液中通(加)入HCl气体或NaOH固体,溶液pH随加入HCl或NaOH的物质的量而变化如图.下列叙述正确的是( )
25℃时,将1.0L w mol•L-1 CH3COOH溶液与0.1mol NaOH固体混合,充分反应后向混合液中通(加)入HCl气体或NaOH固体,溶液pH随加入HCl或NaOH的物质的量而变化如图.下列叙述正确的是( )| A. | a、b、c 对应的混合液中,水的电离程度由大到小的顺序的是a>b>c | |
| B. | c点混合液中c(Na+)>c(CH3COO-) | |
| C. | a、b、c三点都有c(CH3COO-)+c(OH-)=c(Na+)+c(H+) | |
| D. | 若忽略体积变化,则25℃时CH3COOH的电离平衡常数 K=$\frac{0.2}{w-0.2}$×10-7 mol•L-1 |
查看答案和解析>>
科目: 来源: 题型:选择题
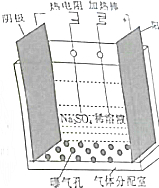
 碱性硼化钒(VB2)-空气电池工作时反应为:4VB2+11O2═4B2O3+2V2O5.用该电池为电源,选用惰性电极电解硫酸铜溶液,实验装置如图所示.当外电路中通过0.04mol电子时,B装置内共收集到0.448L气体(标准状况),则下列说法正确的是( )
碱性硼化钒(VB2)-空气电池工作时反应为:4VB2+11O2═4B2O3+2V2O5.用该电池为电源,选用惰性电极电解硫酸铜溶液,实验装置如图所示.当外电路中通过0.04mol电子时,B装置内共收集到0.448L气体(标准状况),则下列说法正确的是( )| A. | 电解过程中,c电极表面先有红色物质析出,然后有气泡产生 | |
| B. | VB2电极发生的电极反应为:2VB2+11H2O-22e-═V2O5+2B2O3+22H+ | |
| C. | A装置中K+移向VB2电极 | |
| D. | b装置内收集的0.448L气体(标准状况)全部为O2 |
查看答案和解析>>
科目: 来源: 题型:解答题
| 化学键 | H-Cl | Cl-Cl | H-H | C-H | C-Cl |
| 键能/(kJ•mol-1) | 431.4 | 242.1 | 435.9 | 413.0 | 338.9 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 相等 | B. | 前者大于后者 | C. | 后者大于前者 | D. | 无法判断 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | Cu(0H)2溶于氨水:Cu(0H)2+4NH3=[Cu(NH3)4]2++20H- | |
| B. | 足量的SO2通入Ca(C10)2溶液:Ca2++2C10-+S02═CaS04↓+2C1- | |
| C. | H2S04溶液与Ba(0H)2溶液反应:Ba2++0H-+H++S0${\;}_{4}^{2-}$═BaSO4↓+H20 | |
| D. | NaHC03溶液与过量澄清石灰水反应:2HC0${\;}_{3}^{-}$+Ca2++20H-═CaC03↓+CO${\;}_{3}^{2-}$+2H20 |
查看答案和解析>>
科目: 来源: 题型:解答题
 香叶醇是合成玫瑰精油的主要原料,其结构简式如下:
香叶醇是合成玫瑰精油的主要原料,其结构简式如下:查看答案和解析>>
科目: 来源: 题型:解答题
 过氧化氢是实验室常用的试剂,在医疗、军事及工业上用途也非常广泛.回答下列问题:
过氧化氢是实验室常用的试剂,在医疗、军事及工业上用途也非常广泛.回答下列问题:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com