
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:选择题
 已知溶液中:氧化性IO3->I2>SO32-.向含3mol NaHSO3的溶液中逐滴加入KIO3溶液,加入的KIO3和析出的I2的物质的量的关系曲线如图所示,下列说法正确的是( )
已知溶液中:氧化性IO3->I2>SO32-.向含3mol NaHSO3的溶液中逐滴加入KIO3溶液,加入的KIO3和析出的I2的物质的量的关系曲线如图所示,下列说法正确的是( )| A. | a点反应的还原剂是NaHSO3,被氧化的元素是碘元素 | |
| B. | b点反应的离子方程式是:3HSO3-+IO3-+3OH-═3SO42-+I-+3H2O | |
| C. | c点到d点的反应中共转移0.6mol电子 | |
| D. | 往200mL 1 mol/L的KIO3溶液中滴加NaHSO3溶液,反应开始时的离子方程式是:5HSO3-+2IO3-═I2+5SO42-+3H++H2O |
查看答案和解析>>
科目: 来源: 题型:选择题
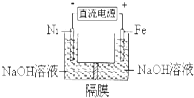
| A. | 铁是阳极,电极反应为Fe-6e-+4H2O═FeO42-+8H+ | |
| B. | 若隔膜为阴离子交换膜,则OH-自左向右移动 | |
| C. | 电解时电子的流动方向为:负极→Ni电极→溶液→Fe电极→正极 | |
| D. | 每制得1mol Na2FeO4,理论上可以产生67.2L气体 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 氯气和水发生反应:Cl2+H2O?2H++Cl-+ClO- | |
| B. | 金属钠和水反应:Na+2H2O═Na++2OH-+H2↑ | |
| C. | 用氢氧化钠除去铝表面的氧化膜时产生气泡的反应2Al+2OH-+6H2O═2[Al(OH)4]-+3H2↑ | |
| D. | 将金属铁加入稀硫酸和硝酸钾混合溶液中,金属溶解:Fe+2H+═Fe2++H2↑ |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 某气体能使品红溶液褪色,则该气体是SO2 | |
| B. | 向无色溶液中加入氯水后振荡,再加入CCl4振荡,下层显示紫红色,则原溶液中有I- | |
| C. | 向某溶液中加入硝酸酸化Ba(NO3)2溶液,产生白色沉淀,则原溶液中有SO42- | |
| D. | 向某溶液中加入NaOH,产生可使湿润的蓝色石蕊试纸变红的气体,则原溶液中有NH4+ |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 1 mol-OH中含有10 NA个电子 | |
| B. | 1 L 1 mol•L-1CH3COONa溶液中含有NA个CH3COO- | |
| C. | 28g晶体硅中含有共价键数目为2NA个 | |
| D. | 常温常压下11.2 L甲烷气体含有的分子数为0.5NA |
查看答案和解析>>
科目: 来源: 题型:解答题
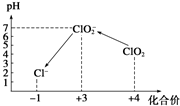
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 热空气能吹出溴是利用溴易挥发的性质 | |
| B. | SO2吸收溴的反应方程式:SO2+2H2O+Br2→H2SO4+2HBr | |
| C. | 流程中循环利用的物质有SO2、Br2、Cl2等多种 | |
| D. | 没有采用直接蒸馏含溴海水得到单质溴的主要原因是为了节能 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | pH=1的溶液:Fe2+、Ca2+、I-、Br- | |
| B. | Ag+、I-、K+、NO3- | |
| C. | 0.1mol/L 的KNO3溶液:H+、Fe2+、Cl-、SO42- | |
| D. | 与铝反应产生大量氢气的溶液:K+、Na+、[Al(OH)4]-、NO3- |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 向Ba(OH)2溶液中,逐滴加入NaHSO4溶液至恰好完全沉淀H++SO42-+Ba2++OH-═BaSO4↓+H2O | |
| B. | 用NaOH吸收少量二氧化硫 OH-+SO2═HSO3- | |
| C. | 氯化铝溶液中加过量氨水Al3++3NH3.H2O═Al(OH)3↓+3 NH4+ | |
| D. | 次氯酸钙溶液中通入过量二氧化碳 ClO-+H2O+CO2═HCO3-+HClO |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com