
科目: 来源: 题型:解答题
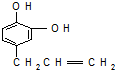

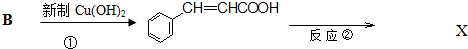
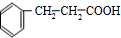 .反应①的化学方程式为:
.反应①的化学方程式为: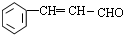 +2Cu(OH)2$\stackrel{△}{→}$
+2Cu(OH)2$\stackrel{△}{→}$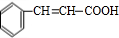 +Cu2O+2H2O.
+Cu2O+2H2O.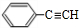 $→_{催化剂}^{HCl}$
$→_{催化剂}^{HCl}$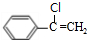 $→_{一定条件}^{CO、H_{2}}$
$→_{一定条件}^{CO、H_{2}}$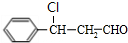 $→_{△}^{NaOH/醇}$
$→_{△}^{NaOH/醇}$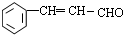 .
.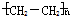
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 同时增大 | B. | v1减小,v2增大 | C. | 同时减小 | D. | v1增大,v2减小 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | NaH的电子式为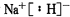 | |
| B. | NaH与H2O反应时水作氧化剂 | |
| C. | NaH中氢元素的离子半径小于Li+的离子半径 | |
| D. | H+与H-的核外电子排布不相同 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 等物质的量的硫蒸气和硫固体分别完全燃烧,后者放出的热量少 | |
| B. | 由单质A转化为单质B时△H=+119 kJ•mol-1可知单质B比单质A稳定 | |
| C. | 稀溶液中:H+(aq)+OH-(aq)═H2O(l)△H=-57.3 kJ•mol-1,若将含0.5 mol H2SO4的浓硫酸与含1 mol NaOH的溶液混合,放出的热量小于57.3 kJ | |
| D. | 在101 kPa时,H2燃烧的热化学方程式为2H2(g)+O2(g)═2H2O(l)△H=-571.6 kJ•mol-1,则H2在101 kPa时的燃烧热为571.6 kJ•mol-1 |
查看答案和解析>>
科目: 来源: 题型:解答题

| 氢氧化物 | Al(OH)3 | Fe(OH)3 | Fe(OH)2 | Cu(OH)2 | Pb(OH)2 | Mn(OH)2 |
| 开始沉淀的pH | 3.3 | 1.5 | 6.5 | 4.2 | 8.0 | 8.3 |
| 沉淀完全的pH | 5.2 | 3.7 | 9.7 | 6.7 | 8.8 | 9.8 |
查看答案和解析>>
科目: 来源: 题型:解答题
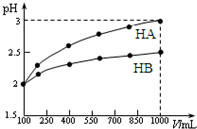 已知100mL pH=2的两种一元酸HA和HB,稀释过程中pH与溶液体积的关系如图所示.
已知100mL pH=2的两种一元酸HA和HB,稀释过程中pH与溶液体积的关系如图所示.查看答案和解析>>
科目: 来源: 题型:选择题
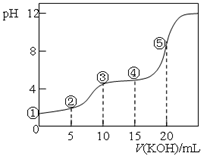 常温下,用0.10mol•L-1 KOH溶液滴定 10.00mL 0.10mol•L-1H2C2O4(二元弱酸)溶液 所得滴定曲线如图(混合溶液的体积可看成混合前溶液的体积之和).下列说法正确的是( )
常温下,用0.10mol•L-1 KOH溶液滴定 10.00mL 0.10mol•L-1H2C2O4(二元弱酸)溶液 所得滴定曲线如图(混合溶液的体积可看成混合前溶液的体积之和).下列说法正确的是( )| A. | 点①所示溶液中:c(H+)/c(OH-)=1012 | |
| B. | 点②所示溶液中:c(K+)+c(H+)=c(HC2O4-)+c(C2O42-)+c(OH-) | |
| C. | 点③所示溶液中:c(H2C2O4)+c(HC2O4-)+c(C2O42-)=0.05mol•L-1 | |
| D. | 点⑤所示溶液中:c(K+)>c(HC2O4-)>c(C2O42-)>c(OH-)>c(H+) |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 元素X 的简单气态氢化物的热稳定性比W 的弱 | |
| B. | 原子半径的大小顺序:rY>rZ>rW>rX | |
| C. | 化合物YX、ZX2、WX3 中化学键的类型相同 | |
| D. | 最高价氧化物对应水化物的酸性:W比Z 的弱 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 原子序数为7 | B. | 周期表中第一电离能最小 | ||
| C. | 周期表中原子半径最大 | D. | 周期表中电负性最大 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | c(H+)=10-12 mol•L-1的溶液:K+、Ba2+、Cl-、Br- | |
| B. | 使紫色石蕊试液变红的溶液:Na+、Mg2+、NO3-、ClO- | |
| C. | 使酚酞试液变红的溶液:Na+、Cl-、SO42-、Fe3+ | |
| D. | 碳酸氢钠溶液:K+、SO42-、Cl-、H+ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com