
科目: 来源: 题型:选择题
| A. | 丙烯与环丁烷互为同系物 | |
| B. | 碳氢化合物中的化学键都是极性键 | |
| C. | 乙醇与金属钠反应时,乙醇分子中的C-H键断裂 | |
| D. | 苯不能使溴的四氯化碳溶液褪色,说明苯分子中没有与乙烯分子中类似的碳碳双键 |
查看答案和解析>>
科目: 来源: 题型:多选题
| A. | 得到沉淀的物质的量最大 | B. | 得到沉淀的质量最大 | ||
| C. | 反应后溶液仍含有Al3+ | D. | 反应后溶液仍含有AlO2- |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 混合碳酸氢钙与氢氧化钠溶液 | B. | 混合硫酸铝与氢氧化钠溶液 | ||
| C. | 混合浓氨水和硫酸铝溶液 | D. | 混合盐酸和硝酸银溶液 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 分液漏斗使用前要检验它是否漏水 | |
| B. | 萃取剂要求不溶于水,且比水更容易使碘溶解,用家里的植物油也行 | |
| C. | 注入碘水和莽取剂,倒转分液漏斗反复用力振荡后要立即分液 | |
| D. | 分液时打开旋塞使下层液体流出,上层液体从上口倒出 |
查看答案和解析>>
科目: 来源: 题型:多选题
| A. | 10℃时pH=12的Na0H溶液与40℃时pH=12的Na0H溶液中:c(OH-)相等 | |
| B. | 25℃时pH=10的NaOH溶液与pH=10的氨水中:c(Na+)═c(NH4+) | |
| C. | 物质的量浓度相等的CH3COOH和CH3COONa溶液等体积混合:c(CH3COO-)+2c(OH-)═2c(H+)+c(CH3COOH) | |
| D. | 向10mLpH=12的Na0H溶液中滴加pH=2的HA溶液达中性:则混合液体积V总≥20mL |
查看答案和解析>>
科目: 来源: 题型:推断题
 ;
;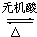 CH3COOH+(CH3)2CHOH.
CH3COOH+(CH3)2CHOH.查看答案和解析>>
科目: 来源: 题型:实验题

查看答案和解析>>
科目: 来源: 题型:填空题
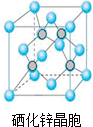 硒(Se)是一种有抗癌、抗氧化作用的元素,可以形成多种化合物.
硒(Se)是一种有抗癌、抗氧化作用的元素,可以形成多种化合物.查看答案和解析>>
科目: 来源: 题型:解答题
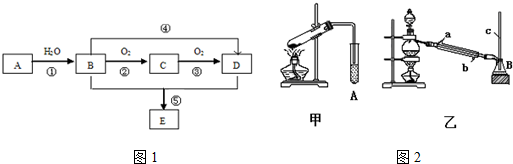
查看答案和解析>>
科目: 来源: 题型:解答题
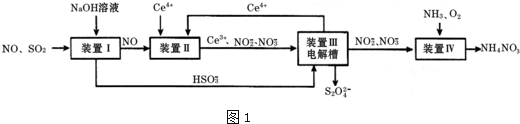
| n(SO32-):n(HSO3-) | 91:9 | 1:1 | 9:91 |
| pH | 8.2 | 7.2 | 6.2 |

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com