
科目: 来源: 题型:选择题
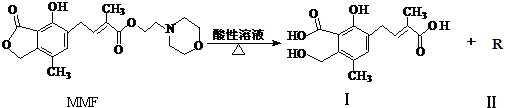
| A. | MMF分子中含有三种官能团 | |
| B. | 可以用NaHCO3溶液区别MMF与化合物Ⅰ | |
| C. | 化合物Ⅱ分子中只含碳、氢元素,属于烃类 | |
| D. | 1 mol MMF与足量NaOH 溶液共热,最多可消耗4 mol NaOH |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 实验室制乙烯:CH3CH2OH$→_{170℃}^{浓H_{2}SO_{4}}$ CH2=CH2↑+H2O | |
| B. | 苯酚钠溶液通入少量CO2:2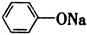 +CO2+H2O→2 +CO2+H2O→2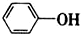 +Na2CO3 +Na2CO3 | |
| C. | 乙酸苯酚酯在足量的NaOH溶液中水解: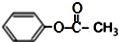 +NaOH→CH3COONa+ +NaOH→CH3COONa+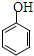 | |
| D. | 工业制聚乙烯:nCH2=CH2 $\stackrel{催化剂}{→}$ |
查看答案和解析>>
科目: 来源: 题型:选择题
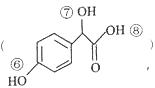 的说法正确的是( )
的说法正确的是( )| A. | Y 既能使溴水褪色又能使酸性高锰酸钾褪色,且原理相同 | |
| B. | Y 的同分异构体中,不存在苯环上的一氯代物只有一种的物质 | |
| C. | 1molY 与氢氧化钠溶液反应时,最多消耗 3mol 氢氧化钠 | |
| D. | Y 中⑥、⑦、⑧三处-OH 的电离程度由大到小的顺序是⑧>⑥>⑦ |
查看答案和解析>>
科目: 来源: 题型:推断题
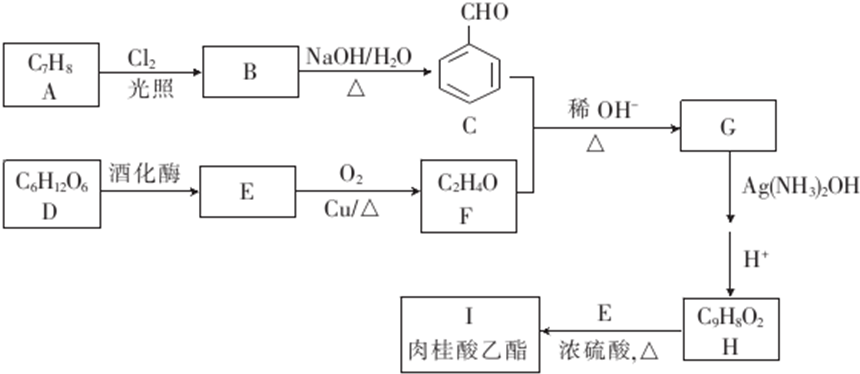
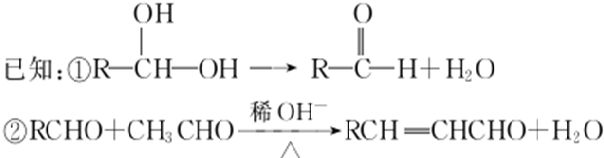
 ,E→F的反应类型是氧化反应.
,E→F的反应类型是氧化反应. .
.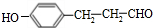 .
.查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 电解精炼铜,当电路中通过的电子数为0.1NA时,阳极质量减少一点为3.2g | |
| B. | 0.5L1mol•L-1NaHS的溶液中,Na+和HS-离子数目之和为NA | |
| C. | 25℃时,7gC2H4和C2H6混合气体中,含有NA个C-H键 | |
| D. | 标况下,11.2L一氯甲烷中含有的氯原子数为0.5NA |
查看答案和解析>>
科目: 来源: 题型:填空题
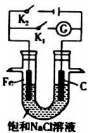
查看答案和解析>>
科目: 来源: 题型:解答题
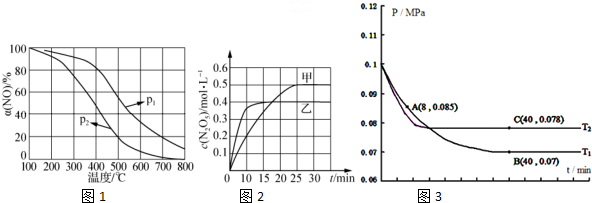
| 容器 | 甲 | 乙 | 丙 |
| 容积/L | 1 | 1 | 2 |
| 反应物起始量 | 1molO3、2molO2 | ||
| 1molO3、2molNO2 | |||
| 1molO3、2molN2O5 | |||
| 温度/K | T1 | T2 | T2 |
查看答案和解析>>
科目: 来源: 题型:解答题
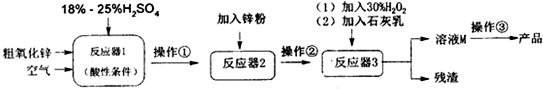
查看答案和解析>>
科目: 来源: 题型:多选题
| A. | 二氧化硅是生产光纤制品的基本原料 | |
| B. | 水玻璃可用于生产黏合剂和防火剂 | |
| C. | 高锰酸钾可用于医药上消毒剂 | |
| D. | 碳酸钠可用于洗涤剂 |
查看答案和解析>>
科目: 来源: 题型:解答题
| 含氧官能团名称 | |||
| 含氧官能团数目 |
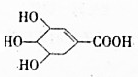 ”,你认为这种结构是否存在:是,该物质在一定条件下能(填“能”或“不能”)发生分子内的酯化反应,作出此判断的理由是含有羟基和羧基.
”,你认为这种结构是否存在:是,该物质在一定条件下能(填“能”或“不能”)发生分子内的酯化反应,作出此判断的理由是含有羟基和羧基.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com