
科目: 来源: 题型:选择题
| A. | CH3Cl只代表一种物质 | B. | CH2Cl2只代表一种物质 | ||
| C. | CHCl3只代表一种物质 | D. | CCl4是非极性分子 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 原子半径X>Y>Z | B. | 气态氢化物稳定性 HX>HZ>HY | ||
| C. | 非金属性X>Y>Z | D. | 气态氢化物还原性HX>HY>HZ |
查看答案和解析>>
科目: 来源: 题型:填空题
查看答案和解析>>
科目: 来源: 题型:实验题
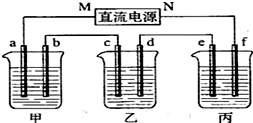
查看答案和解析>>
科目: 来源: 题型:填空题
 是地球上最常见的物质之一,是所有生命体生存的重要资源,约占人体体重的三分之二.
是地球上最常见的物质之一,是所有生命体生存的重要资源,约占人体体重的三分之二. 无色,无气味并且易燃.是常见的一种化石能源.
无色,无气味并且易燃.是常见的一种化石能源. 有强氧化性的弱酸,见光易分解,具有漂白性,可以用于消毒杀菌.
有强氧化性的弱酸,见光易分解,具有漂白性,可以用于消毒杀菌.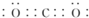 .
.查看答案和解析>>
科目: 来源: 题型:推断题
| 元素 | 相关信息 |
| X | X的基态原子L层电子数是K层电子数的2倍 |
| Y | Y是地壳中含量最高的元素 |
| Z | Z的基态原子最外层电子排布式为3s23p1 |
| W | W有多种化合价,其白色氢氧化物在空气中会迅速变成灰绿色,最后变成红褐色 |
 ;
;查看答案和解析>>
科目: 来源: 题型:推断题
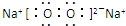 ,AB2所含化学键的类型:离子键、非极性共价键(极性共价键、非极性共价键、离子键).
,AB2所含化学键的类型:离子键、非极性共价键(极性共价键、非极性共价键、离子键).查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 原子半径:W>Z>Y>X | |
| B. | Y元素在周期表中的位置为第三周期第ⅣA族 | |
| C. | 1 mol甲与足量的乙完全反应共转移了1 mol电子 | |
| D. | 1.0 L 0.1 mol•L-1戊溶液中阴离子总的物质的量小于0.1 mol |
查看答案和解析>>
科目: 来源: 题型:推断题
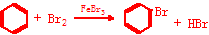 .
.查看答案和解析>>
科目: 来源: 题型:选择题
| A. | NaCl固体(CaCl2):溶解,加Na2CO3溶液、过滤后加适量盐酸,最后蒸发结晶 | |
| B. | KCl固体(MnO2):溶解、过滤、蒸发结晶 | |
| C. | NaCl溶液(I2):加酒精,萃取、分液 | |
| D. | KNO3溶液(I2):加四氯化碳,萃取、分液 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com